Với giải sách bài tập Khoa học tự nhiên 9 Bài 15: Tính chất chung của kim loại sách Cánh diều hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Khoa học tự nhiên 9. Mời các bạn đón xem:
Giải SBT Khoa học tự nhiên 9 Bài 15: Tính chất chung của kim loại
Bài 15.1 trang 45 Sách bài tập KHTN 9: Kim loại có thể kéo dài thành sợi, dễ dát mỏng hoặc uốn cong do có
A. tính dẫn điện.
B. ánh kim.
C. tính dẻo.
D. tính dẫn nhiệt.
Lời giải:
Đáp án đúng là: C
Kim loại có thể kéo dài thành sợi, dễ dát mỏng hoặc uốn cong do có tính dẻo.
Bài 15.2 trang 45 Sách bài tập KHTN 9: Hai kim loại nào sau đây thường được sử dụng làm dây dẫn điện?
A. Sắt, vàng.
B. Nhôm, chì.
C. Nhôm, bạc.
D. Nhôm, đồng.
Lời giải:
Đáp án đúng là: D
Nhôm và đồng thường được sử dụng làm dây dẫn điện.
Vàng và bạc tuy dẫn điện tốt nhưng không được sử dụng làm dây dẫn điện do giá thành đắt và là kim loại nặng.
Bài 15.3 trang 45 Sách bài tập KHTN 9: Ở điều kiện thường, dãy các kim loại nào sau đây có khả năng dẫn điện giảm dần theo chiều từ trái qua phải?
A. Ag, Cu, Fe, Al, Au.
B. Ag, Cu, Au, Al, Fe.
C. Au, Ag, Cu, Al, Fe.
D. Al, Cu, Fe, Au, Ag.
Lời giải:
Đáp án đúng là: B
Ở điều kiện thường, dãy các kim loại có khả năng dẫn điện giảm dần theo chiều từ trái qua phải là: Ag, Cu, Au, Al, Fe.
Bài 15.4 trang 45 Sách bài tập KHTN 9: Vẻ sáng lấp lánh của các kim loại ở điều kiện thường được gọi là
A. tính dẫn điện.
B. ánh kim.
C. tính dẫn nhiệt.
D. tính dẻo.
Lời giải:
Đáp án đúng là: B
Vẻ sáng lấp lánh của các kim loại ở điều kiện thường được gọi là ánh kim.
Bài 15.5 trang 45 Sách bài tập KHTN 9: Tungsten (W) được dùng để làm sợi đốt bóng đèn là do kim loại này có tính chất vật lí đặc trưng là
A. độ cứng cao.
B. nhiệt độ nóng chảy cao.
C. có ánh kim.
D. dẫn điện tốt.
Lời giải:
Đáp án đúng là: B
Tungsten (W) được dùng để làm sợi đốt bóng đèn là do kim loại này có tính chất vật lí đặc trưng là nhiệt độ nóng chảy cao.
Bài 15.6 trang 45 Sách bài tập KHTN 9: Kim loại nào là chất lỏng ở điều kiện thường, có màu trắng bạc, thường được dùng trong nhiệt kế, áp kế?
A. Bạc.
B. Nhôm.
C. Thuỷ ngân.
D. Đồng.
Lời giải:
Đáp án đúng là: C
Kim loại thuỷ ngân là chất lỏng ở điều kiện thường, có màu trắng bạc, thường được dùng trong nhiệt kế, áp kế.
Bài 15.7 trang 45 Sách bài tập KHTN 9: Nhôm là kim loại được dùng để chế tạo dụng cụ nhà bếp (nồi, xoong, ấm, chảo, …). Có ứng dụng này là do nhôm bền, không độc và có tính chất vật lí ưu việt là
A. dẫn điện tốt.
B. mềm, dẻo.
C. có ánh kim.
D. dẫn nhiệt tốt.
Lời giải:
Đáp án đúng là: D
Nhôm là kim loại được dùng để chế tạo dụng cụ nhà bếp (nồi, xoong, ấm, chảo, …). Có ứng dụng này là do nhôm bền, không độc và có tính chất vật lí ưu việt là dẫn nhiệt tốt.
Bài 15.8 trang 46 Sách bài tập KHTN 9: Kim loại nào sau đây có độ cứng cao nhất trong các kim loại, thường được dùng để chế tạo hợp kim không gỉ, có độ bền cơ học cao?
A. Chromium.
B. Nhôm.
C. Sắt.
D. Đồng.
Lời giải:
Đáp án đúng là: A
Chromium có độ cứng cao nhất trong các kim loại, thường được dùng để chế tạo hợp kim không gỉ, có độ bền cơ học cao.
Bài 15.9 trang 46 Sách bài tập KHTN 9: Ở điều kiện thường, cho biết: Khối lượng riêng của nước là 1,00 g/cm3. Khối lượng riêng của các kim loại K, Na, Mg, Fe lần lượt là 0,86 g/cm3; 0,97 g/cm3; 1,74 g/cm3; 7,90 g/cm3. Khi cho từng mẫu kim loại trên vào nước, số kim loại nổi trên nước là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: B
Các kim loại K (DK = 0,86 g/cm3), Na (DNa = 0,97 g/cm3) có khối lượng riêng nhỏ hơn khối lượng riêng của nước (1 gam/cm3) nên nhẹ hơn nước và nổi trên nước.
Bài 15.10 trang 46 Sách bài tập KHTN 9: Cặp kim loại nào sau đây đều phản ứng với nước ở nhiệt độ thường?
A. Na, Al.
B. Al, Cu.
C. K, Na.
D. Mg, K.
Lời giải:
Đáp án đúng là: C
Cặp kim loại K, Na đều phản ứng với nước ở điều kiện thường.
2K + 2H2O → 2KOH + H2
2Na + 2H2O → 2NaOH + H2
Bài 15.11 trang 46 Sách bài tập KHTN 9: Thực hiện các thí nghiệm sau:
(1) Cho Zn vào dung dịch H2SO4.
(2) Cho Ag vào dung dịch H2SO4.
(3) Cho Fe vào dung dịch CuSO4
(4) Cho Cu vào dung dịch FeSO4.
a) Trong các thí nghiệm trên, số thí nghiệm xảy ra phản ứng là
A. 1.
B. 2.
C. 3.
D. 4.
b) Viết phương trình hoá học của các phản ứng xảy ra.
Lời giải:
a) Đáp án đúng là: B
Các phản ứng (1) và (3) xảy ra.
b) Viết phương trình hoá học của các phản ứng xảy ra:
Zn + H2SO4 → ZnSO4 + H2↑
Fe + CuSO4 → FeSO4 + Cu.
Bài 15.12 trang 46 Sách bài tập KHTN 9: Chọn các chất thích hợp để điền vào dấu ? và hoàn thành các phương trình hoá học sau:
a) ? + HCl → ZnCl2 + H2↑
b) ? + CuSO4 → FeSO4 + Cu
c) ? + O2 CuO
d) S + ? FeS
e) Zn + ? ZnO + H2↑
Lời giải:
a) Zn + 2HCl → ZnCl2 + H2↑
b) Fe + CuSO4 → FeSO4 + Cu
c) 2Cu + O2 2CuO
d) S + Fe FeS
e) Zn + H2O ZnO + H2↑
Bài 15.13 trang 47 Sách bài tập KHTN 9: Quan sát hình 15.1, mô tả các hiện tượng thí nghiệm. Rút ra nhận xét về khả năng phản ứng của kim loại với các dung dịch acid (HCl, H2SO4 loãng, …) và sắp xếp khả năng phản ứng theo chiều giảm dần.
Lời giải:
Hiện tượng:
- Khi cho đồng vào ống nghiệm chứa các dung dịch acid (HCl, H2SO4 loãng, …) không thấy hiện tượng gì xuất hiện.
- Khi cho natri vào ống nghiệm chứa các dung dịch acid (HCl, H2SO4 loãng, …) thấy phản ứng xảy ra mãnh liệt, kim loại chuyển động xung quanh bề mặt dung dịch và bốc cháy.
- Khi cho chì vào ống nghiệm chứa các dung dịch acid (HCl, H2SO4 loãng, …) thấy có khí thoát ra chậm.
- Khi cho magnesium vào ống nghiệm chứa các dung dịch acid (HCl, H2SO4 loãng, …) thấy sủi bọt khí mãnh liệt, kim loại tan dần.
- Khi cho sắt vào ống nghiệm chứa các dung dịch acid (HCl, H2SO4 loãng, …) thấy có khí thoát ra mạnh nhưng êm dịu hơn so với khi cho magnesium vào ống nghiệm chứa các dung dịch acid (HCl, H2SO4 loãng, …).
Nhận xét: Nhiều kim loại tác dụng được với các dung dịch acid (HCl, H2SO4 loãng, …) tạo thành muối và giải phóng khí H2.
Sắp xếp khả năng phản ứng theo chiều giảm dần: Natri, Magnesium, Sắt, Chì, Đồng.
Bài 15.14 trang 47 Sách bài tập KHTN 9: Hình 15.2 mô tả thí nghiệm điều chế và thu khí H2 bằng phương pháp đẩy không khí.
a) Viết phương trình hoá học của phản ứng xảy ra.
b) Vì sao để thu khí H2 bằng cách đẩy không khí ta phải úp ngược ống nghiệm?
Ngoài cách trên, còn có cách thu khí H2 nào khác không? Nêu và giải thích cách thu đó (nếu có).
Lời giải:
a) Phương trình hoá học của phản ứng xảy ra:
Zn + 2HCl → ZnCl2 + H2
b) Do khí H2 nhẹ hơn không khí nên để thu khí H2 bằng cách đẩy không khí ta phải úp ngược ống nghiệm.
Ngoài cách đẩy không khí, có thể thu khí H2 bằng cách đẩy nước do H2 không tác dụng với nước.
Lý thuyết Tính chất chung của kim loại
I. Tính chất vật lí của kim loại
1. Tính dẻo
- Kim loại có tính dẻo nên có thể rèn, kéo dài thành sợi hoặc dát mỏng.
- Những kim loại có tính dẻo cao là Au, Ag, Al, Cu, Fe.
2. Tính dẫn điện
Các kim loại có khả năng dẫn điện khác nhau. Kim loại dẫn điện tốt nhất là Ag, Cu, Au, Al,…
3. Tính dẫn nhiệt
Kim loại có tính dẫn nhiệt, các kim loại thường có khả năng dẫn nhiệt khác nhau.
4. Ánh kim
Kim loại có tính ánh kim nên một số kim loại được dùng làm đồ trang sức và các vật dụng trang trí khác
5. Một số tính chất vật lí khác của kim loại
- Khối lượng riêng
- Nhiệt độ nóng chảy
- Tính cứng
II. Tính chất hóa học
1. Phản ứng của kim loại với phi kim
- Tác dụng với oxygen
Nhiều kim loại khác như Ca, Fe, Cu,…có phản ứng với O2 tạo thành các oxide
Ví dụ: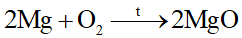
- Tác dụng với phi kim khác
Ở nhiệt độ cao, các kim loại Mg, Cu, Fe, Al,… có phản ứng với S, Cl2 cho sản phẩm là các muối sulfide, chlorua.
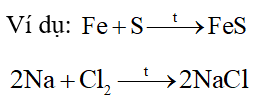
2. Phản ứng của kim loại với dung dịch acid
- Nhiều kim loại phản ứng với các dung dịch acid (HCl, H2SO4 loãng,…) tạo thành muối và giải phóng khí H2
Ví dụ: 2Al + 6HCl 2AlCl3 + 3H2
- Một số kim loại như Cu, Ag, Au,… không tác dụng với dung dịch acid (HCl, H2SO4 loãng,…)
3. Phản ứng của kim loại với dung dịch muối
- Kim loại hoạt động hóa học mạnh (trừ các kim loại K, Na, Ca,…) có thể đẩy được kim loại có mức hoạt động hóa học yếu hơn ra khỏi dung dịch muối, tạo thành muối mới và kim loại mới
Ví dụ: Fe + CuSO4 FeSO4 + Cu
4. Phản ứng với nước
- Một số kim loại như K, Na, Ca,… tác dụng được với nước ở nhiệt độ thường tạo thành hydroxide và khí H2
Ví dụ: 2Na + H2O 2NaOH + H2
III. Sự khác biệt về tính chất của một số kim loại
- Nhôm là kim loại có màu trắng bạc, khá mềm, dẫn nhiệt, dẫn điện tốt và nhẹ. Nhôm tác dụng với nhiều phi kim, nhiều dung dịch acid, dung dịch muối,…Tuy nhiên, nhôm bền trong môi trường không khí và nước do có lớp màng Al2O3 bền vững bảo vệ
- Sắt có màu trắng hơi xám, có tính dẻo, có độ cứng và có tính nhiễm từ.
- Vàng là kim loại có tính dẻo, tính dẫn điện, dẫn nhiệt rất tốt, có màu vàng, lấp lánh. Vàng bền trong không khí, không bị hòa tan trong dung dịch HCl, H2SO4
Sơ đồ tư duy Tính chất chung của kim loại
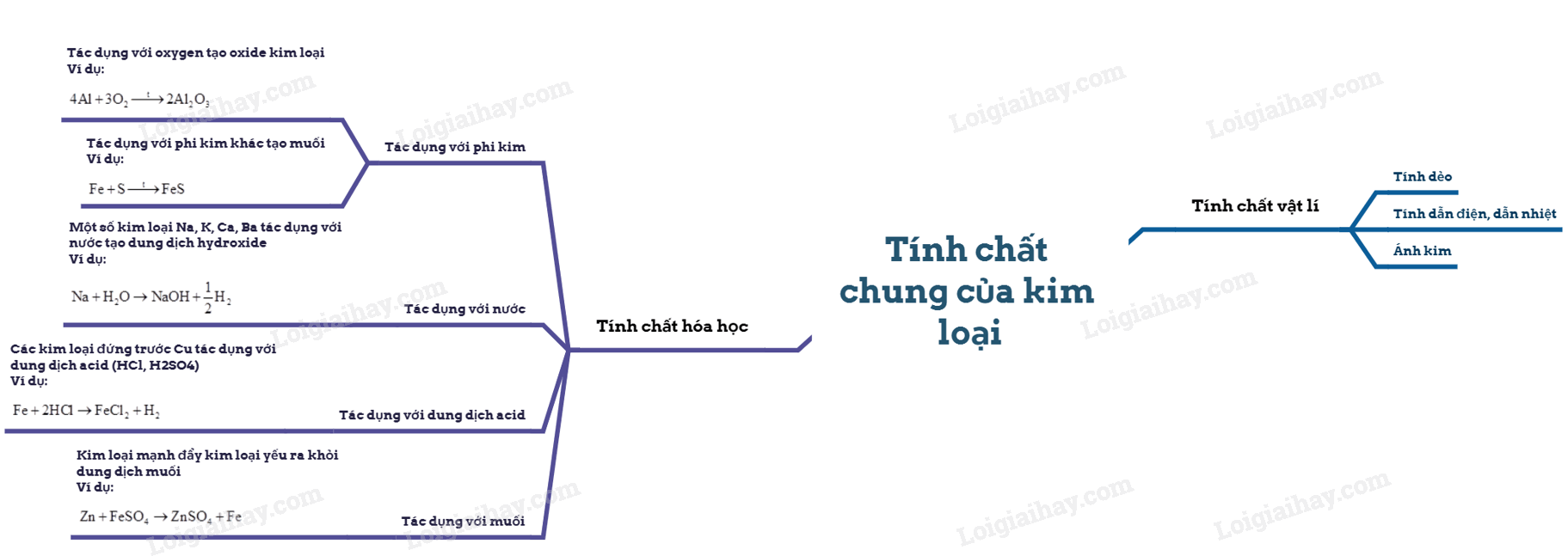
Xem thêm các bài giải SBT Khoa học tự nhiên 9 Cánh diều hay, chi tiết khác:
Bài 15: Tính chất chung của kim loại
Bài 17: Tách kim loại. Sử dụng hợp kim