Tailieumoi.vn giới thiệu Giải bài tập Hóa Học lớp 11 Bài 9: Axit nitric và muối nitrat chính xác, chi tiết nhất giúp học sinh dễ dàng làm bài tập Axit nitric và muối nitrat lớp 11.
Giải bài tập Hóa Học lớp 11 Bài 9: Axit nitric và muối nitrat
Bài 1 trang 45 sgk hóa học 11: Viết công thức electron, công thức cấu tạo của axit nitric. Cho biết nguyên tố nitơ có hóa trị và số oxi hóa bao nhiêu ?
Trả lời:
Công thức electron của HNO3:
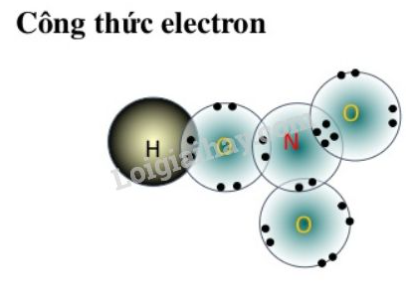
Công thức cấu tạo phân tử HNO3:
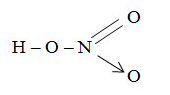
Trong HNO3, nitơ có số oxi hóa +5 và hóa trị là 4.
Bài 2 trang 45 sgk hóa học 11: Lập các phương trình hóa học:
a) Ag + HNO3 (đặc) → NO2 ↑ + ? + ?
b) Ag + HNO3 (loãng) → NO ↑ + ? + ?
c) Al + HNO3 → N2O ↑ + ? + ?
d) Zn + HNO3 → NH4NO3 + ? + ?
e) FeO + HNO3 → NO ↑ + Fe(NO3)3 + ?
g) Fe3O4 + HNO3 → NO ↑ + Fe(NO3)3 + ?
Phương pháp giải:
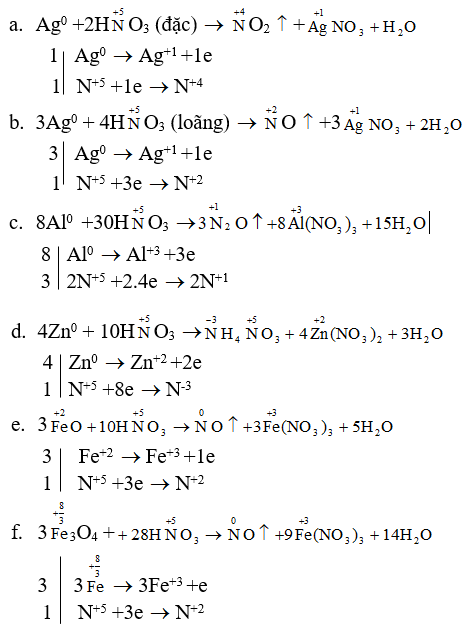
Bài 3 trang 45 sgk hóa học 11: Hãy chỉ ra những tính chất hóa học chung và khác biệt giữa axit nitric và axit sunfuric. Viết các phương trình hóa học để minh họa.
Phương pháp giải:
- Chỉ ra những tính chất chung: có tính axit mạnh
- Tính chất riêng: HNO3 và H2SO4 đặc có tính oxi hóa mạnh
Trả lời:
- Những tính chất chung:
- Với axit H2SO4 loãng và HNO3 đều có tính axit mạnh
+ Làm quỳ tím đổi sang màu đỏ
+ Tác dụng với bazơ, oxit bazơ không có tính khử (các nguyên tố có số oxi hoá cao nhất):
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3+ 6H2O
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2↑
H2SO4 + Na2SO3 → Na2SO4 + H2O + SO2↑
- Với axit H2SO4(đặc) và axit HNO3 đều có tính oxi hoá mạnh
+ Tác dụng được với hầu hết các kim loại (kể cả kim loại đứng sau hiđro trong dãy hoạt động hoá học) và đưa kim loại lên số oxi hoá cao nhất.
Fe + 4HNO3 → Fe(NO3)3 + NO↑ + 2H2O
Cu + 2H2SO4(đặc) → CuSO4 + SO2↑ + 2H2O
+ Tác dụng với một số phi kim (đưa phi kim lên số oxi hoá cao nhất)
C + 2H2SO4(đặc) → CO2↑ + 2SO2↑ + 2H2O
S + 2HNO3 → H2SO4 + 2NO↑
+ Tác dụng với hợp chất( có tính khử)
3FeO + 10HNO3 → 3Fe(NO3)3 + NO↑ + 5H2O
2Fe(OH)2 + 4H2SO4(đặc) → Fe2(SO4)3 + SO2↑ + H2O
Cả hai axit khi làm đặc nguội đều làm Fe và Al bị thụ động hoá (có thể dùng bình làm bằng nhôm và sắt để đựng axit nitric và axit sunfuaric đặc)
- Những tính chất khác biệt:
- Với axit H2SO4 loãng có tính axit, còn H2SO4 đặc mới có tính oxi hoá mạnh, còn axit HNO3 dù là axit đặc hay loãng đề có tính oxi hoá mạnh khi tác dụng với các chất có tính khử.
- H2SO4 loãng không tác dụng được với các kim loại đứng sau hiđro trong dãy hoạt động hoá học như axit HNO3.
Fe + H2SO4 (loãng) → FeSO4 + H2↑
Cu + H2SO4 (loãng) : không có phản ứng
Bài 4 trang 45 sgk hóa học 11: a) Trong phương trình hóa học của phản ứng nhiệt phân sắt (III) nitrat, tổng các hệ số bằng bao nhiêu ?
A. 5 B. 7
C. 9 D. 21
b) Trong phương trình hóa học của phản ứng nhiệt phân thủy ngân (II) nitrat, tổng các hệ số bằng bao nhiêu ?
A. 5 B. 7
C. 9 D. 21
Phương pháp giải:
a) Phương trình nhiệt phân
4Fe(NO3)3 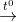 2Fe2O3 + 12NO2 + 3O2
2Fe2O3 + 12NO2 + 3O2
Vậy tổng hệ số là 4 + 2 + 12 + 3 = 21
Đáp án D
b) Phương trình nhiệt phân
Hg(NO3)3 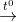 Hg + 2NO2 + O2
Hg + 2NO2 + O2
Vậy tổng hệ số là 1 + 1 + 2 + 1 = 5
Đáp án A
Lưu ý: Phản ứng nhiệt phân muối nitrat
+ Các muối nitrat của kim loại hoạt động mạnh (K, Na,…) bị phân hủy tạo muối nitrit và O2
+ Các muối nitrat của kim loại Mg, Zn, Fe, Cu, Pb,… bị phân hủy tạo oxit kim loại tương ứng, NO2 và O2
+ Muối nitrat của Ag, Au, Hg,… bị phân hủy tạo thành kim loại tương ứng, NO2 và O2
Bài 5 trang 45 sgk hóa học 11: Viết phương trình hóa học của các phản ứng thực hiện dãy chuyển hóa sau đây:
NO2 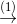 HNO3
HNO3 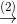 Cu(NO3)2
Cu(NO3)2 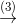 Cu(OH)2
Cu(OH)2 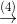 Cu(NO3)2
Cu(NO3)2 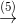 CuO
CuO 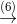 Cu
Cu 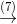 CuCl2
CuCl2
Trả lời:
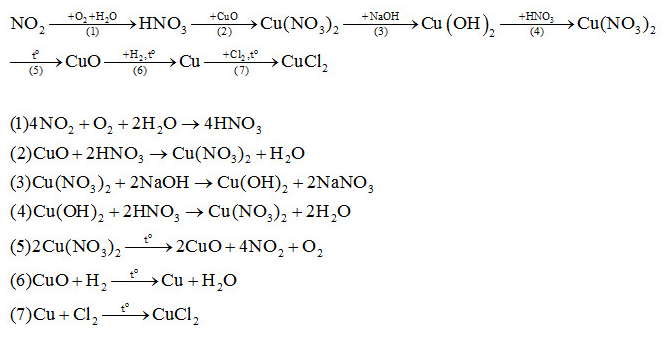
Bài 6 trang 45 sgk hóa học 11: Khi hòa tan 30,0 g hỗn hợp đồng và đồng(II) oxit trong 1,50 lít dung dịch axit nitric 1,00M (loãng) thấy thoát ra 6,72 lít nitơ monooxit (đktc). Xác định hàm lượng phần trăm của đồng(II) oxit trong hỗn hợp, nồng độ mol của đồng(II) nitrat và axit nitric trong dung dịch sau phản ứng, biết rằng thể tích dung dịch không thay đổi.
Phương pháp giải:

Bài 7 trang 45 sgk hóa học 11: Để điều chế 5,000 tấn axit nitric nồng độ 60,0 % cần dùng bao nhiêu tấn amoniac ?
Biết rằng sự hao hụt amoniac trong quá trình sản xuất là 3,8 %.
Trả lời:

Lý thuyết Bài 9: Axit nitric và muối nitrat
A. AXIT NITRIC
I. CẤU TẠO
- Trong hợp chất HNO3, nguyên tố nitơ có số oxi hóa cao nhất là +5
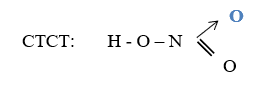
II. TÍNH CHẤT VẬT LÍ
- Axit nitric tinh khiết là chất lỏng không màu, bốc khói mạnh trong không khí ẩm.
- Axit HNO3 tan vô hạn trong nước.
- Axit nitric kém bền. Trong điều kiện thường, có ánh sáng, dung dịch axit đặc bị phân hủy 1 phần giải phóng khí nito dioxit, khí này lại tan trong dung dịch axit làm cho dung dịch có màu vàng
4HNO3 → 4NO2 + O2 + 2H2O
III. TÍNH CHẤT HÓA HỌC
1. Axit HNO3 là một trong các axit mạnh
- Làm quỳ tím hóa đỏ, tác dụng với bazơ và oxit bazơ, tác dụng với muối của axit yếu.
VD:
CuO + 2HNO3 → Cu(NO3)2 + H2O
Ba(OH)2 + 2HNO3 → Ba(NO3)2 + 2H2O
CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O
2. Axit HNO3 là chất oxi hóa mạnh
* Phản ứng với hầu hết các kim loại trừ Pt và Au,
VD:
Cu + 4HNO3 đặc → Cu(NO3)2 + 2NO2 + 2H 2O
* Một số phi kim, nhiều hợp chất vô cơ và hữu cơ.
(Một số hợp chất hữu cơ bốc cháy khi gặp HNO3 đặc)
VD:
C + 4HNO3 (đ) CO2 + 4NO2 + 2H2O
3FeO + 10HNO3 (đ) → 3Fe(NO3)3 + NO + 5H2O
- Sản phẩm khử sinh ra tùy thuộc nồng độ axit, tính khử của kim loại và nhiệt độ phản ứng.
* Lưu ý: Al, Fe, Cr bị thụ động trong HNO3 đặc nguội.
IV. ĐIỀU CHẾ
1. Trong phòng thí nghiệm
Axit HNO3 được điều chế bằng cách cho NaNO3 hoặc KNO3 tác dụng với axit H2SO4 đăc, nóng:
2NaNO3(tt) + H2SO4(đ) Na2SO4 + 2HNO3
2. Trong công nghiệp
Được sản xuất theo sơ đồ sau:
N2 NH3 NO NO2 HNO3
B. MUỐI NITRAT
I. TÍNH CHẤT VẬT LÍ
Tất cả các muối nitrat đều tan nhiều trong nước và là chất điện li mạnh.
II. TÍNH CHẤT HÓA HỌC
Các muối nitrat kém bền với nhiệt, chúng bị phân hủy khi đun nóng
- Muối nitrat của các kim loại hoạt động mạnh đứng trước Mg (kali, natri,…) bị phân hủy thành muối nitrit và oxit
VD: 2KNO3 2KNO2 + O2
- Muối nitrat của kim loại từ Mg đến Cu bị phân hủy thành oxit kim loại tương ứng, NO2 và O2
VD: 2Cu(NO3)2 2CuO + 4NO2 + O2
- Muối nitrat của kim loại kém hoạt động (Sau Cu) bị phân hủy thành kim loại tương ứng, khí NO2 và O2.
VD: 2AgNO3 2Ag + 2NO2 + O2
III. NHẬN BIẾT ION NITRAT
- Trong môi trường axit, ion NO3- thể hiện tính oxi hóa giống như HNO3. Do đó thuốc thử dùng để nhận biết ion NO3- là hỗn hợp vụn đồng và dung dịch H2SO4 loãng, đun nóng.
- Hiện tượng: dung dịch có màu xanh, khí không màu hóa nâu đỏ trong không khí.
3Cu + 8H+ + 2NO3- → 3Cu2+ (dd màu xanh) + 2NO↑ + 4H2O
2NO + O2 (không khí) → 2NO2 (màu nâu đỏ)
IV. ỨNG DỤNG
- Các muối nitrat được sử dụng chủ yếu làm phân bón hóa học (phân đạm) trong nông nghiệp như NH4NO3, NaNO3, KNO3.
- KNO3 còn được sử dụng để chế thuốc nổ đen.
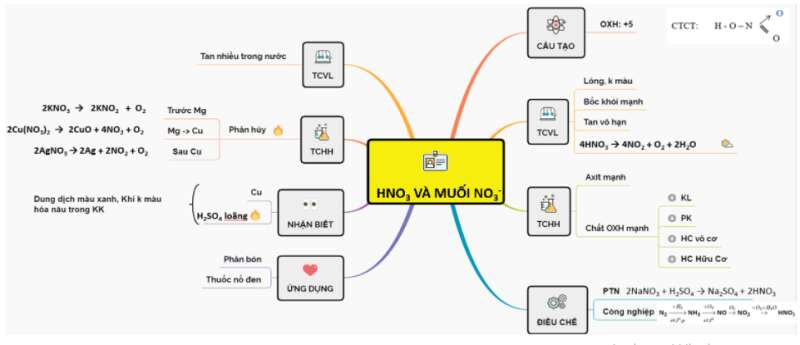
Sơ đồ tư duy: Axit nitric và muối nitrat.
Phương pháp giải một số dạng bài tập về Axit nitric - Muối nitrat
Dạng 1: Lý thuyết về tính chất của axit nitric và muối nitrat
* Một số lưu ý cần nhớ:
- Axit nitric là chất lỏng không màu, bốc khói mạnh trong không khí ẩm, không bền và dễ bị phân hủy khi có ánh sáng
- Axit nitric có tính axit và tính OXH mạnh (có thể oxh hầu hết các kim loại từ Au, Pt)
- Trong phòng thí nghiệm, người ta cho NaNO3 (rắn) tác dụng với H2SO4 (đặc) để thu được HNO3 (khí); trong công nghiệp người ta sản xuất HNO3 bằng khí NH3.
- Tất cả các muối nitrat có khả năng tan được trong nước
Khi nhiệt phân muối nitrat
- Nếu muối nitrat của kim loại đứng trước Mg → muối nitrit và O2
- Nếu muối của kim loại trung bình (từ Mg đến Cu) → oxit kim loại + NO2 + O2
- Nếu muối nitrat của kim loại sau Cu → kim loại + NO2 + O2
* Một số ví dụ điển hình:
Ví dụ 1: Thí nghiệm với dung dịch HNO3 thường sinh ra khí độc NO2. Để hạn chế khí NO2 thoát ra từ ống nghiệm, người ta nút ống nghiệm bằng
(a) bông khô
(b) bông có tẩm nước
(c) bông có tẩm nước vôi trong
(d) bông có tẩm giấm ăn
Trong 4 biện pháp trên, biện pháp có hiệu quả nhất là:
A. (b)
B. (a)
C. (d)
D. (c)
Hướng dẫn giải chi tiết
Trong 4 biện pháp trên, biện pháp có hiệu quả nhất là dùng bông có tẩm nước vôi trong để nút vào ống nghiệm.
2Ca(OH)2 + 4NO2 → Ca(NO3)2 + Ca(NO2)2 + 2H2O
Đáp án D
Ví dụ 2: Cho các mệnh đề sau :
1) Các muối nitrat đều tan trong nước và đều là chất điện li mạnh.
2) Ion NO3- có tính oxi hóa trong môi trường axit.
3) Khi nhiệt phân muối nitrat rắn ta đều thu được khí NO2.
4) Hầu hết muối nitrat đều bền nhiệt.
Các mệnh đề đúng là :
A. (1), (2), (3).
B. (2) và (4).
C. (2) và (3).
D. (1) và (2).
Hướng dẫn giải chi tiết:
Các mệnh đề đúng là: (1) và (2)
(3) sai vì muối nitrat của K, Na, Ba, Ca nhiệt phân không thu được khí NO2
(4) sai vì các muối nitrat hầu hết kém bền nhiệt
Đáp án D.
Ví dụ 3: Khi cho kim loại Fe phản ứng với HNO3 tạo thành khí độc hại. Biện pháp nào xử lý tốt nhất để chống ô nhiễm môi trường ?
A. Nút ống nghiệm bằng bông tẩm nước.
B. Nút ống nghiệm bằng bông tẩm cồn
C. Nút ống nghiệm bằng bông tẩm giấm.
D. Nút ống nghiệm bằng bông tẩm xút.
Hướng dẫn giải chi tiết:
Khí sinh ra là NO2 => cần dung dịch kiềm để hấp thụ => nút ống nghiệm bằng bông tẩm xút.
Đáp án D
Dạng 2: Bài toán về axit nitric
a, Bài toán kim loại tác dụng với axit nitric
* Một số lưu ý cần nhớ
- HNO3 tác dụng với hầu hết các kim loại (trừ Au, Pt) để sinh ra muối + sản phẩm khử + H2O
- Sản phẩm khử của phản ứng này thường là: NH4NO3; N2O; NO; NO2; N2
- n e trao đổi = n NO2 + 3 . n NO + 8 . n N2O + 8 . n NH4+ + 10 . n N2
n HNO3 = 2 . n NO2 + 4 . n NO + 10 . n N2O + 10 . n NH4NO3 + 12 . n N2
Trường hợp sản phẩm không sinh ra muối NH4NO3 ta có n e trao đổi = n NO3
Đối với dạng bài tập này, ta thường áp dụng định luật bảo toàn electron, bảo toàn điện tích và bảo toàn khối lượng để giải quyết yêu cầu của đề bài.
* Một số ví dụ điển hình
Ví dụ 1: Hòa tan hoàn toàn m gam Al trong dung dịch HNO3 loãng thu được 1,12 lít hỗn hợp X gồm 3 khí NO, N2O, N2 có tỉ lệ số mol là: 1 : 2 : 2. Giá trị của m là :
A. 5,4 gam.
B. 3,51 gam.
C. 2,7 gam.
D. 8,1 gam.
Hướng dẫn giải chi tiết
Ta có số mol của hỗn hợp khí thu được sau phản ứng là: 1,12 : 22,4 = 0,05 (mol)
Theo đề bài, tỉ lệ mol của 3 khí NO; N2O; N2 là 1 : 2 : 2
=> n NO = 0,01 mol; n N2O = 0,02 mol; n N2 = 0,02 mol.
Áp dụng định luật bảo toàn electron:
3 . n Al = 3 . n NO + 8 . n N2O + 10 . n N2 = 3 . 0,01 + 0,02 . 8 + 0,02 . 10 = 0,39
=> n Al = 0,13 mol => m Al = 3,51 gam
Đáp án B.
Ví dụ 2: Cho m gam bột Fe vào dung dịch HNO3 lấy dư, ta được hỗn hợp gồm hai khí NO2 và NO có VX = 8,96 lít (đktc) và tỉ khối đối với O2 bằng 1,3125. Thành phần phần trăm theo thể tích của NO, NO2 và khối lượng m của Fe đã dùng là :
A. 25% và 75% ; 1,12 gam.
B. 25% và 75% ; 11,2 gam.
C. 35% và 65% ; 11,2 gam.
D. 45% và 55% ; 1,12 gam.
Hướng dẫn giải chi tiết:
Theo đề bài, ta tính được n X = 0,4 mol
Khối lượng mol trung bình của X là: 1,3125 . 32 = 42 (gam/mol)
Gọi số mol NO; NO2 lần lượt là x, y mol
=> Ta có hệ phương trình:
x + y = 0,4
(30x + 46y) : (x + y) = 42
=> x = 0,1 ; y = 0,3
% V NO = 0,1 : 0,4 . 100% = 25%
% V NO2 = 0,3 : 0,4 . 100% = 75%
Áp dụng định luật bảo toàn electron vào hệ trên ta sẽ có được:
3 . n Fe = 3 . n NO + n NO2
=> n Fe = (3 . 0,1 + 0,3 ) : 3 = 0,2 mol
=> m Fe = 0,2 . 56 = 11,2 gam.
Đáp án B
Ví dụ 3: Cho 1,35 gam hỗn hợp gồm Cu, Mg, Al tác dụng với dung dịch HNO3 dư, thu được 1,12 lít (đktc) hỗn hợp khí NO và NO2 có tỉ khối so với hiđro bằng 20. Tổng khối lượng muối nitrat sinh ra là :
A. 66,75 gam.
B. 33,35 gam.
C. 6,775 gam.
D. 3,335 gam.
Hướng dẫn giải chi tiết:
n hỗn hợp khí = 1,12 : 22,4 = 0,05 mol
Khối lượng mol trung bình của hỗn hợp khí là: 20 . 2 = 40 (gam/mol)
Gọi số mol của NO; NO2 lần lượt là x , y mol
Ta có hệ phương trình:
x + y = 0,05
(30x + 46y) : (x + y) = 40
=> x = 0,01875 ; y = 0,03225
=> số mol e trao đổi là: 3x + y = 0,0875 (mol)
=> m muối tạo thành sau phản ứng là: m Fe + m NO3- = 1,35 + 0,0875 . 62 = 6,775 gam
Đáp án C.
b, Bài toán hợp chất tác dụng với axit nitric
Ví dụ 1: Hoà tan đến phản ứng hoàn toàn 0,1 mol FeS2 vào HNO3 đặc nóng dư. Thể tích NO2 bay ra (ở đktc, biết rằng N+4 là sản phẩm khử duy nhất của N+5) là
Hướng dẫn giải chi tiết:
Xét quá trình cho – nhận e:
=> VNO2 = 1,5.22,4 = 33,6 lít
Ví dụ 2: Trộn 0,81 gam bột nhôm với bột Fe2O3 và CuO rồi đốt nóng để tiến hành phản ứng nhiệt nhôm thu được hỗn hợp A. Hoà tan hoàn toàn A trong dung dịch HNO3 đun nóng thu được V lít khí NO (sản phẩm khử duy nhất) ở đktc. Giá trị của V là :
A. 0,224 lít.
B. 0,672 lít.
C. 2,24 lít.
D. 6,72 lít.
Hướng dẫn giải chi tiết:
Ta nhận thấy Fe2O3 và CuO đều có số OXH max khi tham gia phản ứng nên không có khả năng nhường e
=> Thực thế chỉ có quá trình cho, nhận e của Al và HNO3.
Ta có:
Quá trình oxi hóa :
Al → Al+3 + 3e
mol : 0,03 → 0,09
Quá trình khử :
N+5 + 3e → N+2
mol : 0,09 → 0,03
Þ VNO = 0,03.22,4 = 0,672 lít.
Đáp án D.
Dạng 3: Bài toán về muối nitrat
* Một số lưu ý cần nhớ:
- Các muối nitrat đều tan và dễ bị phân hủy khi bị đun nóng
a. Muối nitrat của các kim loại hoạt động (trước Mg) nhiệt phân sinh ra muối Nitrit + O2
2KNO3 2KNO2 + O2
b) Muối nitrat của các kim loại từ Mg đến Cu nhiệt phân sinh ra oxit kim loại + NO2 + O2
2Cu(NO3)2 2CuO + 4NO2 + O2
c. Muối của những kim loại kém hoạt động (sau Cu ) nhiệt phân sinh ra kim loại + NO2 + O2
2AgNO3 2Ag + 2NO2 + O2
* Một số ví dụ điển hình
Ví dụ 1: Nung nóng hết 27,3 gam hỗn hợp X gồm NaNO3 và Cu(NO3)2 rồi hấp thụ toàn bộ khí thu được vào H2O thấy có 1,12 lít khí (đktc) bay ra. Khối lượng Cu(NO3)2 trong X là
Hướng dẫn giải chi tiết:
Gọi nNaNO3 = a mol; nCu(NO3)2 = b mol
=> mhỗn hợp = 85a + 188b = 27,3 (1)
2NaNO3 2NaNO2 + O2
a → 0,5a
2Cu(NO3)2 2CuO + 4NO2 + O2
b → 2b → 0,5b
Hấp thụ khí vào nước:
4NO2 + O2 + 2H2O → 4HNO3
2b → 0,5b
=> nkhí còn lại = 0,5a = 0,05 => a = 0,1
Thay a = 0,1 vào (1) => b = 0,1
=> mCu(NO3)2 = 0,1.188 = 18,8 gam
Ví dụ 2: Đem nung một lượng Cu(NO3)2 sau một thời gian thì dừng lại làm nguội rồi cân thấy khối lượng giảm 0,54 gam. Khối lượng muối đã bị nhiệt phân là
Hướng dẫn giải chi tiết:
2Cu(NO3)2 2CuO + 4NO2 + O2
x → x → 2x → 0,5x
mgiảm = mkhí sinh ra = mNO2 + mO2
=> 2x.46 + 0,5x.32 = 0,54 => x = 0,005 mol
=> mCu(NO3)2 = 0,94 gam