Với giải Bài 15.13 trang 72 SBT Hóa Học lớp 11 Chân trời sáng tạo chi tiết trong Bài 15: Dẫn xuất halogen giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa Học 11. Mời các bạn đón xem:
Sách bài tập Hóa học 11 Bài 15: Dẫn xuất halogen
Bài 15.13 trang 72 Sách bài tập Hóa học 11: Biểu đồ dưới đây biểu diễn nhiệt độ sôi (°C) của một số loại dẫn xuất halogen. Quan sát và trả lời các câu hỏi:
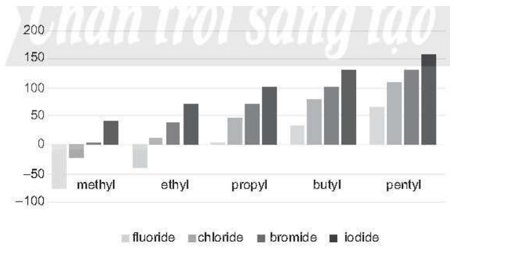
Nhiệt độ sôi của dẫn xuất halogen
a) Trong điều kiện chuẩn (25 °C, 1 bar), liệt kê tên hoặc công thức một số dẫn xuất halogen ở thể khí.
b) Nhận xét nhiệt độ sôi các dẫn xuất halogen của hydrocarbon. Giải thích nguyên nhân dẫn đến xu hướng biến đổi nhiệt độ sôi các dẫn xuất.
Lời giải:
a) Hướng dẫn: Xác định điểm ở giữa nhiệt độ 0 °C và 50 °C, dùng bút chì vẽ đường thẳng song song với đường nằm ngang, biểu diễn đường nhiệt độ 25 °C.
Trong điều kiện thường (25 °C, 1 bar), một số dẫn xuất halogen ở thể khí: fluoromethane (CH3F), chloromethane (CH3Cl), bromomethane (CH3Br), fluoroethane (CH3CH2F), chloroethane (CH3CH2Cl) và fluoropropane (CH3CH2CH2F).
b) Nhận xét về nhiệt độ sôi các dẫn xuất halogen của hydrocarbon:
- Với các dẫn xuất cùng loại halogen, nhiệt độ sôi tăng dần từ gốc methyl đến pentyl.
- Với các dẫn xuất halogen cùng gốc alkyl, nhiệt độ sôi tăng từ dẫn xuất fluorine đến dẫn xuất iodine.
Trong dẫn xuất halogen, tương tác van der Waals càng lớn thì nhiệt độ sôi càng cao:
- Cùng gốc alkyl, tương tác van der Waals tăng từ dẫn xuất fluoride đến iodide nên nhiệt độ sôi tăng.
- Cùng dẫn xuất halogen, khối lượng gốc alkyl tăng từ methyl đến pentyl làm cho tương tác van der Waals tăng nên nhiệt độ sôi tăng.
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 15.1 trang 70 Sách bài tập Hóa học 11: Hợp chất thuộc loại dẫn xuất halogen của hydrocarbon là...
Bài 15.2 trang 70 Sách bài tập Hóa học 11: Số liên kết của nguyên tử halogen trong phân tử dẫn xuất halogen của hydrocarbon là...
Bài 15.3 trang 70 Sách bài tập Hóa học 11: Mô hình phân tử nào là dẫn xuất halogen của hydrocarbon?...
Bài 15.4 trang 70 Sách bài tập Hóa học 11: Bậc của dẫn xuất halogen là bậc của nguyên tử carbon liên kết với nguyên tử halogen. Bậc của dẫn xuất halogen nào sau đây là không phù hợp?...
Bài 15.5 trang 71 Sách bài tập Hóa học 11: Dẫn xuất halogen bậc II có tên và công thức cấu tạo phù hợp là...
Bài 15.6 trang 71 Sách bài tập Hóa học 11: Công thức cấu tạo nào sau đây ứng với tên gọi không đúng?...
Bài 15.7 trang 71 Sách bài tập Hóa học 11: Nhiệt độ sôi của các dẫn xuất halogen được sắp xếp theo thứ tự: CH3F < CH3CI < CH3Br < CH3I. Nguyên nhân dẫn đến sự tăng dần nhiệt độ sôi từ CH3F đến CH3I là do....
Bài 15.8 trang 71 Sách bài tập Hóa học 11: Phát biểu nào sau đây không phù hợp với tính chất vật lí của dẫn xuất halogen?....
Bài 15.9 trang 71 Sách bài tập Hóa học 11: Sản phẩm chính của phản ứng nào sau đây không đúng?..
Bài 15.10 trang 72 Sách bài tập Hóa học 11: Trong thể thao, khi các vận động viên bị chán thương do va chạm, không gây ra vết thương hở, gãy xương, ... thường được nhân viên y tế dùng loại thuốc xịt, xịt vào chỗ bị thương để gây tê cục bộ và vận động viên có thể quay trở lại thi đấu. Hợp chất chính có trong thuốc xịt là:......
Bài 15.11 trang 72 Sách bài tập Hóa học 11: a) Các nhà hoá học đã tìm ra một số dẫn xuất halogen không chứa chlorine như: CF3CH2F, CF3CH2CF2CH3,... đang được sử dụng trong công nghiệp nhiệt lạnh, vì sự phân huỷ các hợp chất này nhanh chóng sau khi phát tán vào không khí nên ảnh hưởng rất ít đến tầng ozone hay sự ấm lên toàn cầu thấp. Gọi tên theo danh pháp thay thế 2 hợp chất đó...
Bài 15.12 trang 72 Sách bài tập Hóa học 11: So sánh nhiệt độ sôi của methane và các dẫn xuất halogen của methane: CH4, CH3Cl,.....
Bài 15.13 trang 72 Sách bài tập Hóa học 11: Biểu đồ dưới đây biểu diễn nhiệt độ sôi (°C) của một số loại dẫn xuất halogen. Quan sát và trả lời các câu hỏi:...
Bài 15.14 trang 73 Sách bài tập Hóa học 11: Tiến hành thí nghiệm nghiên cứu khả năng phản ứng của dẫn xuất tert-butyl chloride với dung dịch ethanol 80% ở 25 °C. Kết quả thí nghiệm thể hiện trong sơ đồ:...
Bài 15.15 trang 73 Sách bài tập Hóa học 11: Tính chất hoá học chung của dẫn xuất halogen thể hiện qua 2 loại phản ứng thế halogen bởi nhóm hydroxy và phản ứng tách hydrogen halide. Trong đó, độ dài liên kết và năng lượng liên kết ảnh hưởng trực tiếp đến khả năng phản ứng của 2 loại phản ứng này. Quan sát biểu đồ bên dưới và trả lời câu hỏi.....
Bài 15.16 trang 74 Sách bài tập Hóa học 11: Cho phương trình hoá học của phản ứng tổng quát:......
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác: