Với giải sách bài tập Hóa học 11 Bài 15: Dẫn xuất halogen sách Chân trời sáng tạo hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Sách bài tập Hóa học 11 Bài 15: Dẫn xuất halogen
Bài 15.1 trang 70 Sách bài tập Hóa học 11: Hợp chất thuộc loại dẫn xuất halogen của hydrocarbon là
A. HIO4. B. C3H3N. C. CH2BrCl. D. C6H6O.
Lời giải:
Đáp án đúng là: C
Dẫn xuất halogen của hydrocarbon là hợp chất hữu cơ mà ngoài C, H ra thì có thêm nguyên tử halogen.
A. 1. B. 2. C. 3. D. 4.
Lời giải:
Đáp án đúng là: A
Halogen có hóa trị I nên halogen có 1 liên kết trong phân tử dẫn xuất halogen của hydrocarbon.
Bài 15.3 trang 70 Sách bài tập Hóa học 11: Mô hình phân tử nào là dẫn xuất halogen của hydrocarbon?
Lời giải:
Đáp án đúng là: B
Mô hình B của dẫn xuất halogen có công thức tổng quát là CH3-X với X là nguyên tử halogen.
A. Dẫn xuất halogen bậc I.
B. Dẫn xuất halogen bậc II.
C. Dẫn xuất halogen bậc III.
D. Dẫn xuất halogen bậc IV.
Lời giải:
Đáp án đúng là: D
Carbon có tối đa 4 liên kết, nên không thể có dẫn xuất halogen bậc IV.
A. 1,2-dichloroethane: Cl —CH2 — CH2 — Cl.
B. 2-iodopropane: CH2 — CHI —CH3.
C. 1-bromo-2-methylpropane: CH3 —CH(CH3) — CH2—Br.
D. 2-fluoro-2-methylpropane: (CH3)3-F
Lời giải:
Đáp án đúng là: B
Dẫn xuất halogen bậc II có tên và công thức cấu tạo phù hợp là
2-iodopropane: CH2 — CHI —CH3.
Bài 15.6 trang 71 Sách bài tập Hóa học 11: Công thức cấu tạo nào sau đây ứng với tên gọi không đúng?
A. CH3Cl: chloromethane.
B. ClCH2Br: chlorobromomethane.
C. CH3CH2I: iodoethane.
D. CH3CH(F)CH3: 2-fluoropropane.
Lời giải:
Đáp án đúng là: B
Tên gọi đúng của hợp chất ClCH2Br là bromochloromethane.
A. sự phân cực của liên kết carbon - halogen giảm dần từ CH3F đến CH3I.
B. độ âm điện của các halogen trong dẫn xuất giảm dần từ F đến I.
C. tương tác van der Waals tăng dần từ CH3F đến CH3I.
D. độ dài liên kết carbon - halogen tăng dần từ CH3F đến CH3I.
Lời giải:
Đáp án đúng là: C
Nguyên nhân dẫn đến sự tăng dần nhiệt độ sôi từ CH3F đến CH3I là do tương tác van der Waals tăng dần từ CH3F đến CH3I.
A. Trong điều kiện thường, dẫn xuất halogen tồn tại ở 3 thể rắn, lỏng hoặc khí.
B. Dẫn xuất halogen không tan trong nước và các dung môi hữu cơ.
C. Một số dẫn xuất halogen có hoạt tính sinh học.
D. Các dẫn xuất halogen có khối lượng phân tử nhỏ thường là chất khí ở điều kiện thường.
Lời giải:
Đáp án đúng là: B
Dẫn xuất halogen không tan trong nước nhưng tan tốt trong các dung môi hữu cơ.
Bài 15.9 trang 71 Sách bài tập Hóa học 11: Sản phẩm chính của phản ứng nào sau đây không đúng?
A. CH3CH(Cl)CH3 + NaOH → CH3CH(OH)CH3 + NaCl
B. CH3CH2Cl + KOH → CH2 = CH2 + KCl + H2O
C. CH3Br + KOH → CH3OH + KBr
D. CH3CH2CH(Br)CH3 + KOH (ethanol) → CH3CH = CHCH3 + KBr + H2O
Lời giải:
Đáp án đúng là: B
CH3CH2Cl + KOH → CH3CH2OH + KCl.
A. carbon dioxide. B. hydrogen chloride.
C. chloromethane. D. chloroethane.
Lời giải:
Đáp án đúng là: D
Hợp chất chính có trong thuốc xịt là chloroethane.
b) Vẽ công thức cấu tạo của hợp chất có tên: 4-chloro-3,4-dimethylpent-2-ene.
c) Viết đồng phân và gọi tên các dẫn xuất halogen bậc I của hợp chất có công thức C4H9Br.
Lời giải:
a) Tên gọi của các hợp chất:
b) Công thức cấu tạo của 4-chloro-3,4-dimethylpent-2-ene:
c) Đồng phân và tên gọi các dẫn xuất halogen bậc I của hợp chất có công thức C4H9Br:
CH3-CH2-CH2-CH2-Br : 1-bromobutan.
(CH3)2CH-CH2-Br : 1-bromo-2-methylpopane.
Lời giải:
Tương tác van der Waals ảnh hưởng đến nhiệt độ sôi của các dẫn xuất halogen, từ trái sang, số lượng nguyên tử chlorine tăng làm cho tương tác van der Waals tăng. Thứ tự nhiệt độ sôi tăng dần theo chiều: CH4 < CH3Cl < CH2Cl2 < CHCl3 < CCl4.
Nhiệt độ sôi của dẫn xuất halogen
a) Trong điều kiện chuẩn (25 °C, 1 bar), liệt kê tên hoặc công thức một số dẫn xuất halogen ở thể khí.
b) Nhận xét nhiệt độ sôi các dẫn xuất halogen của hydrocarbon. Giải thích nguyên nhân dẫn đến xu hướng biến đổi nhiệt độ sôi các dẫn xuất.
Lời giải:
a) Hướng dẫn: Xác định điểm ở giữa nhiệt độ 0 °C và 50 °C, dùng bút chì vẽ đường thẳng song song với đường nằm ngang, biểu diễn đường nhiệt độ 25 °C.
Trong điều kiện thường (25 °C, 1 bar), một số dẫn xuất halogen ở thể khí: fluoromethane (CH3F), chloromethane (CH3Cl), bromomethane (CH3Br), fluoroethane (CH3CH2F), chloroethane (CH3CH2Cl) và fluoropropane (CH3CH2CH2F).
b) Nhận xét về nhiệt độ sôi các dẫn xuất halogen của hydrocarbon:
- Với các dẫn xuất cùng loại halogen, nhiệt độ sôi tăng dần từ gốc methyl đến pentyl.
- Với các dẫn xuất halogen cùng gốc alkyl, nhiệt độ sôi tăng từ dẫn xuất fluorine đến dẫn xuất iodine.
Trong dẫn xuất halogen, tương tác van der Waals càng lớn thì nhiệt độ sôi càng cao:
- Cùng gốc alkyl, tương tác van der Waals tăng từ dẫn xuất fluoride đến iodide nên nhiệt độ sôi tăng.
- Cùng dẫn xuất halogen, khối lượng gốc alkyl tăng từ methyl đến pentyl làm cho tương tác van der Waals tăng nên nhiệt độ sôi tăng.
Xác định loại phản ứng (1) và (2). Cho biết phản ứng nào chiếm ưu thế trong thí nghiệm trên.
Lời giải:
Phản ứng (1) thuộc loại phản ứng thế, phản ứng (2) thuộc loại phản ứng tách. Dựa vào kết quả thí nghiệm: 83% sản phẩm của phản ứng thế và 17% sản phẩm của phản ứng tách, nên phản ứng thế chiếm ưu thế hơn.
Tương quan giữa độ dài liên kết với năng lượng liên kết C-X trong dẫn xuất halogen
a) Nhận xét sự tương quan giữa độ dài liên kết và năng lượng liên kết C-X trong dẫn xuất halogen của hydrocarbon.
b) Độ dài liên kết và năng lượng liên kết ảnh hưởng như thế nào đến khả năng phản ứng của dẫn xuất halogen. Lấy ví dụ cụ thể cho 2 hợp chất iodoethane và bromoethane.
Lời giải:
a) Trong dẫn xuất halogen, các liên kết C-X có năng lượng liên kết càng lớn thì độ dài liên kết càng nhỏ.
b) Dẫn xuất halogen có năng lượng liên kết C-X càng lớn, độ dài liên kết C-X càng nhỏ thì khả năng phản ứng càng yếu, nguyên nhân là do liên kết bền, cần năng lượng lớn để phá vỡ liên kết cũ để hình thành liên kết mới. Ví dụ: Đối với 2 hợp chất CH3CH2Br và CH3CH2I, năng lượng liên kết của liên kết C-Br lớn hơn của liên kết C-I, nên khả năng phản ứng thế và phản ứng tách của hợp chất CH3CH2I dễ dàng hơn CH3CH2Br.
Bài 15.16 trang 74 Sách bài tập Hóa học 11: Cho phương trình hoá học của phản ứng tổng quát:
R-X + NaOH → R-OH + NaX
Tốc độ phản ứng thế của dẫn xuất halogenoalkane với dung dịch kiềm của một số hợp chất cho giá trị tương đối thể hiện trong bảng sau:
|
STT thí nghiệm |
Hợp chất |
Tốc độ phản ứng (đơn vị tốc độ phản ứng) |
|
1 |
CH3X |
30 |
|
2 |
CH3CH2X |
1 |
|
3 |
(CH3)2CHX |
3.10-2 |
|
4 |
(CH3)3CCH2X |
1.10-5 |
|
5 |
(CH3)3CX |
~0 |
a) So sánh khả năng phản ứng thế bởi nhóm -OH của các halogenoalkane theo thứ tự từ 1 đến 5.
b) Quan sát hình bên dưới, cho biết yểu tố nào ảnh hưởng đến khả năng phản ứng thế nhóm -OH của các halogenoalkane trên?
Lời giải:
a) Tốc độ phản ứng thế của dẫn xuất halogenoalkane với dung dịch kiềm theo thứ tự từ thí nghiệm 1 đến 5 cho các giá trị giảm dần, nên khả năng phản ứng của các chất giảm.
b) Các gốc methyl, ethyl, isopropyl, neopentyl và terf-butyl tăng dần mức độ cồng kềnh của gốc hydrocarbon, làm tăng sự che chắn nhóm -OH thế vào vị trí halogen.
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Lý thuyết Dẫn xuất halogen
1. Khái niệm
- Khi thay thế nguyên tử H trong phân tử hydrocarbon bằng một hay nhiều nguyên tử halogen, ta được dẫn xuất halogen của hydrocarbon.
2. Đồng phân và danh pháp
- Đồng phân cấu tạo của dẫn xuất halogen gồm có: đồng phân mạch carbon, đồng phân vị trí liên kết đôi, liên kết ba và đồng phân vị trí nguyên tử halogen.
- Tên thay danh pháp thay thế của dẫn xuất halogen:
Số chỉ vị trí nhóm thế - Tên nhóm thế halogen+tên hydrocarbon
-Tên gốc – chức: tên gốc hydrocarbon+halide
3. Tính chất vật lý
- Nhiệt độ sôi của các dẫn xuất halogen có xu hướng tăng dần theo chiều tăng khối lượng phân tử.
- Dẫn xuất halogen không tan trong nước, nhưng tan trong dung môi hữu cơ như alcohol, ether, benzene.
4. Tính chất hóa học
a) Phản ứng thế nguyên tử halogen bằng nhóm OH
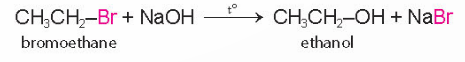
- Dẫn xuất halogen mà nguyên tử halogen lien kết với nguyên tử carbon no có phản ứng thế nhóm –OH trong dung dịch kiếm, đun nóng.
b) Phản ứng tách hydrogen halide
- Các dẫn xuất halogenoalkane có thể bị tách hydrogen halide để tạo thành alkene.
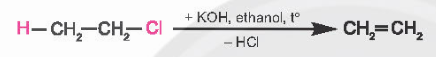
- Quy tắc Zaitsev: trong phản ứng tách HX ra khỏi dẫn xuất halogen, nguyên tử X ưu tiên tách ra cùng với nguyên tử H ở nguyên C bên cạnh có bậc cao hơn, tạo ra sản phẩm chính.
5. Ứng dụng
- Dẫn xuất halogen được sử dụng trong nhiều lĩnh vực: làm dung môi hữu cơ, sản xuất các loại thuốc bảo vệ thực vật, thuốc tăng trưởng thực vật, chất dẻo,…
- Lạm dụng thuốc bảo vệ và thuốc kích thích tăng trưởng thực vật gây tác hại nghiêm trọng đến sức khỏe người tiêu dùng.
- Thay thế các dẫn xuất halogen chứa chlorine bằng fluorine trong công nghiệp nhiệt lạnh làm giảm tác hại đến tầng ozone.