Tài liệu Bộ đề thi Hoá học lớp 12 học kì 1 có đáp án năm học 2022 - 2023 gồm 04 đề thi tổng hợp từ đề thi môn Hoá học 12 của các trường THCS trên cả nước đã được biên soạn đáp án chi tiết giúp học sinh ôn luyện để đạt điểm cao trong bài thi học kì 1Hoá học lớp 12. Mời các bạn cùng đón xem:
Phòng Giáo dục và Đào tạo .....
Đề thi Học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 1)
Câu 1: Polipeptit (HN-CH2-CO)n là sản phẩm của phản ứng trùng ngưng
A. alanin.
B. axit - amino propionic.
C. axit glutamic.
D. glyxin.
Câu 2: Một α- amino axit X trong phân tử có một nhóm –NH2 và một nhóm –COOH. Cho 26,70 gam X phản ứng hoàn toàn với lượng dư dung dịch HCl, thu được dung dịch chứa 37,65 gam muối. Công thức của X là
A. CH3-CH(NH2)-COOH. B. H2N-CH2-COOH.
C. H2N-CH2-CH2-COOH. D. CH3-CH2-CH(NH2)-COOH.
Câu 3: Kim loại Fe không phản ứng với dung dịch nào sau đây?
A. AgNO3. B. CuSO4.
C. HCl. D. NaNO3.
Câu 4: Cho các chất có công thức cấu tạo sau: (1) CH3OOC-COOC2H5; (2) CH3CH2COOCH3; (3) HCOOC2H5; (4) CH3COOH; (5) CH3OCOC2H5; (6) OHCH2CH2COOH.
Những chất thuộc loại este là
A. (2), (3), (5), (6). B. (2), (3), (4), (5).
C. (1), (2), (3), (5). D. (1), (2), (3), (6).
Câu 5: Hỗn hợp E gồm ba peptit mạch hở: đipeptit X, tripeptit Y, tetrapeptit Z có tỉ lệ mol tương ứng là 2 : 1 : 1. Cho một lượng E phản ứng hoàn toàn với dung dịch NaOH dư, thu được 24,25 gam muối của glyxin, 22,20 gam muối của alanin và 13,90 gam muối của valin. Mặt khác, đốt cháy hoàn toàn m gam E, thu được tổng khối lượng của CO2 và H2O là 39,14 gam. Giá trị của m là
A. 22,64. B. 25,08.
C. 20,17. D. 16,78.
Câu 6: Cho các chất sau: fructozơ, glucozơ, etyl axetat, Val-Gly-Ala. Số chất phản ứng với Cu(OH)2 ở nhiệt độ thường, tạo dung dịch màu xanh lam là
A. 4. B. 1.
C. 2. D. 3.
Câu 7: Cho các phát biểu sau:
(1) Các kim lọai Na, K, Ba đều phản ứng mạnh với nước.
(2) Kim loại Cu tác dụng với dung dịch hỗn hợp NaNO3 và H2SO4 (loãng).
(3) Dùng khí CO (dư) khử CuO nung nóng, thu được kim loại Cu.
(4) Dung dịch Fe2(SO4)3 dư có thể tách Ag ra khỏi hỗn hợp Ag và Cu.
(5) Kim loại cứng nhất là Cr.
Số phát biểu đúng là
A. 2. B. 3.
C. 4. D. 5.
Câu 8: Kim loại nào sau đây phản ứng được với dung dịch NaOH ?
A. Al. B. Cu.
C. Fe. D. Ag.
Câu 9: Fructozơ là một loại monosaccarit có nhiều trong mật ong, có vị ngọt sắc. Công thức phân tử của fructozơ là
A. C12H22O11. B. C2H4O2.
C. (C8H10O5)n. D. C6H12O6.
Câu 10: Thực hiện các thí nghiệm sau:
(a) Cho Al vào dung dịch HNO3 loãng, nguội.
(b) Cho Na vào dung dịch CuSO4.
(c) Cho Ag vào dung dịch H2SO4 loãng (không có oxi không khí).
(d) Cho Fe vào dung dịch Fe2(SO4)3.
Trong các thí nghiệm trên, số thí nghiệm xảy ra phản ứng là
A. 1. B. 2.
C. 3. D. 4.
Câu 11: Cho các phát biểu sau:
(1) Phản ứng thủy phân este trong môi trường bazơ là phản ứng thuận nghịch.
(2) Xà phòng hóa chất béo luôn thu được glyxerol và xà phòng.
(3) Benzyl axetat là este có mùi chuối chín.
(4) Tơ nilon - 6,6; tơ visco và tơ axetat thuộc loại tơ bán tổng hợp.
(5) Saccarozơ được cấu tạo từ hai gốc α- glucozơ và β- fructozơ.
(6) Tinh bột và xenlulozơ là hai đồng phân cấu tạo của nhau.
Số phát biểu sai là
A. 3. B. 4.
C. 5. D. 2.
Câu 12: Este A được điều chế từ ancol metylic có tỉ khối so với O2 bằng 2,3125. Công thức cấu tạo của A là
A. CH3COOCH3. B. C2H5COOCH3.
C. C2H3COOCH3. D. HCOOCH3.
Câu 13: Cho các phát biểu sau:
(1) Anilin có tính bazơ, tính bazơ yếu hơn amoniac.
(2) Ở điều kiện thường metylamin, đimetylamin là những chất khí có mùi khai.
(3) Trimetyl amin là amin bậc ba.
(4) Dung dịch của các amino axit đều không làm đổi màu quỳ tím.
(5) Glucozơ bị oxi hóa bởi dung dịch AgNO3 trong NH3, đun nóng.
(6) Tinh bột thuộc loại polisaccarit.
(7) Liên kết peptit là liên kết –CO-NH- giữa hai đơn vị - amino axit.
(8) Polietilen được điều chế bằng phản ứng trùng ngưng.
Số phát biểu đúng là
A. 7. B. 6.
C. 4. D. 5.
Câu 14: Đốt cháy hoàn toàn m gam hỗn hợp gồm xenlulozơ, tinh bột, glucozơ và saccarozơ cần 2,52 lít O2 (đo ở đktc), thu được 1,8 gam nước. Giá trị của m là
A. 6,2. B. 3,15.
C. 3,6. D. 5,25.
Câu 15: Phát biểu nào sau đây là đúng ?
A. Poli acrilonitrin được điều chế bằng phản ứng trùng ngưng.
B. Các este bị thủy phân trong môi trường kiềm đều tạo muối và ancol.
C. Saccarozơ làm mất màu nước brom.
D. Amilopectin có cấu trúc mạch phân nhánh.
Câu 16: Cho các phát biểu sau:
(1) Tính chất hóa học đặc trưng của kim loại là tính khử.
(2) Trong các hợp chất, các kim loại đều chỉ có một mức oxi hóa duy nhất.
(3) Ở điều kiện thường, tất cả các kim loại đều ở trạng thái rắn.
(4) Tính chất vật lí chung của kim loại là do các electron tự do gây ra.
(5) Các kim loại Na, K và Al đều có thể tan tốt trong dung dịch KOH ở điều kiện thường.
(6) Kim loại Cu khử được Fe2+ trong dung dịch.
(7) Để hợp kim Fe-Ni ngoài không khí ẩm thì kim loại Ni bị ăn mòn điện hóa học.
Số phát biểu sai là
A. 4. B. 6.
C. 5. D. 3.
Câu 17: Sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh được gọi chung là
A. Sự ăn mòn điện hóa.
B. Sự khử kim loại.
C. Sự ăn mòn kim loại.
D. Sự ăn mòn hóa học.
Câu 18: Phản ứng nào sau đây dùng để chuyển chất béo lỏng thành chất béo rắn ?
A. Hiđro hóa. B. Oxi hóa.
C. Polime hóa. D. Brom hóa.
Câu 19: Cho từ từ đến dư kim loại Na vào dung dịch có chứa muối FeCl2. Số phản ứng xảy ra là
A. 3. B. 2.
C. 5. D. 6.
Câu 20: Cho các nhận định sau:
(1) Ở điều kiện thường, các amino axit là chất rắn kết tinh, tương đối dễ tan trong nước.
(2) Tất cả các dung dịch protein đều có phản ứng màu biure.
(3) Tinh bột bị thủy phân khi có xúc tác axit vô cơ loãng hoặc các enzim.
(4) Các amino axit đều có tính chất lưỡng tính.
(5) Anilin tác dụng với nước Br2 tạo kết tủa trắng.
(6) Tripanmitin và tristearin đều là những chất béo rắn.
(7) Amilozơ thuộc loại polisaccarit.
Số nhận định đúng là
A. 4. B. 5.
C. 7. D. 6.
Câu 21: Cho dãy các chất: glucozơ, xenlulozơ, saccarozơ, tinh bột. Số chất trong dãy tham gia phản ứng tráng gương là
A. 2. B. 4.
C. 1. D. 3.
Câu 22: Este X có công thức cấu tạo CH2-C(CH3)COOCH3. Tên gọi của X là
A. Metyl metacrylat. B. Metyl acrylic.
C. Metyl acrylat. D. Metyl metacrylic.
Câu 23: Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất ?
A. Li. B. Na.
C. K. D. Hg.
Câu 24: Thủy phân hoàn toàn m gam chất béo bằng dung dịch NaOH đun nóng, thu được 9,2 gam glixerol và 91,80 gam muối. Giá trị của m là
A. 101. B. 89.
C. 85. D. 93.
Câu 25: Hòa tan hoàn toàn 7,68 gam Cu bằng dung dịch HNO3 loãng (dư), sinh ra V lít khí NO (sản phẩm khử duy nhất, đo ở đktc). Giá trị của V là
A. 0,896. B. 2,688.
C. 5,376. D. 1,792.
Câu 26: Xà phòng hóa hoàn toàn 17,6 gam hỗn hợp gồm 2 este etyl axetat và metyl propionat bằng lượng vừa đủ V ml dung dịch NaOH 0,5M. Giá trị của V là
A. 200. B. 500.
C. 400. D. 600.
Câu 27: Thủy phân este X trong môi trường axit, thu được C2H5COOH và CH3OH. Công thức cấu tạo của X là
A. HCOOC2H5. B. C2H5COOCH3.
C. C2H5OCOCH3. D. CH3COOC2H5.
Câu 28: Cho a gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, ở cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích các khí đo ở đktc. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 7,8. B. 6,45.
C. 10,2. D. 14,55.
Câu 29: Cho các phát biểu sau:
(1) Để phân biệt Gly-Gly-Ala với anbumin có thể dùng Cu(OH)2.
(2) Tính bazơ của anilin thể hiện qua phản ứng của anilin với nước brom.
(3) Trong một phân tử tetrapeptit mạch hở có 4 liên kết peptit.
(4) Các este đều không tham gia phản ứng tráng bạc.
(5) Xenlulozơ trinitrat được dùng làm thuốc súng không khói.
(6) Glucozơ có vị ngọt hơn fructozơ.
(7) Amilopectin trong tinh bột chỉ có các liên kết α - 1,4 – glicozit.
(8) Axit glutamic là hợp chất lưỡng tính.
Số phát biểu sai là
A. 4. B. 6.
C. 7. D. 5.
Câu 30: Hòa tan 2,4 gam hỗn hợp gồm 2 kim loại Mg và Fe bằng lượng vừa đủ dung dịch H2SO4 loãng. Sau phản ứng thu được 1,344 lít H2 (đo ở đktc). Khối lượng muối khan thu được là
A. 5,76 gam. B. 9,12 gam.
C. 8,16 gam. D. 7,2 gam.
Câu 1: Đáp án D
- HN – CH2 – CO - : mắt xích gly.
Câu 2: Đáp án A
Đặt X: H2N – R – COOH
H2N – R – COOH + HCl → ClH3N – R – COOH
Bảo toàn khối lượng có: nHCl = 37,65 – 26,7 = 10,95 gam
→ nX = nHCl = 10,95 : 36,5 = 0,3 mol.
→ MX = 26,7 : 0,3 = 89. Vậy X là Alanin: CH3-CH(NH2)-COOH.
Câu 3: Đáp án D
Fe + NaNO3 → không phản ứng.
Câu 4: Đáp án C
Khi thay nhóm – OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm – OR thì được este.
Những chất thuộc este là : (1) CH3OOC-COOC2H5; (2) CH3CH2COOCH3; (3) HCOOC2H5; (5) CH3OCOC2H5.
Câu 5: Đáp án D
Giả sử số mol của X, Y, Z lần lượt là 2x, x, x (mol)
nNaOH = nGly-Na + nAla-Na + nVal-Na = 0,25 + 0,2 + 0,1 = 0,55 mol
Lại có: nNaOH = 2nX + 3nY + 4nZ → 0,55 = 2.2x + 3x + 4x → x = 0,05 mol.
→ nE = 4x = 0,2 mol
Quy đổi hỗn hợp E thành: C2H3ON (a mol); CH2 (b mol) và H2O (c mol)
nNaOH = 0,55 mol → a = 0,55 mol.
npeptit (E) = c = 0,2 mol.
Bảo toàn C có: 2a + b = 2.nGly + 3.nAla + 5.nVal → 2.0,55 + b = 2.0,25 + 3.0,2 + 0,1.5 → b = 0,5 mol.
→ mE = 57.0,55 + 14.0,5 + 0,2.18 = 41,95 gam.
Tỉ lệ:
Đốt cháy: 41,95 gam E → mCO2 + mH2O = 97,85 gam
Đốt cháy: m gam E → mCO2 + mH2O = 39,14 gam
Câu 6: Đáp án C
Fructozơ, glucozơ phản ứng với Cu(OH)2 ở nhiệt độ thường, tạo dung dịch màu xanh lam.
Câu 7: Đáp án D
1 – đúng. Các kim loại Na, K, Ba đều phản ứng mạnh với nước.
2 – đúng. 3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O.
3 – đúng. CO + CuO -to→ Cu + CO2.
4 – đúng. Vì Cu phản ứng với Fe2(SO4)3 thu được dung dịch, còn Ag không phản ứng nên tách được Ag ra khỏi hỗn hợp.
5 – đúng. Nếu quy ước độ cứng của kim cương là 10 thì độ cứng của crom là 9.
Câu 8: Đáp án A
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Câu 9: Đáp án D
Fructozơ là C6H12O6.
Câu 10: Đáp án B
a – Al thụ động hóa trong HNO3 loãng, nguội.
b – 2Na + 2H2O → 2NaOH + H2; CuSO4 + 2NaOH → Cu(OH)2 ↓ + Na2SO4.
c - Ag đứng sau H trong dãy hoạt động hóa học nên không phản ứng với H2SO4 loãng.
d – Fe + 2Fe2(SO4)3 → 3FeSO4.
Câu 11: Đáp án A
1 – sai. Phản ứng thủy phân este trong môi trường kiềm là phản ứng 1 chiều.
2 – đúng.
3 – sai. Isoamyl axetat có mùi chuối chín.
4 – sai vì tơ nilon – 6,6 là tơ tổng hợp.
5 – đúng.
Câu 12: Đáp án A
MA = 32.2,3125 = 74.
Vậy A là CH3COOCH3.
Câu 13: Đáp án B
4 – sai. Dung dịch của các amino axit có thể làm đổi màu quỳ tím hoặc không.
8 – sai. Polietilen được điều chế bằng phản ứng trùng hợp etilen.
Câu 14: Đáp án B
Do hỗn hợp gồm cacbonhiđrat nên quy hỗn hợp về dạng : Cm(H2O)n.
Cm(H2O)n + mO2 (0,1125) → mCO2 + nH2O (0,1 mol)
Bảo toàn khối lượng có : m = 0,1.18 + 0,1125.44 – 0,1125.32 = 3,15 gam.
Câu 15: Đáp án D
Câu 16: Đáp án A
2 – sai. Ví dụ Fe, trong hợp chất có thể có số oxi hóa +2 hoặc +3.
3 – sai. Hg ở trạng thái lỏng ở điều kiện thường.
6 – sai. Cu không khử được Fe2+.
7 – sai. Ni không bị ăn mòn.
Câu 17: Đáp án C
Sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh được gọi chung là sự ăn mòn kim loại.
Câu 18: Đáp án A
Phản ứng hiđro hóa dùng để chuyển chất béo lỏng thành chất béo rắn.
Câu 19: Đáp án A
2Na + 2H2O → 2NaOH + H2
FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3.
Câu 20: Đáp án C
Câu 21: Đáp án C
Chỉ glucozơ tham gia phản ứng tráng gương.
Câu 22: Đáp án A
CH2-C(CH3)COOCH3 : Metyl metacrylat.
Câu 23: Đáp án D
Hg là kim loại có nhiệt độ nóng chảy thấp nhất (-390C).
Câu 24: Đáp án B
Sơ đồ: Chất béo + 3NaOH (0,3) → muối (0,1 mol) + C3H5(OH)3
Bảo toàn khối lượng có : m + 0,3.40 = 9,2 + 91,8 → m = 89 gam.
Câu 25: Đáp án D
Bảo toàn electron có: 2.nCu = 3.nNO → nNO = 0,08 mol
→ VNO = 0,08.22,4 = 1,792 lít.
Câu 26: Đáp án C
Etyl axetat: CH3COOC2H5, metyl propionat: CH3CH2COOCH3
→ Etyl axetat và metyl propionat có cùng công thức phân tử là C4H8O2
→ neste = 17,6 : 88 = 0,2 mol
Gọi công thức chung của hỗn hợp este là RCOOR’
RCOOR’ + NaOH → RCOONa + R’OH
→ nNaOH = neste = 0,2 mol → 0,5.V.10-3 = 0,2 → V = 400ml.
Câu 27: Đáp án B
X là C2H5COOCH3.
C2H5COOCH3 + H2O ⇆ C2H5COOH + CH3OH.
Câu 28: Đáp án A
Gọi số mol Mg và Al lần lượt là x và y mol.
X phản ứng với HCl :
→ x + 1,5y = 0,4.
X tác dụng với NaOH chỉ có Al phản ứng :
Giải hệ phương trình được x = 0,1 và y = 0,2.
a = 0,1.24 + 0,2.27 = 7,8 gam.
Câu 29: Đáp án B
1 – sai do cả Gly-Gly-Ala với anbumin đều có phản ứng màu biure.
2 – sai phản ứng thế ở nhân thơm của anilin thể hiện qua phản ứng của anilin với nước brom.
3 – sai trong một phân tử tetrapeptit mạch hở có 3 liên kết peptit.
4 – sai ví dụ HCOOCH3 có thể tham gia phản ứng tráng bạc.
5 – đúng.
6 – sai do glucozơ ít ngọt hơn fructozơ.
7 – sai ngoài liên kết α- 1,4 – glicozit còn có liên kết α- 1,6 – glicozit tại vị trí phân nhánh.
8 – đúng.
Câu 30: Đáp án C
naxit = nkhí = 0,06 mol
Bảo toàn khối lượng: mKL + maxit = mmuối + mkhí → mmuối = 2,4 + 0,06.98 – 0,06.2 = 8,16 gam.
…………………………….Hết……………………………
Phòng Giáo dục và Đào tạo .....
Đề thi Học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 2)
Câu 1: Chất nào sau đây thuộc loại este no, đơn chức, mạch hở?
A. CH3-COOC6H5. B. CH2=CH-COOCH3.
C. CH3-COOCH=CH2. D. CH3-COOC2H5.
Câu 2: Cho dãy các chất: glucozơ, saccarozơ, xenlulozơ, tinh bột. Số chất trong dãy tham gia phản ứng thủy phân là
A. 2. B. 4.
C. 1. D. 3.
Câu 3: Khi cho dung dịch iot vào dung dịch hồ tinh bột, dung dịch chuyển màu
A. xanh tím. B. đỏ gạch.
C. không chuyển màu. D. vàng.
Câu 4: Chất nào sau đây được dùng làm thuốc súng không khói?
A. tơ visco. B. xenlulozơ trinitrat.
C. tơ axetat. D. xenlulozơ.
Câu 5: Số đồng phân cấu tạo amin bậc hai có cùng công thức phân tử C4H11N là
A. 4. B. 1.
C. 2. D. 3.
Câu 6: Hợp chất nào dưới đây thuộc loại amino axit ?
A. H2NCH2COOH. B. CH3COOC2H5.
C. C2H5NH2. D. HCOONH4.
Câu 7: Công thức phân tử của glyxin (axit aminoaxetic) là
A. C3H7O2N. B. C2H5O2N.
C. C2H7O2N. D. C4H9O2N.
Câu 8: Số gốc α-amino axit trong phân tử tripeptit mạch hở là
A. 1. B. 3.
C. 2. D. 4.
Câu 9: Chất nào sau đây không tham gia vào phản ứng màu biure?
A. Ala-Val-Gly-Val. B. Gly-Ala-Ala.
C. Val-Gly-Ala. D. Gly-Ala.
Câu 10: Tơ visco thuộc loại polime
A. bán tổng hợp. B. thiên nhiên.
C. tổng hợp. D. trùng hợp.
Câu 11: Cho dãy các chất: H2NCH2COOH, C2H5NH2, CH3NH2, CH3COOH. Số chất trong dãy phản ứng với HCl trong dung dịch là
A. 4. B. 1.
C. 2. D. 3.
Câu 12: Cho các phát biểu sau:
(1) Fructozơ và glucozơ đều có khả năng tham gia phản ứng tráng bạc;
(2) Saccarozơ và tinh bột đều không bị thủy phân khi có axit H2SO4 (loãng) làm xúc tác;
(3) Tinh bột được tạo thành trong cây xanh nhờ quá trình quang hợp;
(4) Xenlulozơ và saccarozơ đều thuộc loại đisaccarit.
Phát biểu đúng là
A. (2) và (4). B. (1) và (3).
C. (3) và (4). D. (1) và (2).
Câu 13: Để trung hòa 3,1 gam một amin đơn chức X cần dùng vừa đủ 100 ml dung dịch HCl 1M. Công thức phân tử của X là
A. C3H9N. B. CH5N.
C. C2H5N. D. C2H7N.
Câu 14: Thủy phân hoàn toàn 1 mol peptit mạch hở X chỉ thu được 3 mol Gly và 2 mol Ala. Phân tử khối của X là
A. 331. B. 349.
C. 335. D. 326.
Câu 15: Thuỷ phân 13,2 gam etyl axetat bằng 300 ml dung dịch NaOH 0,2M. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch, thu được m gam chất rắn khan. Giá trị của m là
A. 12,30. B. 12,84.
C. 15,60. D. 4,92.
Câu 16: Để điều chế etyl axetat trong phòng thí nghiệm, người ta lắp dụng cụ như hình vẽ sau:
Hóa chất được cho vào bình 1 trong thí nghiệm trên là
A. CH3COOH, C2H5OH và H2SO4 đặc.
B. CH3COOH, CH3OH và HCl đặc.
C. CH3COOH, C2H5OH và H2SO4 loãng.
D. CH3COOH, CH3OH và H2SO4 đặc.
Câu 17: Nhận xét nào sau đây đúng ?
A. Khi thủy phân CH3COOCH=CH2 bằng dung dịch NaOH thu được muối và ancol tương ứng.
B. Muối natri stearat không thể dùng để sản xuất xà phòng.
C. Vinyl axetat, metyl metacrylat đều có khả năng tham gia phản ứng trùng hợp.
D. Phản ứng thủy phân este trong môi trường axit là phản ứng một chiều.
Câu 18: Trong các kim loại sau đây, kim loại nào dẻo nhất?
A. Sn. B. Au.
C. Cu. D. Al.
Câu 19: Trong các kim loại: Na, Ca, Fe và Cu, số kim loại phản ứng với nước ở điều kiện thường là
A. 2. B. 4.
C. 3. D. 1.
Câu 20: Cho 5,6 gam Fe tác dụng hết với dung dịch HNO3 (dư), sinh ra V lít khí NO (ở đktc, sản phẩm khử duy nhất). Giá trị của V là
A. 1,12. B. 3,36.
C. 4,48. D. 2,24.
Câu 21: Cho 15,2 gam hỗn hợp bột Mg và Cu vào dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn thu được 2,24 lít khí H2 (đktc). Khối lượng Cu trong hỗn hợp là
A. 6,4 gam. B. 12,8 gam.
C. 9,6 gam. D. 4,8 gam.
Câu 22: Phản ứng nào sau đây không xảy ra ?
A. Fe + CuSO4 → FeSO4 + Cu.
B. 2Ag + Cu(NO3)2 → Cu + 2AgNO3.
C. Cu + 2FeCl3 → CuCl2 + 2FeCl2.
D. Hg + S → HgS.
Câu 23: Có 3 chất saccarozơ, mantozơ, anđehit axetic. Dùng thuốc thử nào để phân biệt?
A. AgNO3/NH3 B. Cu(OH)2/NaOH.
C. Dung dịch Br2 D. Na.
Câu 24: Đun nóng dung dịch chứa 27 gam glucozơ với dung dịch AgNO3/NH3(dư) thì khối lượng Ag tối đa thu được là
A. 21,6 gam B. 32,4 gam
C. 16,2 gam D. 10,8 gam
Câu 25: Lên men 162 gam tinh bột với hiệu suất toàn bộ quá trình lên men là 72%. Biết khối lượng riêng của C2H5OH nguyên chất là 0,8 g/ml. Thể tích dung dịch rượu 40o thu được là
A. 115 ml. B. 230 ml.
C. 207 ml. D. 82,8 ml.
Câu 26: Cho m gam một este E vào một lượng vừa đủ KOH đun nóng thu được dung dịch X. Cô cạn X thu được 16,5 gam muối khan của một axit đơn chức và 6,9 gam một ancol đơn chức Y. Cho toàn bộ Y tác dụng với Na dư thu được 1,68 lít khí (ở đktc). Tên của E là
A. etyl propionat B. etyl acrylat
C. metyl metacrylat D. etyl axetat
Câu 27: Phản ứng lưu hóa cao su thuộc loại:
A. Giữ nguyên mạch polime
B. Giảm mạch polime
C. Đề polime hóa
D. Tăng mạch polime
Câu 28: X là một aminoaxit. Cứ 0,01 mol X tác dụng vừa hết 80ml dung dịch HCl 0,125M thu được 1,835g muối. Mặt khác 0,01 mol X tác dụng với dung dịch NaOH thì cần 25 gam dung dịch NaOH 3,2%. Vậy công thức cấu tạo của X là
A. H2NC3H5(COOH)2 B. (H2N)2C3H5COOH
C. H2NC3H6COOH D. H2NC7H12COOH
Câu 29: Chọn câu sai:
A. Lòng trắng trứng có phản ứng màu biure với Cu(OH)2.
B. Liên kết của nhóm CO với nhóm NH giữa hai đơn vị α-amino axit được gọi là liên kết peptit.
C. Thủy phân hoàn toàn protein đơn giản thu được các α-amino axit.
D. Pentapeptit: Tyr – Ala – Gly – Val – Lys (mạch hở) có 5 liên kết peptit.
Câu 30: Thủy phân 14,6 gam Gly-Ala trong dung dịch NaOH dư thu được m gam muối. Giá trị của m là
A. 16,8. B. 18,6.
C. 20,8. D. 20,6.
Câu 1: Đáp án D
CH3-COOC2H5 là este no, đơn chức, mạch hở.
Câu 2: Đáp án D
Saccarozơ, xenlulozơ, tinh bột tham gia phản ứng thủy phân.
Câu 3: Đáp án A
Khi cho dung dịch iot vào dung dịch hồ tinh bột, dung dịch chuyển màu xanh tím.
Câu 4: Đáp án B
Xenlulozơ trinitrate được ứng dụng làm thuốc súng không khói.
Câu 5: Đáp án D
Các amin bậc II ứng với công thức phân tử C4H11N là:
CH3 – NH – CH2 – CH2 – CH3; CH3 – NH – CH (CH3)2; C2H5 – NH – C2H5.
Câu 6: Đáp án A
Amino axit là hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm – NH2 và – COOH.
→ H2NCH2COOH là amino axit.
Câu 7: Đáp án B
Glyxin: H2N – CH2 – COOH → CTPT là: C2H5O2N.
Câu 8: Đáp án B
Trong phân tử tripeptit mạch hở có 3 gốc α-amino axit.
Câu 9: Đáp án D
Chỉ peptit có từ 2 liên kết peptit trở nên mới có phản ứng màu biure.
Câu 10: Đáp án A
Tơ visco thuộc loại polime bán tổng hợp.
Câu 11: Đáp án D
H2NCH2COOH, C2H5NH2, CH3NH2 phản ứng được với HCl.
Câu 12: Đáp án B
2 – sai vì Saccarozơ và tinh bột đều bị thủy phân khi có axit H2SO4 (loãng) làm xúc tác;
4 – sai vì Xenlulozơ thuộc loại polisaccarit.
Câu 13: Đáp án B
Đặt công thức amin là R-NH2
→ Mamin = 3,1 : 0,1 = 31. Vậy amin là CH3NH2 → CTPT: CH5N.
Câu 14: Đáp án A
Phân tử khối của X là: 75.3 + 2.89 – 4.18 = 331 (g/ mol).
Câu 15: Đáp án D
CH3COOC2H5 (0,15) + NaOH (0,06 mol) → CH3COONa + C2H5OH
Theo phản ứng este dư, vậy chất rắn sau phản ứng chỉ gồm CH3COONa: 0,06 mol
→ m = 0,06.82 = 4,92 gam.
Câu 16: Đáp án A
Câu 17: Đáp án C
A sai vì CH3COOCH=CH2 + NaOH → CH3COONa + CH3CHO.
B sai vì Muối natri stearat dùng để sản xuất xà phòng.
D sai vì Phản ứng thủy phân este trong môi trường axit là phản ứng thuận nghịch.
Câu 18: Đáp án B
Kim loại dẻo nhất là Au
Câu 19: Đáp án A
Na và Ca phản ứng với nước ở điều kiện thường.
Câu 20: Đáp án D
Bảo toàn electron có: 3.nFe = 3.nNO → nFe = nNO = 0,1mol.
Vkhí = 0,1.22,4 = 2,24 lít.
Câu 21: Đáp án B
Cu không phản ứng.
Mg (0,1) + 2HCl → MgCl2 + H2 (0,1 mol)
→ mCu = 15,2 – 0,1.24 = 12,8 gam.
Câu 22: Đáp án B
Ag + Cu(NO3)2 → không xảy ra.
Câu 23: Đáp án B
Dùng Cu(OH)2/NaOH phân biệt saccarozơ, mantozơ, anđehit axetic.
Ở nhiệt độ thường saccarozơ, mantozơ hòa tan Cu(OH)2 tạo dung dịch phức đồng màu xanh lam, anđehit axetic không hiện tượng → nhận ra anđehit axetic.
Sau đó đun nóng hai ống nghiệm có phức xanh → xuất hiện chất kết tủa màu đỏ
gạch Cu2O → mantozơ.
Câu 24: Đáp án B
Trong phản ứng tráng gương cứ 1 mol glucozơ → 2 mol Ag
nglucozơ = 0,15 mol ⇒ nAg = 0,3 mol
⇒ mAg = 0,3.108 = 32,4g.
Câu 25:
(C6H10O5)n → nC6H12O6 → 2nC2H5OH .
nC2H5OH = 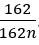
Thể tích rượu C2H5OH 40o là:
Câu 26: Đáp án B
Giả sử E là RCOOR'
Cô cạn X thu được 16,5 gam muối RCOOK và 6,9 gam R'OH
2R'OH (0,15) + 2Na → 2R'ONa + H2 (0,075 mol)
⇒ MR'OH = 6,9 : 0,15 = 46 ⇒ MR' = 29 ⇒ R' là C2H5-.
nRCOOK = nR'OH = 0,15 mol
⇒ MRCOOK = 16,5 : 0,15 = 110 ⇒ MR = 27 ⇒ R là CH2=CH-
X + KOH → CH2=CHCOOK + CH3CH2OH
Vậy X là CH2=CHCOOCH2CH3: etyl acrylat
Câu 27: Đáp án D
Phản ứng lưu hóa chuyển cao su từ mạch thẳng thành mạch không gian ⇒ Tăng mạch polime.
Câu 28: Đáp án A
Ta có: nX = nHCl = 0,01mol ⇒ X chứa 1 nhóm -NH2
nNaOH = 0,02 = 2nX ⇒ X chứa 2 nhóm -COOH
⇒ Aminoaxit X có dạng: H2N-R-(COOH)2
mX = mmuối - mHCl = 1,835 - 0,01.36,5 = 1,47gam
⇒ M = 147 ⇒ R = 41 ⇒ R là -C3H5
Vậy X là H2NC3H5(COOH)2
Câu 29: Đáp án D
D sai vì pentapeptit chỉ có 4 liên kết peptit.
Câu 30: Đáp án C
MGly-Ala = 75 + 89 - 18 = 146
Muối sau phản ứng là: NH2CH2COONa 0,1 mol và CH3CH(NH2)COONa 0,1 mol
mmuối = 0,1.(97 + 111) = 20,8 gam.
…………………………….Hết……………………………
Phòng Giáo dục và Đào tạo .....
Đề thi Học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 3)
Cho nguyên tử khối của một số nguyên tố: H = 1; He = 4; C = 12; N = 14; O = 16; S = 32; Cl = 35,5; Na = 23; K = 39; Ca = 40; Ba = 137; Al =27; Fe =56; Cu = 64; Zn = 65; Ag = 108.
Câu 1: Thủy phân 324 gam tinh bột với hiệu suất của phản ứng là 75%, khối lượng glucozơ thu được là
A. 300 gam. B. 360 gam.
C. 270 gam. D. 250 gam.
Câu 2: Nilon - 6,6 là một loại
A. tơ axetat. B. polieste.
C. tơ poliamit. D. tơ visco.
Câu 3: Peptit X có công thức cấu tạo sau: Gly-Ala-Val-Gly-Ala, hãy cho biết khi thủy phân peptit X có thể thu được bao nhiêu đipeptit?
A. 3. B. 4.
C. 2. D. 5.
Câu 4: X và Y (MX < MY) là 2 peptit mạch hở, đều tạo bởi glyxin và alanin (X và Y hơn kém nhau 1 liên kết peptit), Z là (CH3COO)3C3H5. Đun nóng 31,88 gam hỗn hợp T gồm X, Y, Z trong 1 lít dung dịch NaOH 0,44 M vừa đủ, thu được dung dịch B chứa 41,04 gam hỗn hợp muối. Biết trong T nguyên tố oxi chiếm 37,139% về khối lượng. Phần trăm khối lượng của Y có trong T gần nhất với
A. 18%. B. 26%.
C. 36%. D. 27%.
Câu 5: Hòa tan hết 7,44 gam hỗn hợp gồm Mg, MgO, Fe, Fe2O3 vào dung dịch chứa 0,4 mol HCl và 0,05 mol NaNO3, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X chứa 22,47 gam muối và 0,448 lít (đktc) hỗn hợp khí gồm NO, N2 có tỷ khối so với H2 bằng 14,5. Cho dung dịch NaOH (dư) vào dung dịch X thu được kết tủa Y, lấy Y nung trong không khí đến khối lượng không đổi thu được 9,6 gam chất rắn. Mặt khác nếu cho dung dịch X tác dụng với dung dịch AgNO3 (dư) thu được m gam kết tủa. Biết chất tan trong X chỉ chứa hỗn hợp các muối. Giá trị của m là
A. 64,96 gam. B. 95,2 gam.
C. 63,88 gam. D. 58,48 gam.
Câu 6: Tráng bạc hoàn toàn m gam glucozơ thu được 86,4 gam Ag. Nếu lên men hoàn toàn m gam glucozơ rồi cho khí CO2 thu được hấp thụ vào nước vôi trong dư thì lượng kết tủa thu được là
A. 40g. B. 60g.
C. 20g. D. 80g.
Câu 7: Mô tả nào dưới đây là không đúng ?
A. Glucozơ và fructozơ đều có vị ngọt và đều ngọt nhiều hơn đường mía.
B. Glucozơ còn có tên gọi là đường nho, fructozơ được gọi là đường mật ong.
C. Glucozơ là chất rắn, dạng tinh thể, không màu, tan trong nước.
D. Glucozơ có mặt trong hầu hết các bộ phận của cây, nhất là trong quả chín; có khoảng 0,1% trong máu người.
Câu 8: Hợp chất X có công thức cấu tạo: CH3CH2COOCH3. Tên gọi của X là:
A. metyl axetat. B. metyl propionat.
C. etyl axetat. D. propyl axetat.
Câu 9: Để điều chế 26,73 kg xenlulozơ trinitrat (hiệu suất 60%) cần dùng ít nhất V lít axit HNO3 94,5% (D = 1,5 g/ml) phản ứng với xenlulozơ dư. Giá trị của V là
A. 30. B. 18.
C. 12. D. 20.
Câu 10: Thành phần chính trong nguyên liệu bông, đay, gai là
A. Glucozơ. B. Tinh bột.
C. Fructozơ. D. Xenlulozơ.
Câu 11: Cation X+ có cấu hình electron lớp ngoài cùng là 3s23p6. Vị trí của X trong bảng tuần hoàn là
A. Chu kì 4, nhómVIIIA.
B. Chu kì 4, nhóm IA.
C. Chu kì 3, nhóm IA.
D. Chu kì 3, nhóm VIIIA.
Câu 12: Dung dịch metylamin trong nước làm
A. quì tím hóa xanh.
B. phenolphtalein hoá xanh.
C. quì tím không đổi màu.
D. phenolphtalein không đổi màu.
Câu 13: Hoà tan hoàn toàn 2,8 gam bột Fe vào dung dịch AgNO3 dư thì khối lượng chất rắn thu được là
A. 21,6 gam. B. 16,2 gam.
C. 15,4 gam. D. 10,8 gam.
Câu 14: Kim loại nào sau đây có tính dẫn điện tốt nhất trong tất cả các kim loại?
A. Nhôm. B. Bạc.
C. Vàng. D. Đồng.
Câu 15: Cho các chất có công thức cấu tạo sau đây: (1) CH3CH2COOCH3; (2) CH3COOCH3; (3) HCOOC2H5; (4) CH3COOH; (5) CH3CH(COOC2H5)COOCH3; (6) HOOCCH2CH2OH; (7) CH3OOC-COOC2H5. Những chất thuộc loại este là
A. (1), (2), (4), (6), (7).
B. (1), (2), (3), (6), (7).
C. (1), (2), (3), (4), (5), (6).
D. (1), (2), (3), (5), (7).
Câu 16: Cho dãy các chất: C6H5NH2 (anilin), H2NCH2COOH, CH3CH2COOH, CH3CH2CH2NH2, C6H5OH (phenol). Số chất trong dãy tác dụng được với dung dịch HCl là
A. 4. B. 5.
C. 3. D. 2.
Câu 17: Đốt cháy một este hữu cơ X thu được 13,2g CO2 và 5,4g H2O. X thuộc loại:
A. Este mạch vòng, đơn chức.
B. Este no, đơn chức.
C. Ese có một liên kết đôi C=C chưa biết mấy chức.
D. Este 2 chức, no.
Câu 18: Cho 6 gam một este của axit cacboxylic no, đơn chức và ancol no, đơn chức phản ứng vừa hết với 100 ml dung dịch NaOH 1M. Tên gọi của este đó là
A. etyl axetat. B. metyl axetat.
C. propyl fomat. D. metyl fomat.
Câu 19: Một α- amino axit X chỉ chứa 1 nhóm amino và 1 nhóm cacboxyl. Cho 10,68 gam X tác dụng với HCl dư thu được 15,06 gam muối. Tên gọi của X là
A. glyxin B. valin.
C. axit glutamic. D. alanin.
Câu 20: Đun nóng chất béo cần vừa đủ 40 kg dung dịch NaOH 15%, giả sử phản ứng xảy ra hoàn toàn. Khối lượng (kg) glixerol thu được là
A. 13,8. B. 4,6.
C. 9,2. D. 6,975.
Câu 21: Một chất khi thủy phân trong môi trường axit, đun nóng không tạo ra glucozơ. Chất đó là
A. xenlulozơ. B. saccarozơ.
C. protit. D. tinh bột.
Câu 22: Đốt cháy hết 5,64 gam hỗn hợp X gồm 1 axit đơn chức, 1 ancol đơn chức và este tạo bởi axit và ancol trên, thu được 11,88 gam CO2 và 4,32 gam H2O. Nếu lấy cùng lượng hỗn hợp trên tác dụng đủ với 250 ml dung dịch NaOH 0,2M, dung dịch sau phản ứng đun nóng thu được 0,896 lít (đktc) hơi ancol và 4,7 gam muối khan Y. Trong số các phát biểu sau:
(1) % về số mol của axit trong hỗn hợp X là 42,86%.
(2) có 2 đồng phân este thỏa mãn đề bài ra.
(3) % về khối lượng của ancol trong hỗn hợp X là 40,43%.
(4) 5,64 gam hỗn hợp X phản ứng tối đa với 0,04 mol Br2.
(5) Khi nung muối Y với hỗn hợp vôi tôi xút (NaOH/CaO) thu được eten.
Số phát biểu đúng là
A. 2. B. 3.
C. 5. D. 4.
Câu 23: Mật ong có vị ngọt đậm là do trong mật ong có nhiều:
A. fructozơ. B. tinh bột.
C. saccarozơ. D. glucozơ.
Câu 24: Thứ tự một số cặp oxi hoá - khử trong dãy điện hoá như sau: Mg2+/Mg; Fe2+/Fe; Cu2+Cu; Fe3+/Fe2+; Ag+/Ag. Dãy chỉ gồm các chất, ion tác dụng được với ion Fe3+ trong dung dịch là:
A. Mg, Fe, Cu.
B. Mg, Cu, Cu2+.
C. Mg, Fe2+, Ag.
D. Fe, Cu, Ag+.
Câu 25: Để khử ion Cu2+ trong dung dịch CuSO4 có thể dùng kim loại
A. K. B. Ba.
C. Fe. D. Na.
Câu 26: Một este có CTPT là C3H6O2, có phản ứng tráng gương với dung dịch AgNO3/NH3. CTCT của este đó là
A. HCOOC3H7 B. CH3COOCH3
C. HCOOC2H5 D. C2H5COOCH3
Câu 27: Sản phẩm cuối cùng của quá trình thủy phân các protein đơn giản nhờ chất xúc tác thích hợp là
A. β-aminoaxit. B. axit cacboxylic.
C. α-aminoaxit. D. este.
Câu 28: Trong các chất dưới đây, chất nào là glyxin
A. H2N-CH2-COOH.
B. H2N-CH2-CH2-COOH.
C. HOOC-CH2CH(NH2)COOH.
D. CH3-CH(NH2)-COOH.
Câu 29: Ngâm một đinh sắt sạch trong 200 ml dung dịch CuSO4 sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch CuSO4 đã dùng là:
A. 0,3M. B. 0,5M.
C. 0,4M. D. 0,25M.
Câu 30: Phân tử khối trung bình của polietilen X là 420.000. Hệ số polime hoá của PE là
A. 12.000. B. 13.000.
C. 17.000. D. 15.000.

Câu 1: Đáp án C
Câu 2: Đáp án C
Tơ nilon – 6,6 là một loại tơ poliamit vì các mắt xích nối với nhau bằng các nhóm amit (– CO – NH –) .
Câu 3: Đáp án A
Thủy phân peptit X có thể thu được các đipeptit là: Gly-Ala; Ala-Val; Val-Gly.
Câu 4: Đáp án A
Quy đổi hỗn hợp peptit về C2H3ON (x mol); CH2 (y mol); H2O (z mol) và (CH3COO)3C3H5 (t mol)
mT = 31,88 gam → 57x + 14y + 18z + 218t = 31,88 (1)
nNaOH = 0,44 mol → x + 3t = 0,44 (2)
Muối trong B gồm: C2H4O2NNa (x mol); CH2 (y mol); CH3COONa (3t mol)
→ 97x + 14y + 82.3t = 41,04 hay 97x + 14y + 246t = 41,04 (3)
Biết trong T nguyên tố oxi chiếm 37,139% về khối lượng nên:
→ mO (T) = 31,88.37,139% = 11,84
Hay x + z + 6t = 0,74 (4)
Từ (1); (2); (3) và (4) có x = 0,2; y = 0,14; z = 0,06; t = 0,08.
Số N trong
→ X là tripeptit (0,04 mol) và Y là tetrapeptit (0,02 mol)
(ghi chú: tính số mol X và Y bằng npeptit = nH2O = z và Số N)
Gọi số mol của Gly và Ala lần lượt a, b
→ a + b = nN (T) = 0,2 và 2a + 3b = nC (peptit) = 2x + y = 0,54
→ a = 0,06 và b = 0,14.
Gọi X là Glyu(Ala)3 – u và Y là Glyv(Ala)4 – v.
nGly = 0,06 → 0,04u + 0,02v = 0,06 hay 2u + v = 3.
Mà X và Y đều chứa Gly và Ala nên u = 1 và v = 1 thỏa mãn.
Vậy Y là Gly(Ala)3
Câu 5: Đáp án C
Gọi số mol NO và N2 lần lượt là x mol và y mol.
nkhí = 0,02 mol → x + y = 0,02 mol
mkhí = 0,02.14,5.2 = 0,58 gam → 30x + 28y = 0,58 gam
Giải hệ được x = y = 0,01 mol.
Do dung dịch X chỉ chứa muối nên HCl phản ứng hết.
BTKL:
MH2O = 7,44 + 0,4.36,5 + 0,05.85 – 22,47 – 0,58 = 3,24 gam → nH2O = 0,18 mol.
Giả sử muối có NH4+
Bảo toàn nguyên tố H có:
nHCl = 2.nH2O + 4.nNH4+ → nNH4+ = 0,01 mol.
Cho NaOH dư vào X thu được kết tủa Y, nung Y trong không khí thu được rắn chứa MgO và Fe2O3 có khối lượng 9,6 gam.
Lượng O để oxi hóa 7,44 gam hỗn hợp ban đầu lên tối đa là:
Cho AgNO3 dư tác dụng với dung dịch X ta thu được kết tủa gồm AgCl 0,4 mol (bảo toàn Cl) và Ag.
Bảo toàn electron có:
nAg = 0,135.2 - 0,01.8 - 0,01.3 - 0,01.10 = 0,06 mol
→ m = 0,4.143,5 + 0,06.108 = 63,88 (gam).
Câu 6: Đáp án D
Câu 7: Đáp án A
A sai vì Glucozơ không ngọt bằng đường mía.
Câu 8: Đáp án B
CH3CH2COOCH3: metyl propionat.
Câu 9: Đáp án D
Câu 10: Đáp án D
Thành phần chính trong nguyên liệu bông, đay, gai là xenlulozơ.
Câu 11: Đáp án B
X → X+ + 1e
→ Cấu hình electron của X là [Ar]4s1.
Vậy X ở chu kỳ 4 (do có 4 lớp electron); nhóm IA (do 1 electron hóa trị, nguyên tố s).
Câu 12: Đáp án A
Dung dịch metylamin trong nước có tính bazơ nên làm quỳ tím chuyền sang màu xanh.
Câu 13: Đáp án B
Fe (0,05) + 3AgNO3 dư → Fe(NO3)3 + 3Ag (0,15 mol)
mAg = 0,15.108 = 16,2 gam.
Câu 14: Đáp án B
Ag dẫn điện tốt nhất.
Câu 15: Đáp án D
Khi thay nhóm - OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm – OR thì được este.
Các chất thuộc loại este là: (1) CH3CH2COOCH3; (2) CH3COOCH3; (3) HCOOC2H5; (5) CH3CH(COOC2H5)COOCH3; (7) CH3OOC-COOC2H5.
Câu 16: Đáp án C
Các chất tác dụng được với HCl là: C6H5NH2 (anilin), H2NCH2COOH, CH3CH2CH2NH2.
Câu 17: Đáp án B
Ta có: nCO2 = nH2O = 0,3(mol)
Vậy X thuộc este no, đơn chức.
Câu 18: Đáp án D
Gọi este có dạng RCOOR’
RCOOR’ (0,1) + NaOH (0,1 mol) → RCOONa + R’OH
Có Meste = 6 : 0,1 = 60 → R + R’ = 16.
Vậy este là HCOOCH3 hay metyl fomat.
Câu 19: Đáp án D
X có dạng: H2N – R – COOH
H2N – R – COOH + HCl → ClH3N – R – COOH
Bảo toàn khối lượng có mHCl = 15,06 – 10,68 = 4,38 gam
→ nX = nHCl = 4,38 : 36,5 = 0,12 mol
→ MX = 10,68 : 0,12 = 89. Vậy X là Alanin.
Câu 20: Đáp án B
Câu 21: Đáp án C
Sản phẩm cuối cùng khi thủy phân các protit là α-amino axit.
Câu 22: Đáp án B
Bảo toàn khối lượng có: mO2 = 11,88 + 4,32 – 5,64 = 10,56 gam → nO2 = 0,33 mol.
Bảo toàn nguyên tố O có: 2x + y + 2z = 0,12 (1)
nNaOH = 0,05 → x + z = 0,05 (2)
Dung dịch sau phản ứng thu được 0,896 lít hơi ancol (đktc) và 4,7 gam muối khan
Từ (1); (2) và (3) có x = 0,03 mol và y = z = 0,02 mol.
Thay vào (4) được R = 27 (- CH= CH2)
Mà khối lượng ban đầu là 5,64 gam → 72.0,03 + (R’ + 17).0,02 + (71 + R’).0,02 = 5,64 → R’ = 43 ( - C3H7).
Vậy X gồm:
CH2 = CH – COOH: 0,03 mol; C3H7OH: 0,2 mol và CH2 = CH – COOC3H7: 0,02 mol
Xét các đáp án:
(1) % về số mol của axit trong hỗn hợp X là 42,86% → đúng.
(2) có 2 đồng phân este thỏa mãn đề bài ra → đúng.
(3) % về khối lượng của ancol trong hỗn hợp X là 40,43% → sai (21,28%)
(4) 5,64 gam hỗn hợp X phản ứng tối đa với 0,04 mol Br2 → sai (0,05 mol)
(5) Khi nung muối Y với hỗn hợp vôi tôi xút (NaOH/CaO) thu được eten → đúng.
Câu 23: Đáp án A
Trong mật ong chứa nhiều fructozơ.
Câu 24: Đáp án A
B sai do Cu2+ không tác dụng với Fe3+.
C sai do Fe2+, Ag không tác dụng với Fe3+.
D sai do Ag+ không tác dụng với Fe3+.
Câu 25: Đáp án C
Fe + CuSO4 → FeSO4 + Cu.
Câu 26: Đáp án C
Chú ý: HCOOC3H7 có phản ứng tráng gương nhưng không chọn do CTPT khác C3H6O2.
Câu 27: Đáp án C
Sản phẩm cuối cùng của quá trình thủy phân các protein đơn giản nhờ chất xúc tác thích hợp là α-aminoaxit.
Câu 28: Đáp án A
Glyxin: H2N-CH2-COOH.
Câu 29: Đáp án B
Câu 30: Đáp án D
Hệ số polime hóa (n)
…………………………….Hết……………………………
Phòng Giáo dục và Đào tạo .....
Đề thi Học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 4)
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Cl = 35,5; Al = 27; K = 39; Ca = 40; Ag = 108, Ba = 137, Mg = 24, Cu = 64, Fe = 56, Mn = 55.
Câu 1: Kim loại nào sau đây tác dụng được với nước ở nhiệt độ thường?
A. Fe. B. Cu.
C. Na. D. Ag.
Câu 2: Kim loại có nhiệt độ nóng chảy cao nhất là
A. Hg. B. Ag.
C. W. D. Fe.
Câu 3: Chất nào sau đây thuộc loại chất béo?
A. Natri oleat. B. Tristearin.
C. Etyl axetat. D. Metyl fomat.
Câu 4: Polietilen (PE) được sử dụng làm chất dẻo. PE được tạo ra bằng phản ứng trùng hợp chất nào sau đây
A. CH2=CH-CI. B. CH2=CH-CN.
C. CH2=CH-CH3. D. CH2=CH2.
Câu 5: Anilin có công thức là
A. C6H5-NH2. B. CH3NH2.
C. NH2-CH2-COOH. D. NH2-CH(CH3)-COOH.
Câu 6: Công thức phân tử của etyl fomat là
A. C4H8O2. B. C3H4O2.
C. C2H4O2. D. C3H6O2.
Câu 7: Phương trình hóa học nào sau đây sai?
A. Cu + FeSO4 → Fe + CuSO4.
B. Mg + Cl2 → MgCl2.
C. Mg + CuSO4 → Cu + MgSO4.
D. 2Al + 3Cl2 → 2AlCl3.
Câu 8: Hợp chất nào dưới đây thuộc loại amino axit ?
A. C2H5NH2. B. CH3COOC2H5.
C. NH2CH2COOH. D. HCOONH4.
Câu 9: Trong các ion sau đây, ion nào có tính oxi hóa mạnh nhất?
A. Ca2+. B. Zn2+.
C. Ag+. D. Cu2+.
Câu 10: Kim loại nào sau đây không tan trong dung dịch HCl?
A. Al. B. Cu.
C. Zn. D. Mg.
Câu 11: Glucozơ thuộc loại monosaccarit, nó được dùng làm thuốc tăng lực cho người già, trẻ em và người ốm. Glucozơ có công thức là
A. C12H22O11. B. (C6H10O5)n.
C. C6H14O6. D. C6H12O6.
Câu 12: Cho các kim loại sau: Na, K, Fe, Mg. Kim loại có tính khử mạnh nhất là?
A. Na. B. Mg.
C. K. D. Fe.
Câu 13: Trong thành phần chất nào sau đây có nguyên tố nitơ?
A. Metylamin. B. Glucozơ.
C. Etyl axetat. D. Tinh bột.
Câu 14: Cho m gam Fe tác dụng hoàn toàn với lượng dư dung dịch HCl thu được 2,24 lít khí H2 (đktc). Giá trị của m là
A. 5,6. B. 2,8.
C. 8,4. D. 11,2.
Câu 15: Thủy phân este nào sau đây (trong dung dịch NaOH vừa đủ) thu được natri axetat và ancol?
A. HCOOCH3. B. HCOOC2H5.
C. C2H3COOCH3. D. CH3COOCH3.
Câu 16: Polime nào sau đây thuộc loại polime thiên nhiên?
A. Polistiren. B. Polietilen.
C. Polipropilen. D. Tinh bột.
Câu 17: Cho y gam kim loại M vào dung dịch Fe2(SO4)3 dư, sau phản ứng hoàn toàn khối lượng phần dung dịch tăng thêm y gam. Kim loại M là
A. Ba. B. Cu.
C. K. D. Ag.
Câu 18: Phát biểu nào sau đây đúng?
A. PVC được điều chế bằng phản ứng trùng hợp.
B. Tơ visco thuộc loại tơ tổng hợp.
C. Amilozơ có cấu trúc mạch phân nhánh.
D. Tơ tằm thuộc loại tơ nhân tạo.
Câu 19:Thủy ngân dễ bay hơi và rất độc. Nếu chẳng may làm vỡ nhiệt kế thủy ngân thì dùng chất nào sau đây để khử độc thủy ngân?
A. Bột lưu huỳnh. B. Bột than.
C. Nước. D. Bột sắt.
Câu 20: Cho phản ứng: aAl + bHNO3 → cAl(NO3)3 + dNO + eH2O. Các hệ số a, b, c, d, e là những số nguyên, tối giản. Tổng (a + b) bằng
A. 5. B. 4.
C. 8. D. 6.
Câu 21: Phân tử khối của peptit Ala-Ala-Ala là
A. 249. B. 189.
C. 267. D. 231.
Câu 22: Dung dịch chất nào sau đây làm quỳ tím chuyển sang màu xanh?
A. Glyxin. B. Axit glutamic.
C. Etylamin. D. Alanin.
Câu 23: Thực hiện phản ứng tráng bạc hoàn toàn dung dịch chứa 18,0 gam glucozơ, thu được tối đa m gam Ag. Giá trị của m là
A. 10,8. B. 5,4.
C. 32,4. D. 21,6.
Câu 24: Thí nghiệm nào sau đây thu được muối sắt (III) sau khi phản ứng kết thúc?
A. Cho FeO vào dung dịch H2SO4 loãng, dư.
B. Cho Fe vào dung dịch HNO3 loãng, dư.
C. Cho Fe vào dung dịch HCl dư.
D. Cho Fe(OH)2 vào dung dịch HCl.
Câu 25: Xà phòng hóa hoàn toàn 0,1 mol chất béo X thu được glixerol và hỗn hợp muối gồm 30,6 gam C17H35COONa và 60,8 gam C17H33COONa. Cho 17,72 gam X tác dụng với lượng dư dung dịch nước brom, số mol brom tối đa phản ứng là
A. 0,02. B. 0,20.
C. 0,40. D. 0,04.
Câu 26: Có 2 kim loại X, Y thỏa mãn các tính chất sau:
| Dung dịch | Kim loại | |
|---|---|---|
| X | Y | |
| HCl | Tác dụng | Không tác dụng |
| HNO3 đặc, nguội | Tác dụng | Tác dụng |
Kim loại X, Y lần lượt là
A. Mg, Cu. B. Cu, Mg.
C. Fe, Mg. D. Al, Fe.
Câu 27: Hòa tan hoàn toàn m gam hỗn hợp X gồm Al, Cu và FeS vào dung dịch chứa 0,32 mol H2SO4 (đặc), đun nóng, thu được dung dịch Y (chất tan chỉ gồm các muối trung hòa) và 0,24 mol SO2 (là chất khí duy nhất). Cho 0,25 mol NaOH phản ứng hết với dung dịch Y, thu được 7,63 gam kết tủa. Giá trị của m là
A. 5,61. B. 4,66.
C. 5,44. D. 5,34.
Câu 28: Lên men m gam tinh bột để sản xuất ancol etylic (hiệu suất cả quá trình là 80%). Toàn bộ lượng CO2 sinh ra hấp thụ hoàn toàn vào dung dịch nước vôi trong dư thu được 40,0 gam kết tủa. Giá trị của m là
A. 40,50. B. 25,92.
C. 45,00. D. 28,80.
Câu 29: Thủy phân hoàn toàn m gam este đơn chức X trong dung dịch NaOH vừa đủ. Sau phản ứng thu được 8,2 gam muối và 4,6 gam ancol etylic. Giá trị của m là
A. 12,80. B. 8,80.
C. 7,40. D. 7,20.
Câu 30: Cho các phát biểu sau:
(a) Trong công nghiệp, saccarozơ được chuyển hóa thành glucozơ dùng để tráng gương, tráng ruột phích.
(b) Phân tử Val-Ala có 8 nguyên tử cacbon.
(c) Saccarozơ tham gia phản ứng thủy phân trong môi trường kiềm.
(d) Dung dịch anbumin phản ứng với Cu(OH)2 trong môi trường kiềm.
(e) Xenlulozơ là thành phần chính tạo nên lớp màng tế bào thực vật, là bộ khung của cây cối.
Số phát biểu đúng là
A. 5. B. 4.
C. 3. D. 2.
Câu 31: Cho kim loại Fe lần lượt phản ứng với các dung dịch: FeCl2, Cu(NO3)2, AgNO3, NaCl. Số trường hợp có phản ứng hóa học xảy ra là
A. 1. B. 3.
C. 2. D. 4.
Câu 32: Cho 19,5 gam hỗn hợp X gồm glyxin và etylamin tác dụng vừa đủ với 200 ml dung dịch NaOH 1,0M. Mặt khác, nếu cho 19,5 gam X tác dụng vừa đủ với V ml dung dịch HCl 1,0M, thu được m gam muối. Giá trị của V và m lần lượt là
A. 300 và 23,90. B. 200 và 26,80.
C. 200 và 23,15. D. 300 và 30,45.
Câu 33: Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian, quan sát thấy hiện tượng gì?
A. Thanh Fe có màu trắng và dung dịch nhạt dần màu xanh.
B. Thanh Fe có màu đỏ và dung dịch nhạt dần màu xanh.
C. Thanh Fe có màu đỏ và dung dịch dần có màu xanh.
D. Thanh Fe có màu trắng xám và dung dịch nhạt dần màu xanh.
Câu 34: Cho vào ống nghiệm 3 - 4 giọt dung dịch CuSO4 5% và 2 ml dung dịch NaOH 10%. Lắc nhẹ, gạn bỏ phần dung dịch, giữ lại kết tủa Cu(OH)2. Tiếp tục nhỏ 2 ml dung dịch chất X nồng độ 1% vào ống nghiệm, lắc nhẹ, thu được dung dịch màu xanh lam. X không thể là
A. glucozơ. B. fructozơ.
C. saccarozơ. D. metanol.
Câu 35: Cho 3,36 gam bột sắt vào 300 ml dung dịch CuSO4 0,05M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
A. 0,96. B. 5,76.
C. 3,48. D. 2,52.
Câu 36: Đốt cháy 5,64 gam hỗn hợp gồm Mg, Al trong khí Cl2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 25,52 gam hỗn hợp muối. Thể tích khí Cl2 (đktc) đã phản ứng là
A. 12,544 lít. B. 4,928 lít.
C. 6,272 lít. D. 3,136 lít.
Câu 37: Cho 39 gam kim loại Kali vào 362 gam nước thu được dung dịch X. Nồng độ phần trăm của chất tan trong dung dịch X là
A. 10,00%. B. 14,00%.
C. 9,75%. D. 13,96%.
Câu 38: Một α-amino axit X (trong phân tử có một nhóm -NH2 và một nhóm -COOH). Cho 21,36 gam X phản ứng với lượng dư dung dịch NaOH, thu được dung dịch chứa 26,64 gam muối. Công thức của X là
A. H2N-CH(C2H5)-COOH. B. H2N-CH(CH3)-COOH.
C. H2N-CH2-COOH. D. H2N-(CH2)2-COOH.
Câu 39: Thủy phân 14,6 gam Gly-Ala trong dung dịch NaOH dư thu được m gam muối. Giá trị của m là
A. 16,8. B. 20,8.
C. 18,6. D. 20,6.
Câu 40: Đốt cháy hoàn toàn m gam hỗn hợp E gồm hai este mạch hở X và Y (đều tạo bởi axit cacboxylic và ancol, MX < MY < 150) thu được 4,48 lít khí CO2. Cho m gam E tác dụng vừa đủ với dung dịch NaOH, thu được một ancol Z và 6,76 gam hỗn hợp muối. Cho toàn bộ Z tác dụng với Na dư, thu được 1,12 lít khí H2. Phần trăm khối lượng của X trong E là
A. 44,30%. B. 74,50%.
C. 60,40%. D. 50,34%.
Câu 1: Đáp án C
Na là kim loại kiềm nên tác dụng được với nước ở ngay nhiệt độ thường.
2Na + 2H2O → 2NaOH + H2↑
Câu 2: Đáp án C
W có nhiệt độ nóng chảy cao nhất (3410oC).
Câu 3: Đáp án B
Chất béo là Trieste của glixerol với axit béo.
Câu 4: Đáp án D
PE được tạo ra bằng phản ứng trùng hợp etilen (CH2 = CH2).
Câu 5: Đáp án A
Anilin: C6H5 – NH2.
Câu 6: Đáp án D
Etyl fomat: HCOOC2H5 → CTPT là: C3H6O2.
Câu 7: Đáp án A
Tính khử của Cu < Fe, do đó phản ứng A không xảy ra.
Câu 8: Đáp án C
Amino axit là hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH).
→ NH2CH2COOH là amino axit.
Câu 9: Đáp án C
Ta có tính oxi hóa: Ca2+ < Zn2+ < Cu2+ < A+.
Câu 10: Đáp án B
Cu đứng sau H trong dãy hoạt động hóa học nên không tác dụng được với HCl.
Câu 11: Đáp án D
Glucozơ: C6H12O6.
Câu 12: Đáp án C
Thứ tự dãy hoạt động hóa học của kim loại: K, Na, Mg, Al ….
Vậy K có tính khử mạnh nhất.
Câu 13: Đáp án A
Metyl amin: CH3NH2.
Câu 14: Đáp án A
Bảo toàn electron có:
2.nFe = 2.nkhí → nFe = nkhí = 0,1 mol.
mFe = 0,1.56 = 5,6 gam.
Câu 15: Đáp án D
CH3COOCH3 + NaOH → CH3COONa + CH3OH.
Câu 16: Đáp án D
Tinh bột là polime thiên nhiên.
Câu 17: Đáp án B
Do thêm kim loại M vào dung dịch Fe2(SO4)3, khối lượng dung dịch tăng đúng bằng khối lượng kim loại phản ứng nên sau phản ứng không thu được kết tủa cũng không có khí thoát ra.
Vậy M là Cu.
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4.
Câu 18: Đáp án A
PVC được điều chế bằng phản ứng trùng hợp vinyl clorua.
B sai vì tơ visco thuộc loại tơ bán tổng hợp.
C sai vì amilozơ có cấu trúc mạch không phân nhánh.
Câu 19:Đáp án A
Thủy ngân phản ứng với lưu huỳnh ở ngay nhiệt độ thường.
Hg + S → HgS.
Câu 20: Đáp án A
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
→ a + b = 1 + 4 = 5.
Câu 21: Đáp án D
MAla – Ala – Ala = 3.89 – 2.18 = 231 (g/mol).
Câu 22: Đáp án C
Etylamin: C2H5NH2 có tính bazơ nên làm quỳ tím chuyển sang màu xanh.
Câu 23: Đáp án D
→ m = 0,2.108 = 21,6 gam.
Câu 24: Đáp án B
FeO + H2SO4 loãng → FeSO4 + H2O
Fe + 4HNO3 loãng → Fe(NO3)3 + NO + 2H2O
Fe + 2HCl → FeCl2 + H2
Fe(OH)2 + 2HCl → FeCl2 + 2H2O
Vậy cho Fe vào HNO3 loãng, dư thu được muối sắt (III).
Câu 25: Đáp án D
Ta có: C17H35COONa: 0,1 mol; C17H33COONa: 0,2 mol
Vậy X là: (C17H33COO)2C3H5OCOC17H35
(C17H33COO)2C3H5OCOC17H35 + 2Br2 → (C17H33Br2COO)2C3H5OCOC17H35
Xét 17,72 gam X → nX = 0,02 mol → nbrom = 2.nX = 0,04 (mol).
Câu 26: Đáp án A
Mg vừa tác dụng với HCl, vừa tác dụng với HNO3 đặc, nguội.
Cu không tác dụng với HCl nhưng tác dụng với HNO3 đặc, nguội.
Câu 27: Đáp án A
Bảo toàn H có nH2O = naxit = 0,32 mol.
Bảo toàn O có:
Cho NaOH phản ứng hết với Y, sau phản ứng dung dịch thu được chứa: Na+: 0,25 mol; SO42-: 0,12 mol; AlO2- x mol.
Bảo toàn điện tích → x = 0,25 – 2.0,12 = 0,01 (mol)
nOH-(trong ↓) = nOH- (ban đầu) – 4.nAlO2- = 0,25 – 4.0,01 = 0,21 (mol)
mKL (trong ↓) = m↓ - mOH-(trong ↓) = 7,63 – 0,21.17 = 4,06 gam.
Bảo toàn S có:
nS (trong FeS) + nS (trong axit) = nS (trong khí) + nS (trong SO42- ở Y)
→ nS (trong FeS) = 0,24 + 0,12 – 0,32 = 0,04 mol
→ m = mKL(trong ↓) + mS (trong FeS) + mAl (trong AlO2-) = 4,06 + 0,04.32 + 0,01.27 = 5,61 gam.
Câu 28: Đáp án A
Giả sử H = 100% → ntinh bột = 0,2/n (mol) → mtinh bột = m = 0,2/n .162n = 32,4 gam.
Do H = 80% nên m = 32,4/80% = 40,5 gam.
Câu 29: Đáp án B
Este X có dạng: RCOOC2H5
RCOOC2H5 + NaOH (0,1) → RCOONa + C2H5OH (0,1 mol)
Bảo toàn khối lượng có:
mX + mNaOH = mmuối + mancol → mX = 8,2 + 4,6 – 0,1.40 = 8,8 gam.
Câu 30: Đáp án B
(a) (b) (d) (e) đúng
(c) sai vì Saccarozơ tham gia phản ứng thủy phân trong môi trường axit hoặc xúc tác enzim.
Câu 31: Đáp án C
Fe + FeCl2 → không phản ứng
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + NaCl → không phản ứng.
Câu 32: Đáp án D
Gọi số mol của glyxin và etylamin lần lượt là x và y mol.
Khi cho X vào NaOH chỉ có glyxin phản ứng.
nGly = nNaOH = 0,2 mol
Cho X tác dụng với NaCl thì cả glyxin và etylamin phản ứng:
nHCl = nGlyxin + netylamin = 0,2 + 0,1 = 0,3 mol → VHCl = 0,3/1 = 0,3 lít = 300ml.
Bảo toàn khối lượng có: mmuối = mX + maxit = 19,5 + 0,3.36,5 = 30,45 gam.
Câu 33: Đáp án B
Fe + CuSO4 → FeSO4 + Cu
Hiện tượng: Dung dịch nhạt màu dần, có lớp kim loại màu đỏ bám ngoài đinh sắt.
Câu 34: Đáp án D
Metanol (CH3OH) không phản ứng với Cu(OH)2.
Câu 35: Đáp án C
Fe (0,06) + CuSO4 (0,015 mol) → Cu + FeSO4
Sau phản ứng CuSO4 hết, Fe dư.
m = 3,36 + (64 – 56).0,015 = 3,48 gam.
Câu 36: Đáp án C
Bảo toàn khối lượng có: mkhí = mmuối – mKL = 25,52 – 5,64 = 19,88 gam
→ nkhí = 19,88/71 = 0,28 mol, Vkhí = 0,28.22,4 = 6,272 lít.
Câu 37:
mCt = mKOH = 1.56 = 56 gam.
mdd = mKL + mnước - mkhí = 39 + 362 – 0,5.1 = 400 gam.
Câu 38: Đáp án B
Đặt X có dạng: H2N – R – COOH.
H2N – R – COOH + NaOH → H2N – R – COONa + H2O
Cứ 1 mol X thu được 1 mol muối → khối lượng tăng 22 gam
→ Khối lượng tăng 26,64 – 21,36 = 5,28 gam → nX = 0,24 mol.
→ MX = 21,36 : 0,24 = 89. Mà X là α-amino axit nên có CTCT là: H2N-CH(CH3)-COOH.
Câu 39: Đáp án B
Sau phản ứng thu được 2 muối: H2N-CH2-COONa: 0,1 mol và H2N-CH(CH3)-COONa: 0,1 mol
mmuối = 0,1 (97 + 111) = 20,8 gam.
Câu 40:
nCO2 = 0,2 mol; nH2 = 0,05 mol → n(-OH ancol) = 0,1 mol → nC (trong ancol) ≥ 0,1 mol;
nNaOH = nO (trong Z) = 0,1 → nC (muối) ≥ 0,1 mol.
nC (trong E) = nC (trong ancol) + nC (muối) = nCO2 = 0,2 mol
→ nC (trong ancol) = 0,1 mol; nC (muối) = 0,1 mol.
→ Ancol có số C = số O; muối có số C = số Na. Vậy ancol là CH3OH (0,1 mol); các muối là HCOONa a mol và (COONa)2 b mol
Bảo toàn Na có: a + 2b = nNaOH = 0,1 mol (1).
mmuối = 6,76 gam → 68a + 134b = 6,76 gam (2)
Từ (1) và (2) có a = 0,06 và b = 0,02.
X là HCOOCH3 0,06 mol và Y là (COOCH3)2 0,02 mol.
…………………………….Hết……………………………