Với giải Câu hỏi 2 trang 37 Khoa học tự nhiên lớp 7 Kết nối tri thức với cuộc sống chi tiết trong Bài 6: Giới thiệu về liên kết hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Khoa học tự nhiên 7. Mời các bạn đón xem:
Giải bài tập Khoa học tự nhiên lớp 7 Bài 6: Giới thiệu về liên kết hóa học
Câu hỏi 2 trang 37 KHTN lớp 7: Cho sơ đồ mô tả sự hình thành liên kết ion trong phân tử magnesium oxide như sau:
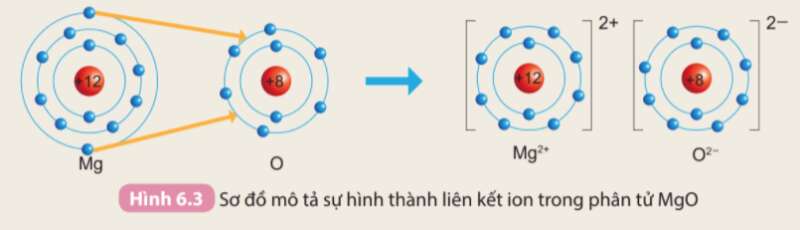
Hãy cho biết nguyên tử Mg đã nhường hay nhận bao nhiêu electron
Phương pháp giải:
Quan sát Hình 6.3, đếm tổng các quả cầu màu xanh của nguyên tử Mg và ion Mg2+
=> Nguyên tử Mg đã nhường hay nhận bao nhiêu electron
Trả lời:
- Nguyên tử Mg có tất cả 12 electron. Ion Mg2+ có tất cả 10 electron
=> Mất đi 2 electron ở lớp vỏ ngoài cùng
=> Nguyên tử Mg đã nhường đi 2 electron ở lớp vỏ ngoài cùng
Lý thuyết Liên kết ion
- Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
- Khi kim loại tác dụng với phi kim, nguyên tử kim loại nhường electron cho nguyên tử phi kim. Nguyên tử kim loại trở thành ion dương và nguyên tử phi kim trở thành ion âm. Các ion dương và âm hút nhau tạo thành liên kết trong hợp chất ion.
Ví dụ: Sự hình thành liên kết trong phân tử muối ăn (NaCl)
+ Nguyên tử sodium (Na) nhường một electron ở lớp electron ngoài cùng cho nguyên tử chlorine (Cl) đề tạo thành ion dương Na+ có vỏ bền vững giống vỏ nguyên tử khí hiếm He.
+ Nguyên tử Cl nhận vào lớp electron ngoài cùng một electron của nguyên tử Na để tạo thành ion âm Cl- có vỏ bền vững giống vỏ nguyên tử khí hiếm Ar.
+ Hai ion được tạo thành mang điện tích ngược dấu hút nhau để hình thành liên kết ion trong phân tử muối ăn.
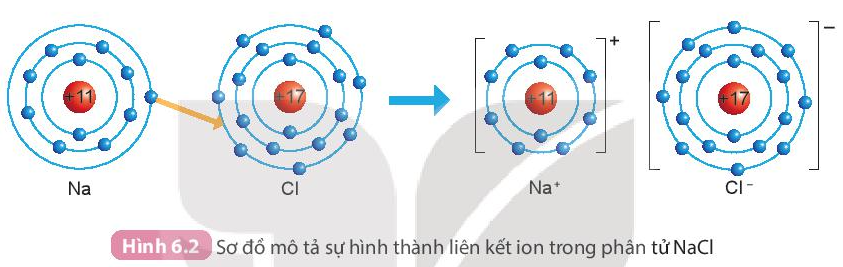
- Liên kết ion thường được tạo thành giữa kim loại điển hình và phi kim điển hình.
+ Các hợp chất ion như muối ăn … là chất rắn ở điều kiện thường, khó bay hơi, khó nóng chảy và khi tan trong nước tạo thành dung dịch dẫn được điện.
Xem thêm các bài giải Khoa học tự nhiên lớp 7 Kết nối tri thức hay, chi tiết khác:
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Kết nối tri thức hay, chi tiết khác:
Bài 5: Phân tử - Đơn chất - Hợp chất
Bài 6: Giới thiệu về liên kết hóa học