Với giải Câu hỏi trang 36 Khoa học tự nhiên lớp 7 Kết nối tri thức với cuộc sống chi tiết trong Bài 6: Giới thiệu về liên kết hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Khoa học tự nhiên 7. Mời các bạn đón xem:
Giải bài tập Khoa học tự nhiên lớp 7 Bài 6: Giới thiệu về liên kết hóa học
Câu hỏi trang 36 KHTN lớp 7: Quan sát Hình 6.1, so sánh số electron lớp ngoài cùng của He, Ne và Ar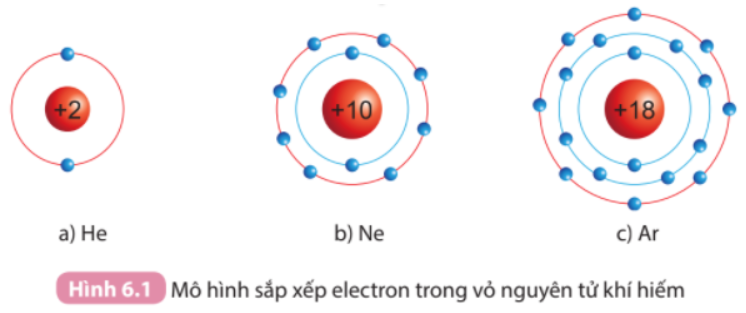
Phương pháp giải:
- Electron là các quả cầu màu xanh nằm trên đường tròn bao quanh hạt nhân
- Lớp ngoài cùng là đường tròn màu đỏ
Trả lời:
- He có 2 electron ở lớp vỏ ngoài cùng
- Ne có 8 electron ở lớp vỏ ngoài cùng
- Ar có 8 electron ở lớp vỏ ngoài cùng
=> Nguyên tố He có số electron ở lớp vỏ ngoài cùng ít hơn. Nguyên tố Ne và Ar có số electron ở lớp vỏ ngoài cùng bằng nhau (đều bằng 8)
Lý thuyết Cấu trúc electron bền vững của khí hiếm
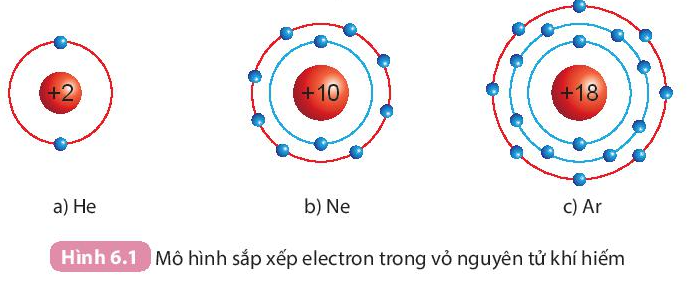
- Ở điều kiện thường, các khí hiếm tồn tại dưới dạng đơn nguyên tử bền vững, khó bị biến đổi hóa học. Lớp electron ngoài cùng của chúng chứa 8 electron (trừ He chứa 2 electron).
- Nguyên tử của các nguyên tố khác có xu hướng tham gia liên kết hóa học để đạt được lớp electron ngoài cùng giống khí hiếm bằng cách nhường, nhận hay dùng chung electron.
Xem thêm các bài giải Khoa học tự nhiên lớp 7 Kết nối tri thức hay, chi tiết khác:
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Kết nối tri thức hay, chi tiết khác:
Bài 5: Phân tử - Đơn chất - Hợp chất
Bài 6: Giới thiệu về liên kết hóa học
Bài 7: Hóa trị và công thức hóa học