Với giải Câu 5 trang 52 Hóa học lớp 10 Kết nối tri thức với cuộc sống chi tiết trong Bài 11: Liên kết ion giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 11: Liên kết ion
Câu 5 trang 52 Hóa học 10: Mô tả sự tạo thành liên kết ion trong:
a) Calcium oxide
b) Magnesium chloride.
Phương pháp giải:
Khi kim loại kết hợp với phi kim, kim loại tạo ion dương (cation) và phi kim tạo ion âm (anion). Các ion này tích điện trái dấu sẽ hút nhau tạo thành liên kết ion.
Lời giải:
a) Calcium oxide: Khi kim loại calcium kết hợp với phi kim oxygen, tạo thành các ion Ca2+ và O2-. Các ion này tích điện trái dấu sẽ hút nhau tạo thành liên kết ion.
Quá trình biểu diễn sự tạo thành liên kết ion trong phân tử CaO như sau:
Ca → Ca2+ + 2e
O + 2e → O2-
Ca2+ + O2- → CaO
b) Magnesium chloride: Khi kim loại magnesium kết hợp với phi kim chlorine, tạo thành các ion Mg2+ và Cl-. Các ion này tích điện trái dấu sẽ hút nhau tạo thành liên kết ion.
Quá trình biểu diễn sự tạo thành liên kết ion trong phân tử MgCl2 như sau:
Cl + 1e → Cl-
Mg → Mg2+ + 2e
Cl + 1e → Cl-
Cl- + Mg2+ + Cl- → MgCl2
Lý thuyết Sự tạo thành liên kết ion
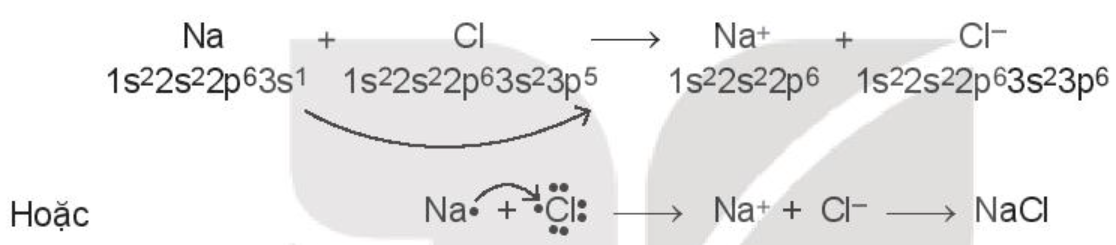
Ví dụ 1: Xét sự tạo thành liên kết hóa học trong phân tử sodium chloride (NaCl):
Khi kim loại sodium kết hợp với phi kim chlorine, tạo thành các ion Na+ và Cl-, các ion này mang điện tích trái dấu sẽ hút nhau tạo thành liên kết ion.
Ví dụ 2: Xét sự thành thành liên kết hóa học trong phân tử calcium chloride (CaCl2):
Khi kim loại calcium kết hợp với phi kim chlorine, tạo thành các ion Ca2+ và Cl-. Các ion này mang điện tích trái dấu sẽ hút nhau tạo thành liên kết ion.

Kết luận:
- Lực hút tĩnh điện giữa các ion mang điện trái dấu trong phân tử (hay tinh thể) tạo ra liên kết ion.
- Liên kết ion thường được hình thành giữa kim loại điển hình và phi kim điển hình. Các hợp chất tạo nên từ các ion được gọi là những hợp chất ion.
Xem thêm các bài giải Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Câu 1 trang 52 Hóa học 10: Hoàn thành các sơ đồ tạo thành ion sau:...
Câu 3 trang 52 Hóa học 10: Vì sao một ion O2- kết hợp được với hai ion Li+?...
Câu 6 trang 54 Hóa học 10: a) Vì sao muối ăn có nhiệt độ nóng chảy cao (8010C)?...
Xem thêm các bài giải SGK Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 13: Liên kết hydrogen và tương tác van der waals