Với Giải hóa học lớp 10 trang 54 Chân trời sáng tạo chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 54 Chân trời sáng tạo
Câu hỏi 5 trang 54 Hóa học 10: Trình bày sự hình thành ion lithium. Cho biết ion lithium có cấu hình electron của khí hiếm tương ứng nào?
Phương pháp giải:
- Viết cấu hình electron của Lithium => Xu hướng nhường hay nhận electron
Lời giải:
- Lithium có số hiệu nguyên tử: Z = 3 => Cấu hình electron: 1s22s1
=> Lithium có xu hướng nhường 1 electron để đạt cấu hình electron bền vững của khí hiếm He
1s22s1 → 1s2 + 1e
Luyện tập trang 54 Hóa học 10: Biết phân tử magnesium oxide hình thành bởi các ion Mg2+ và O2-. Vận dụng quy tắc octet, trình bày sự hình thành các ion trên từ những nguyên tử tương ứng.
Phương pháp giải:
- Nguyên tử Mg có 2 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 2 electron
- Nguyên tử O có 6 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 2 electron
Lời giải:
- Nguyên tử Mg có Z = 12 => Cấu hình electron: 1s22s22p63s2
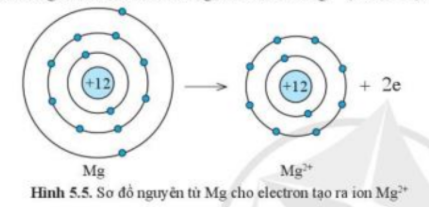
=> Nguyên tử Mg sẽ nhường 2 electron tạo thành ion Mg2+ để đạt cấu hình electron bền vững của khí hiếm:
1s22s22p63s2 → 1s22s22p6 + 2e ( Mg → Mg2+ + 2e)
- Nguyên tử O có Z = 8 => Cấu hình electron: 1s22s22p4
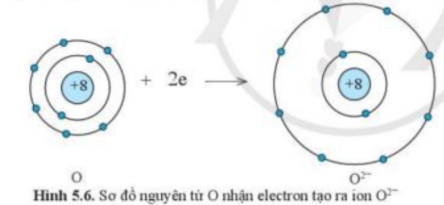
=> Nguyên tử O sẽ nhận 2 electron tạo thành ion O2- để đạt cấu hình electron bền vững của khí hiếm:
1s22s22p4 + 2e → 1s22s22p6 ( O + 2e → O2-)
Bài 1 trang 54 Hóa học 10: Nguyên tử của nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khí hiếm argon khi tham gia hình thành liên kết hóa học?
A. Fluorine
B. Oxygen
C. Hydrogen
D. Chlorine
Phương pháp giải:
Cấu hình electron khí hiếm Argon: 1s22s22p63s23p6
Lời giải:
- Fluorine (Z = 9): 1s22s22p5 => Có xu hướng nhận 1 electron thành F- có cấu hình: 1s22s22p6
- Oxygen (Z = 8): 1s22s22p4 => Có xu hướng nhận 2 electron thành O2- có cấu hình: 1s22s22p6
- Hydrogen (Z = 1): 1s1 => Có xu hướng góp chung 1 electron để tạo thành 1 cặp electron dùng chung đạt cấu hình: 1s2
- Chlorine (Z = 17): 1s22s22p63s23p5 => Có xu hướng nhận 1 electron thành Cl- có cấu hình: 1s22s22p63s23p6
=> Nguyên tử của nguyên tố chlorine có xu hướng đạt cấu hình electron bền vững của khí hiếm argon
Đáp án D
Bài 2 trang 54 Hóa học 10: Để đạt quy tắc octet, nguyên tử của nguyên tố potassium (Z = 19) phải nhường đi
A. 2 electron
B. 3 electron
C. 1 electron
D. 4 electron
Phương pháp giải:
- Viết cấu hình electron của nguyên tử potassium
=> Xu hướng nhường bao nhiêu electron
Lời giải:
- Nguyên tử potassium có Z = 19
=> Cấu hình electron: 1s22s22p63s23p64s1
=> Có xu hướng nhường 1 electron để đạt cấu hình electron bền vững của khí hiếm Argon: 1s22s22p63s23p6
Đáp án C
Bài 3 trang 54 Hóa học 10: Vận dụng quy tắc octet, trình bày sơ đồ mô tả sự hình thành phân tử potassium chloride (KCl) từ nguyên tử của các nguyên tố potassium và chlorine.
Phương pháp giải:
Bước 1: Viết cấu hình electron của nguyên tử K và Cl => Xu hướng nhường hay nhận electron của K và Cl
Bước 2: Vẽ sơ đồ mô tả
Lời giải:
- Nguyên tử K (Z = 19): 1s22s22p63s23p64s1 => Có xu hướng nhường 1 electron
- Nguyên tử Cl (Z = 17): 1s22s22p63s23p5 => Có xu hướng nhận 1 electron
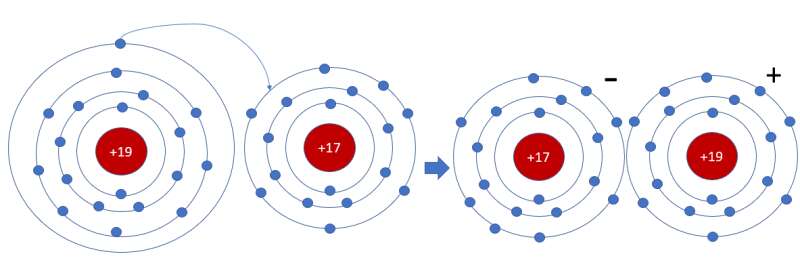
=> Nguyên tử Cl sẽ nhận 1 electron của nguyên tử K để hình thành phân tử potassium chlorine (KCl)
- Sơ đồ mô tả:
Bài 4 trang 54 Hóa học 10: Giải thích sự hình thành liên kết trong phân tử H2O bằng cách áp dụng quy tắc octet
Phương pháp giải:
Bước 1: Viết cấu hình electron của O và H => Xu hướng nhường hay nhận electron của O và H
Bước 2: Vẽ sơ đồ mô tả
Lời giải:
- Nguyên tử O (Z = 8): 1s22s22p4 => Có xu hướng nhận 2 electron
- Nguyên tử H (Z = 1): 1s1 => Có xu hướng nhận 1 electron
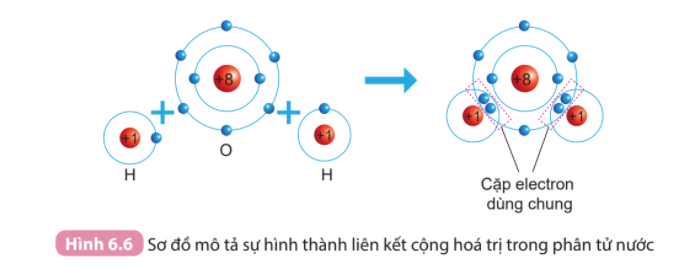
=> Mỗi nguyên tử H sẽ bỏ ra 1 electron và góp chung với 2 electron của nguyên tử O tạo thành 2 cặp electron dùng chung
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác: