Với Giải hóa học lớp 10 trang 24 Kết nối tri thức chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 24 Kết nối tri thức
Câu 6 trang 24 Hóa học 10: Cấu hình electron của nguyên tử có Z = 16 là
A. 1s22s22p63s23p3
B. 1s22s22p63s23p5
C. 1s22s22p63s23p4
D. 1s22s22p63s23p6
Phương pháp giải:
Bước 1: Xác định số electron trong nguyên tử
Bước 2: Viết thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng:
1s 2s 2p 3s 3p 4s 3d…
Bước 3: Điền các electron vào các phân lớp theo nguyên lí vững bền cho đến electron cuối cùng
Lời giải:
- Nguyên tử có Z = 16 => Có 16 electron
- Viết theo thứ tự: 1s 2s 2p 3s 3p 4s 3d… (trong đó phân lớp s chứa tối ta 2 electron, phân lớp p chứa tối đa 6 electron, phân lớp d chứa tối đa 10 electron, phân lớp f chứa tối đa 14 electron)
- Điền các electron: 1s22s22p63s23p4
Đáp án C
Câu 7 trang 24 Hóa học 10: Biểu diễn cấu hình electron của các nguyên tử có Z = 8 và Z = 11 theo ô orbital
Phương pháp giải:
Bước 1: Viết cấu hình electron của nguyên tử
Bước 2: Vẽ các AO ứng với mỗi phân lớp trong đó ( phân lớp s có 1 AO, phân lớp p có 3 AO, phân lớp d có 5 AO, phân lớp f có 7 AO)
+ Mỗi AO chứa tối đa 2 electron được biểu diễn bằng 2 mũi tên ngược chiều nhau và phân bố trên các orbital sao cho số electron độc thân là tối đa (quy tắc Hund)
Lời giải:
- Nguyên tử có Z = 8 => Có 8 electron
- Điền các electron: 1s22s22p4
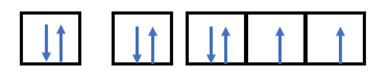
- Nguyên tử có Z = 11 => Có 11 electron
- Điền các electron: 1s22s22p63s1
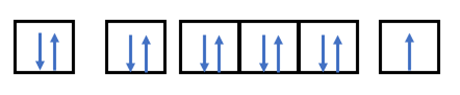
Xem thêm các bài giải Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác: