Tailieumoi.vn xin giới thiệu Trắc nghiệm Hóa học lớp 10 Bài 18: Hydrogen halide và một số phản ứng của ion halide sách Chân trời sáng tạo. Bài viết gồm 20 câu hỏi trắc nghiệm với đầy đủ các mức độ và có hướng dẫn giải chi tiết sẽ giúp học sinh ôn luyện kiến thức và rèn luyện kĩ năng làm bài trắc nghiệm Hóa học 10. Ngoài ra, bài viết còn có phần tóm tắt nội dung chính lý thuyết Bài 18: Hydrogen halide và một số phản ứng của ion halide. Mời các bạn đón xem:
Trắc nghiệm Hóa học 10 Bài 18: Hydrogen halide và một số phản ứng của ion halide
Phần 1: Trắc nghiệm Bài 18: Hydrogen halide và một số phản ứng của ion halide
Câu 1. Cho phản ứng: NaCl + H2SO4 đặc
Sản phẩm thu được là
A. NaHSO4 và HCl;
B. Cl2, SO2, Na2SO4 và H2O;
C. Na2SO4 và HCl;
D. Không phản ứng.
Đáp án đúng là: C
2NaCl + H2SO4 đặc Na2SO4 + 2HCl ↑
Câu 2. Khi phản ứng với sulfuric acid đặc thì:
(1) Ion Cl− khử H2SO4 trong dung dịch H2SO4 đặc thành SO2.
(2) Ion Br− khử H2SO4 trong dung dịch H2SO4 đặc thành SO2.
(3) Ion I− khử H2SO4 trong dung dịch H2SO4 đặc thành H2S, S, SO2 tùy vào điều kiện phản ứng.
Khẳng định đúng là
A. (1)
B. (1), (2) và (3)
C. (2) và (3)
D. (1) và (2)
Đáp án đúng là: C
Khi phản ứng với sulfuric acid đặc thì:
(1) Ion Cl− khử H2SO4 trong dung dịch H2SO4 đặc thành SO2 ⇒ sai. Vì ion Cl− không khử được H2SO4 nên chỉ xảy ra phản ứng trao đổi.
(2) Ion Br− khử H2SO4 trong dung dịch H2SO4 đặc thành SO2 ⇒ đúng.
(3) Ion I− khử H2SO4 trong dung dịch H2SO4 đặc thành H2S, S, SO2 tùy vào điều kiện phản ứng ⇒ đúng.
Câu 3. Hydrohalic acid có tính acid mạnh nhất là
A. Hydrochloric acid;
B. Hydrofluoric acid;
C. Hydrobromic acid;
D. Hydroiodic acid.
Đáp án đúng là: D
Tính acid của các hydrohalic acid tăng dần từ hydrochloric acid (HF) đến hydroiodic acid (HI).
Do đó hydroiodic acid có tính acid mạnh nhất.
Câu 4. Nguyên nhân chủ yếu làm tăng độ mạnh của các acid theo dãy từ HF đến HI là do
A. sự tăng khối lượng phân tử từ HF đến HI;
B. sự giảm độ phân cực của liên kết từ HF đến HI;
C. sự giảm độ bền liên kết từ HF đến HI;
D. sự tăng kích thước từ HF đến HI.
Đáp án đúng là: C
Nguyên nhân chủ yếu làm tăng độ mạnh của các acid theo dãy từ HF đến HI là do sự giảm độ bền liên kết từ HF đến HI (năng lượng liên kết giảm, độ dài liên kết tăng).
Câu 5. Phản ứng nào dưới đây chứng minh tính khử của các ion halide?
A. BaCl2 + H2SO4 ⟶ BaSO4 ↓ + 2HCl;
B. HI + NaOH ⟶ NaI + H2O;
C. 2HBr + H2SO4 ⟶ Br2 + SO2 ↑ + 2H2O;
D. CaO + 2HCl ⟶ CaCl2 + H2O.
Đáp án đúng là: C
+ H2SO4 ⟶ BaSO4 ↓ + 2
+ NaOH ⟶+ H2O
CaO + 2⟶+ H2O
Phản ứng chứng minh tính khử của các ion halide là:
2+ H2SO4 ⟶ + SO2 ↑ + 2H2O
Bromide có số oxi hóa tăng từ − 1 lên 0, thể hiện tính khử trong phản ứng.
Câu 6. Hydrogen halide là
A. đơn chất halogen (X2);
B. hợp chất của hydrogen với halogen (HX);
C. hợp chất của hydrogen với chlorine (HCl);
D. hợp chất của hydrogen với halogen và oxygen (HXO).
Đáp án đúng là: B
Hydrogen halide là hợp chất của hydrogen với halogen (HX).
Câu 7. Hydrogen halide có nhiệt độ sôi cao nhất là
A. HF;
B. HCl;
C. HBr;
D. HI.
Đáp án đúng là: A
Từ HCl đến HI nhiệt độ sôi tăng dần. Riêng HF có nhiệt độ sôi cao nhất, cao bất thường do tạo được liên kết hydrogen liên phân tử.
… H – F … H – F …
Câu 8. Quá trình ion halide bị oxi hóa thành đơn chất tương ứng là
A. ⟶ + 2e;
B. + 2e ⟶ ;
C. + 2e ⟶ ;
D. ⟶ + 2e.
Đáp án đúng là: A
Quá trình ion halide bị oxi hóa thành đơn chất tương ứng là ⟶ + 2e.
Câu 9. Nhận định sai khi nói về tính acid của các dung dịch HCl, HBr, HI là
A. làm quỳ tím chuyển màu xanh;
B. tác dụng với kim loại đứng trước hydrogen trong dãy hoạt động hóa học;
C. tác dụng với basic oxide, base;
D. tác dụng với một số muối.
Đáp án đúng là: A
Các dung dịch HCl, HBr, HI có tính acid nên làm quỳ tím chuyển màu đỏ.
Do đó, nhận định A sai.
Câu 10. Cho phản ứng: KI + H2SO4⟶ I2 + H2S + K2SO4 + H2O
Hệ số cân bằng của H2SO4 là
A. 8
B. 5
C. 4
D. 3
Đáp án đúng là: B
+ ⟶ + + K2SO4 + H2O
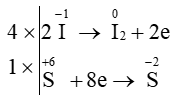
⇒ 8 + 5 ⟶ 4 + + 4K2SO4 + 4H2O
Câu 11. Trong các ion halide X-, ion có tính khử mạnh nhất là
A. F−
B. I−
C. Br−
D. Cl−
Đáp án đúng là: B
Trong các ion halide X−,ion có tính khử mạnh nhất là I−.
Câu 12. Dung dịch hydrohalic acid nào không được bảo quản trong lọ thủy tinh?
A. HCl;
B. HF;
C. HBr;
D. HI.
Đáp án đúng là: B
Hydrofluoric acid (HF) có tính chất đặc biệt là ăn mòn thủy tinh theo phản ứng:
SiO2 + 4HF ⟶ SiF4 + 2H2O
Do đó không bảo quản dung dịch HF trong lọ thủy tinh.
Câu 13. Nhỏ vài giọt dung dịch silver nitrate vào ống nghiệm chứa dung dịch hydrohalic acid thì thấy không có hiện tượng xảy ra. Công thức của hydrohalic acid đó là
A. HCl;
B. HF;
C. HBr;
D. HI.
Đáp án đúng là: B
AgNO3 (aq) + HF (aq) ⟶ Không xảy ra phản ứng.
Do đó, không có hiện tượng xảy ra.
Câu 14. Thuốc thử để phân biệt dung dịch NaCl và NaNO3 là
A. Dùng quỳ tím;
B. Dùng dung dịch H2SO4;
C. Dùng dung dịch Ca(OH)2;
D. Dùng dung dịch AgNO3.
Đáp án đúng là: D
AgNO3(aq)+ NaNO3(aq)⟶ không phản ứng.
Do đó không hiện tượng.
AgNO3(aq)+ NaCl(aq) ⟶ NaNO3(aq)+ AgCl (s)↓ (trắng)
Hiện tượng: xuất hiện kết tủa trắng.
Vậy thuốc thử để phân biệt dung dịch NaCl và NaNO3 là dung dịch AgNO3.
Câu 15. Dùng để loại bỏ gỉ thép; sản xuất chất tẩy rửa nhà vệ sinh, các hợp chất vô cơ và hữu cơ phục vụ cho đời sống, sản xuất… là ứng dụng của
A. hydrogen fluoride;
B. hydrogen chloride;
C. hydrogen bromide;
D. hydrogen iodide;
Đáp án đúng là: B
Dùng để loại bỏ gỉ thép; sản xuất chất tẩy rửa nhà vệ sinh, các hợp chất vô cơ và hữu cơ phục vụ cho đời sống, sản xuất… là ứng dụng của hydrogen chloride.
Phần 2: Lý thuyết Bài 18: Hydrogen halide và một số phản ứng của ion halide
I. Tính chất vật lí của hydrogen halide
- Hydrogen halide là hợp chất của hydrogen với halogen, công thức tổng quát là HX, với X là halogen. Hậu tố “ide” trong hydrogen halide được thay thế từ hậu tố “ine” của tên halogen.
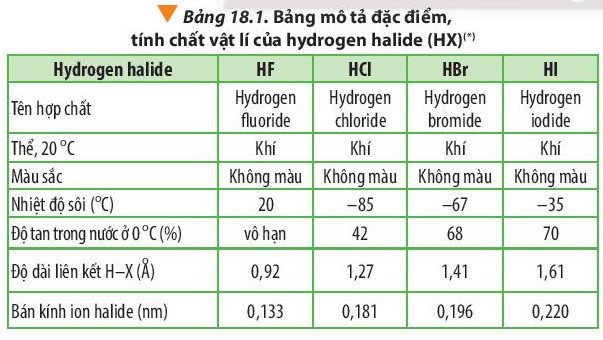
+ Nhiệt độ sôi của các hydrogen halide tăng dần từ HCl đến HI.
Giải thích: Khối lượng phân tử tăng làm tăng năng lượng cần thiết cho quá trình sôi; đồng thời, sự tăng kích thước và số electron trong phân tử dẫn đến tương tác van der Waals giữa các phân tử tăng.
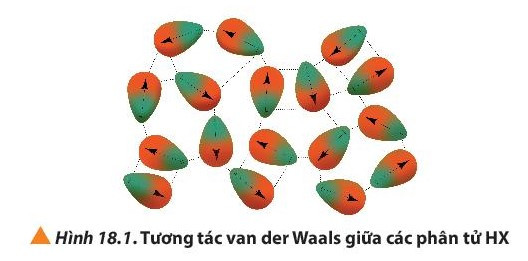
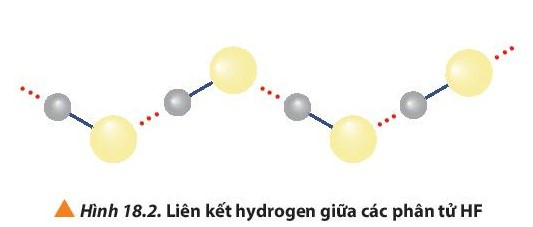
+ Các phân tử hydrogen fluoride hình thành liên kết hydrogen liên phân tử, loại liên kết này bền hơn tương tác van der Waals, nên nhiệt độ sôi của hydrogen flouride cao bất thường so với các hydrogen halide còn lại.
+ Nhờ liên kết hydrogen giữa các phân tử nên hydrogen fluoride khó bay hơi hơn các hydrogen halide còn lại.
II. Hydrohalic acid
- Các hydrogen halide tan trong nước, tạo thành hydrohalic acid tương ứng.
- Tính acid của các hydrohalic acid tăng dần từ hydrofluoric acid đến hydroiodic acid.
- Hydrofluoric acid (HF) là acid rất yếu, nhưng có tính chất đặc biệt là ăn mòn thủy tinh, phương trình hóa học của phản ứng:
SiO2 + 4HF → SiF4↑ + 2H2O
- Các dung dịch HCl, HBr, HI là những acid mạnh, có đầy đủ tính chất hóa học chung của acid như: làm quỳ tím chuyển sang màu đỏ, tác dụng với kim loại đứng trước hydrogen trong dãy hoạt động hóa học, tác dụng với basic oxide, base và một số muối.
Ví dụ:
NaOH + HCl → NaCl + H2O
Zn + 2HCl → ZnCl2 + H2
CaO + 2HBr → CaBr2 + H2O
K2CO3 + 2HI → 2KI + H2O + CO2
III. Tính khử của các ion halide
- Trong ion halide, các halogen có số oxi hóa thấp nhất là -1, do đó ion halide chỉ thể hiện tính khử trong phản ứng oxi hóa – khử.
- Tính khử của các ion halide tăng theo chiều: F- < Cl- < Br- < I-
Ví dụ: Khi đun nóng các muối khan halide với H2SO4 đặc:
+ Ion chloride không khử được H2SO4 nên chỉ xảy ra phản ứng trao đổi.
KCl + H2SO4 (đặc) → KHSO4 + HCl↑
+ Ion bromide khử H2SO4 đặc thành SO2 và Br- bị oxi hóa thành Br2, sản phẩm có màu vàng đậm.
2KBr + 2H2SO4 (đặc) → Br2 + SO2↑ + K2SO4 + 2H2O
+ Ion iodide có thể khử H2SO4 đặc thành H2S, S, SO2 tùy vào điều kiện phản ứng và I- bị oxi hóa thành I2 có màu đen tím.
2KI + 2H2SO4 (đặc) → I2↓ + SO2↑ + K2SO4 + 2H2O
6KI + 4H2SO4 (đặc) → 3I2↓ + S↓ + 3K2SO4 + 4H2O
8KI + 5H2SO4 (đặc) → 4I2 + H2S↑ + 4K2SO4 + 4H2O
IV. Nhận biết ion halide trong dung dịch
- Phân biệt các ion F-, Cl-, Br- và I- bằng cách cho dung dịch silver nitrate (AgNO3) vào dung dịch muối của chúng.
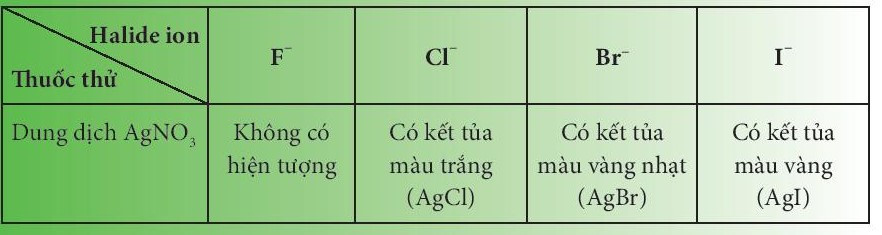
- Phương trình hóa học minh họa:
NaF + AgNO3 → không phản ứng
NaCl + AgNO3 → AgCl↓ + NaNO3
NaBr + AgNO3 → AgBr↓ + NaNO3
NaI + AgNO3 → AgI↓ + NaNO3

V. Ứng dụng của các hydrogen halide
- Hydrogen fluoride: Dùng để tẩy cặn trong các thiết bị trao đổi nhiệt; chất xúc tác trong các nhà máy lọc dầu, công nghệ làm giàu uranium, sản xuất dược phẩm, …
- Hydrogen chloride: Dùng để loại bỏ gỉ thép, sản xuất chất tẩy rửa nhà vệ sinh, các hợp chất vô cơ và hữu cơ phục vụ đời sống và sản xuất,…
- Hydrogen bromide: Làm chất xúc tác cho các phản ứng hữu cơ, tổng hợp chất chống cháy chứa nguyên tố bromine như tetrabromobisphenol A, điều chế nhựa epoxy, sản xuất các vi mạch điện tử.
- Hydrogen iodide: Dùng làm chất khử phổ biến trong các phản ứng hóa học; sản xuất iodine và ankyl iodide...
Xem thêm các bài trắc nghiệm Hóa học 10 Chân trời sáng tạo hay, chi tiết khác:
Trắc nghiệm Hóa 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Trắc nghiệm Hóa 10 Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Trắc nghiệm Hóa 10 Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Trắc nghiệm Hóa 10 Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Trắc nghiệm Hóa 10 Bài 18: Hydrogen halide và một số phản ứng của ion halide