Với giải Luyện tập 8 trang 43 Khoa học tự nhiên lớp 7 Cánh diều chi tiết trong Bài 6: Hóa trị, công thức hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Khoa học tự nhiên 7. Mời các bạn đón xem:
Giải bài tập Khoa học tự nhiên lớp 7 Bài 6: Hóa trị, công thức hóa học
Luyện tập 8 trang 43 KHTN lớp 7: Calcium carbonate là thành phần chính của đá vôi, có công thức hóa học là CaCO3. Tính phần trăm khối lượng của mỗi nguyên tố trong hợp chất trên
Phương pháp giải:
Bước 1: Tính khối lượng mỗi nguyên tố có trong 1 phân tử hợp chất
Bước 2: Tính khối lượng phân tử
Bước 3: Tính phần trăm khối lượng của nguyên tố theo công thức:

Trả lời:
Calcicum carbonate gồm: 1 nguyên tử Ca, 1 nguyên tử C và 3 nguyên tử O
Ta có: Khối lượng của nguyên tố Ca trong CaCO3 là:
mCa = 1 x 40 amu = 40 amu
Khối lượng của nguyên tố C trong CaCO3 là:
mC = 1 x 12 amu = 12 amu
Khối lượng của nguyên tố O trong CaCO3 là:
mO = 3 x 16 amu = 48 amu
=> Khối lượng phân tử CaCO3 là: MCaCO3 = 40 + 12 + 48 = 100 amu
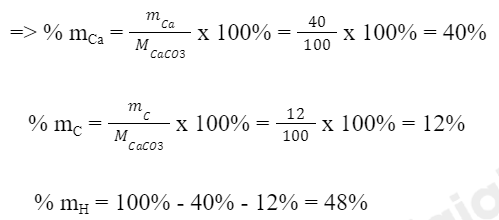
Lý thuyết Công thức hóa học
1. Công thức hóa học
- Công thức hóa học dùng để biểu diễn chất.
- Công thức hóa học gồm hai phần:
+ Phần chữ: gồm kí hiệu hóa học của nguyên tố tạo thành chất.
+ Phần số: gồm các số được ghi bên phải, dưới chân kí hiệu hóa học, ứng với số nguyên tử của nguyên tố trong một phân tử (nếu chỉ có một nguyên tử thì không ghi). Các số này được gọi là chỉ số.

- Công thức hóa học của hợp chất có hai kí hiệu hóa học trở lên.
Ví dụ: NaCl, CaO, HNO3, BaSO4,…
- Công thức hóa học của các đơn chất chỉ có một kí hiẹu hóa học.
+ Với phi kim, phân tử thường có hai nguyên tử.
Ví dụ: N2, H2, O2, Br2,…
+ Với kim loại và một số phi kim, kí hiệu hóa học của nguyên tố được coi là công thức hóa học của đơn chất.
Ví dụ: Kim loại: Fe, Cu, Al, Mg,… và phi kim: C, S, P,…
2. Ý nghĩa của công thức hóa học
Công thức hóa học của một số chất cho biết một số thông tin
+ Nguyên tố tạo ra chất.
+ Số nguyên tử của mỗi nguyên tố có trong một phân tử chất.
+ Khối lượng phân tử của chất.
Ví dụ: Công thức hóa học của nitric acid là HNO3:
+ Nitric acid được tạo thành từ H, N và O.
+ Trong một phân tử nitric acid có 1 nguyên tử H, 1 nguyên tử N và 3 nguyên tử O.
+ Khối lượng phân tử của nitric là:
1 × 1 amu + 1 × 14 amu + 3 × 16 amu = 63 amu
Biết công thức hóa học tính được phần trăm khối lượng các nguyên tố trong hợp chất
- Khi biết công thức hóa học của một chất, tính được thành phần phần trăm khối lượng của các nguyên tố tạo ra chất theo các bước sau:
+ Tính khối lượng mỗi nguyên tố có trong một phân tử hợp chất.
+ Tính khối lượng phân tử.
+ Tính phần trăm khối lượng của nguyên tố theo công thức:
(Khối lượng nguyên tố : Khối lượng phân tử hợp chất) × 100%
Ví dụ: Tính phần trăm khối lượng của Cu, O trong hợp chất CuO.
Hướng dẫn giải:
Ta có: Khối lượng của nguyên tố O trong CuO là:
mO = 1 × 16 amu = 16 amu
Khối lượng của nguyên tố Cu trong CuO là:
mCu = 1 × 64 amu = 64 amu
Khối lượng của phân tử CuO là: MCuO = 16 + 64 = 80 (amu)
Phần trăm khối lượng của Cu trong hợp chất CuO là:
Phần trăm về khối lượng của O trong hợp chất CuO là:
%mO = 100% - %mCu = 100% - 80% = 20%
Biết công thức hóa học và hóa trị của một nguyên tố, xác định được hóa trị của nguyên tố còn lại trong hợp chất
- Cách xác định hóa trị khi biết công thức hóa học và hóa trị của một nguyên tố:
+ Đặt hóa trị của nguyên tố chưa biết là a.
+ Xác định a dựa vào quy tắc hóa trị.
Ví dụ: Xác định hóa trị của Al trong hợp chất có công thực hóa học Al2O3.
Giải:
Gọi hóa trị của Al trong hợp chất là a.
Vì O có hóa trị II nên ta có biểu thức: a × 2 = II × 3 → a = III
Vậy Al có hóa trị III trong hợp chất Al2O3.
3. Xác định công thức hóa học của hợp chất khi biết hóa trị hoặc phần trăm khối lượng của các nguyên tố
a) Biết hóa trị của các nguyên tố, lập công thức hóa học của hợp chất tạo thành từ hai nguyên tố
- Nếu hai nguyên tố A, B có hóa trị tương ứng là a, b thì công thức hóa học của hợp chất tạo thành từ A và B được xác định như sau:
+ Đặt công thức hóa học của hợp chất AxBy.
+ Áp dụng quy tắc hóa trị, xác định tỉ lệ
+ Xác định x, y (x, y thường là những số nguyên tố nhỏ nhất thỏa mãn tỉ lệ trên).
Ví dụ: Lập công thức hóa học của hợp chất được tạo bởi S hóa trị IV và O.
Hướng dẫn giải
+ Đặt công thức của hợp chất là SxOy.
+ Theo quy tắc hóa trị: x × IV = y × II
+ Ta có tỉ lệ:
+ Công thức hóa học của hợp chất là: SO2.
b) Xác định công thức hóa học của hợp chất khi biết phần trăm khối lượng của các nguyên tố và khối lượng phân tử của hợp chất
- Khi biết phần trăm khối lượng của hai nguyên tố A, B tạo nên hợp chất và khối lượng phân tử của chất đó, xác định công thức hóa học theo bước sau:
+ Đặt công thức hóa học của hợp chất AxBy.
+ Tính khối lượng của A, B trong một phân tử chất.
+ Tìm x, y.
Ví dụ: R là hợp chất của Fe và O, khối lượng phân tử của R là 72 amu. Biết phần trăm khối lượng của oxygen trong R là 22,22%. Hãy xác định công thức hóa học của R.
Hướng dẫn giải
+ Đặt công thức hóa học của R là FexOy.
+ Khối lượng của nguyên tố O trong một phân tử R là:
+ Khối lượng của nguyên tố S trong một phân tử R là:
72 – 16 = 56 (amu)
+ Ta có: 16 amu × y = 16 amu ⇒ y = 1
56 amu × x = 56 amu ⇒ x = 1
Vậy công thức hóa học của R là FeO.
Xem thêm lời giải bài tập Khoa học tự nhiên 7 Cánh diều hay, chi tiết khác:
Câu hỏi 3 trang 41 KHTN lớp 7: Cho công thức hóa học của một số chất như sau:...
Luyện tập 5 trang 42 KHTN lớp 7: Viết công thức hóa học của các chất:...
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Bài 5: Giới thiệu về liên kết hóa học
Bài 6: Hóa trị, công thức hóa học
Bài 8: Đồ thị quãng đường - thời gian