Với giải Câu hỏi 5 trang 92 Hóa học lớp 10 Cánh diều chi tiết trong Bài 16: Tốc độ phản ứng hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 16: Tốc độ phản ứng hóa học
Câu hỏi 5 trang 92 Hóa học 10: Trong phản ứng (6), nếu nồng độ của H2tăng gấp đôi thì tốc độ phản ứng thay đổi như thế nào?
H2(g) + I2(g) → 2HI(g)
Phương pháp giải:
Theo định luật tác dụng khối lượng: v = kCH2.CI2
Lời giải:
Áp dụng định luật tác dụng khối lượng: v = kCH2.CI2
=> Ở một nhiệt độ không đổi, tốc độ phản ứng (6) tỉ lệ thuận với nồng độ của H2 cũng như nồng độ của I2
=> Nếu nồng độ của H2 tăng gấp đôi thì tốc độ phản ứng (6) tăng gấp đôi
Lý thuyết Định luật tác dụng khối lượng
- Thí nghiệm: Cho hai mảnh Zn có cùng khối lượng vào hai bình chứa cùng thể tích dung dịch H2SO4 loãng, dư, nồng độ dung dịch ở mỗi bình lần lượt là 0,5M và 1M.
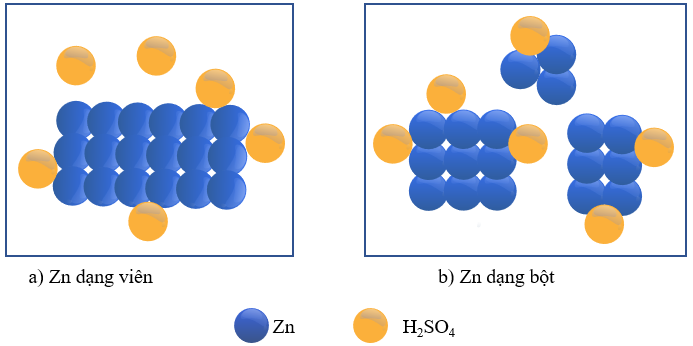
Hình 16.2. Minh họa mô hình Zn trong dung dịch H2SO4 loãng
- Giải thích: Để phản ứng xảy ra, cần phải có sự va chạm giữa H2SO4 và Zn. Nồng độ của H2SO4 ở bình (b) lớn gấp đôi nồng độ H2SO4 ở bình (a), do vậy số va chạm của H2SO4 với Zn trong bình (b) sẽ nhiều hơn, dẫn đến tốc độ phản ứng ở bình (b) là lớn hơn.
- Kết luận: Khi nồng độ các chất tham gia phản ứng càng lớn thì tốc độ phản ứng càng lớn.
- Giải thích: Để phản ứng xảy ra, các phân tử phản ứng phải va chạm với nhau, nồng độ càng lớn thì số lượng va chạm càng nhiều (trong cùng một đơn vị thời gian, một đơn vị thể tích) nên tốc độ phản ứng càng lớn.
- Định luật tác dụng khối lượng áp dụng cho các phản ứng đơn giản, biểu thị sự phụ thuộc tốc độ phản ứng theo nồng độ các chất phản ứng.
Lưu ý: Phản ứng đơn giản là phản ứng chỉ diễn ra qua một giai đoạn duy nhất, chất phản ứng tạo thành sản phẩm không qua một chất trung gian nào khác.
- Cho phản ứng tổng quát: aA + bB sản phẩm
+ Tốc độ phản ứng được tính như sau: v = k(4)
+ Trong đó: CA, CB là nồng độ mol. L-1 tương ứng của chất A và B; k là hằng số tốc độ phản ứng mà giá trị của nó chỉ phụ thuộc vào nhiệt độ và bản chất các chất tham gia phản ứng.
- Định luật tác dụng khối lượng: Tốc độ phản ứng tỉ lệ thuận với tích nồng độ các chất tham gia phản ứng với số mũ thích hợp.
® Hằng số tốc độ phản ứng càng lớn thì tốc độ phản ứng càng lớn.
- Hằng số tốc độ phản ứng có giá trị đúng bằng tốc độ phản ứng khi nồng độ các chất phản ứng bằng nhau và bằng 1M. Đây chính là ý nghĩa của hằng số tốc độ phản ứng.
Ví dụ: Phản ứng của N2 và H2 là phản ứng đơn giản:
N2(g) + 3H2(g) 2NH3(g) (5)
+ Theo định luật tác dụng khối lượng, tốc độ của phản ứng (5) được viết dưới dạng:
v = k
+ Ở một nhiệt độ không đổi, tốc độ phản ứng (5) tỉ lệ với nồng độ N2 và H2.
Lưu ý: Tốc độ phản ứng tính theo định luật tác dụng khối lượng là tốc độ tức thời của phản ứng tại một thời điểm, khác với tốc độ trung bình của phản ứng trong một khoảng thời gian như đã nêu trên.
Xem thêm lời giải bài tập Hóa Học 10 Cánh diều hay, chi tiết khác:
Vận dụng 3 trang 93 Hóa học 10: Hãy giải thích các hiện tượng dưới đây....
Vận dụng 4 trang 94 Hóa học 10: Giải thích vì sao thanh củi chẻ nhỏ hơn thì sẽ cháy nhanh hơn...
Xem thêm các bài giải SGK Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Bài 14 : Phản ứng hóa học và enthalpy
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Bài 16: Tốc độ phản ứng hóa học
Bài 17: Nguyên tố và đơn chất halogen
Bài 18: Hydrogen halide và hydrohalic acid