Với giải sách bài tập Khoa học tự nhiên 9 Bài 23: Ethylic alcohol sách Cánh diều hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Khoa học tự nhiên 9. Mời các bạn đón xem:
Giải SBT Khoa học tự nhiên 9 Bài 23: Ethylic alcohol
Bài 23.1 trang 63 Sách bài tập KHTN 9: Ethylic alcohol tác dụng được với Na còn ethane không tác dụng được với Na vì
A. khối lượng phân tử của ethylic alcohol lớn hơn khối lượng phân tử của ethane.
B. trong phân tử ethylic alcohol có nguyên tử oxygen còn trong phân ethane không có nguyên tử oxygen.
C. ethylic alcohol là chất lỏng còn ethane là chất khí.
D. trong phân tử ethylic alcohol có nhóm -OH còn trong phân tử ethane không có nhóm -OH.
Lời giải:
Đáp án đúng là: D
Ethylic alcohol tác dụng được với Na còn ethane không tác dụng được với Na vì trong phân tử ethylic alcohol có nhóm -OH còn trong phân tử ethane không có nhóm -OH.
Bài 23.2 trang 63 Sách bài tập KHTN 9: Trong số các chất sau: CH3 - OH, CH3 - O - CH3, CH3 - CH2 - CH2 - OH, CH3 – O – CH2 – CH3, 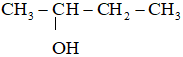
Số chất có tính chất hoá học tương tự ethylic alcohol là:
A. 2
B. 3
C. 4
D. 5
Lời giải:
Đáp án đúng là: B
Các chất có tính chất hoá học tương tự ethylic alcohol là:
H3 - OH, CH3 - CH2 - CH2 - OH,
Bài 23.3 trang 63 Sách bài tập KHTN 9: Thêm một lượng nước cất thích hợp vào cồn 96° sẽ thu được cồn 70° thường được sử dụng trong y tế. Bằng cách trên, từ 3,5 L cồn 96° sẽ thu được lượng cồn 70° là:
A. 5,0 L.
B. 2,55 L.
C. 4,8 L.
D. 7,43 L.
Lời giải:
Đáp án đúng là: C
Thể tích cồn nguyên chất có trong 3,5 L cồn 96o là:
Thể tích cồn 70o thu được từ 3,5 L cồn 96o là:
Bài 23.4 trang 63 Sách bài tập KHTN 9: Trên nhãn của một chai rượu có ghi 700 mL; 40% Alc/Vol có nghĩa là thể tích rượu trong chai là 700 mL và độ rượu là 40°. Số mL ethylic alcohol nguyên chất có trong chai rượu trên là:
A. 280 mL.
B. 400 mL.
C. 420 mL.
D. 700 mL.
Lời giải:
Đáp án đúng là: A
Số mL ethylic alcohol nguyên chất có trong chai rượu trên là:
Bài 23.5 trang 63 Sách bài tập KHTN 9: Có thể bảo quản Na bằng cách ngâm vào chất lỏng nào sau đây: dầu hoả, nước cất, cồn 70°, cồn 96°. Giải thích và viết phương trình hoá học của các phản ứng xảy ra (nếu có) khi cho Na vào các dung dịch trên.
Lời giải:
- Có thể bảo quản Na bằng cách ngâm vào dầu hoả vì nước, cồn đều có phản ứng với Na.
- Phương trình hoá học xảy ra khi cho Na vào nước cất:
2Na + 2H2O → 2NaOH + H2
- Phương trình hoá học xảy ra khi cho Na vào cồn 70°, cồn 96°:
2CH3 - CH2 - OH + 2Na → 2CH3 - CH2 - ONa + H2
2Na + 2H2O → 2NaOH + H2
(do trong dung dịch cồn vẫn có nước)
Bài 23.6 trang 64 Sách bài tập KHTN 9: Hai chất hữu cơ A, B có cùng công thức phân tử C2H6O. Ở điều kiện thường, A là chất khí không tan trong nước, B là chất lỏng tan trong nước theo bất kì tỉ lệ nào. Trong hai chất A, B, chỉ có một chất tác dụng được với Na, chất còn lại không tác dụng. Hãy xác định công thức cấu tạo của A, B.
Lời giải:
Ứng với công thức phân tử C2H6O có hai công thức cấu tạo là CH3 – O – CH3 và CH3 – CH2 – OH. Trong đó, chất có công thức cấu tạo là CH3 – CH2 – OH là ethylic alcohol tan trong nước và tác dụng với Na.
Vậy chất B có công thức cấu tạo là CH3 – CH2 – OH, chất A có công thức cấu tạo là CH3 – O – CH3.
Bài 23.7 trang 64 Sách bài tập KHTN 9: Chọn các chất thích hợp với các chữ cái A, B, D trong các phương trình hoá học sau:
a) A + H2O → B
b) B + 3O2 → 2CO2 + 3H2O
c) B + Na → D + H2
Lời giải:
A: CH2 = CH2
B: CH3 – CH2 – OH
D: C2H5ONa
Hoàn thiện phương trình hoá học:
a) CH2 = CH2 + H2O CH3 – CH2 – OH
b) CH3 – CH2 – OH + 3O2 → 2CO2 + 3H2O
c) 2CH3 – CH2 – OH + 2Na → 2C2H5ONa + H2
Bài 23.8 trang 64 Sách bài tập KHTN 9: Ba chất hữu cơ X, Y, Z có cùng công thức phân tử C3H8O. Biết:
• X, Z là chất lỏng tác dụng được với Na, còn Y là chất khí không tác dụng với Na.
• Trong phân tử X có một nguyên tử C chỉ liên kết trực tiếp với một nguyên tử H. Hãy xác định công thức cấu tạo của X, Y, Z.
Lời giải:
- Với công thức phân tử C3H8O có ba công thức cấu tạo:
CH3 – CH2 – CH2 – OH, CH3 – CH(OH) – CH3 và CH3 – O – CH2 – CH3.
- Hai chất có nhóm –OH đều tác dụng được với Na. Vậy chất Y có công thức cấu tạo: CH3 – O – CH2 – CH3.
Chất X có một nguyên tử C chỉ liên kết với một nguyên tử H, vậy chất X có công thức cấu tạo: CH3 – CH(OH) – CH3.
Chất Z có công thức cấu tạo: CH3 – CH2 – CH2 – OH.
Lý thuyết Ethylic alcohol
I. Cấu tạo phân tử
- Ethylic alcohol có công thức phân tử C2H6O và có công thức cấu tạo: CH3 – CH2 – OH
- Trong phân tử ethylic alcohol có một nguyên tử H không liên kết với nguyên tử C mà liên kết với O tạo thành nhóm – OH
II. Tính chất vật lí
- Ethylic alcohol là chất lỏng, không màu, có mùi đặc trưng, vị cay, tan vô hạn trong nước, hòa tan được nhiều chất như iodine, benzene, xăng,…
- Ethylic alcohol sôi ở 78,3oC và có khối lượng riêng là 0,789 gam/cm3
- Độ cồn là số mililít ethylic alcohol nguyên chất có trong 100ml dung dịch ở 20oC.
III. Tính chất hóa học
1. Phản ứng cháy của ethylic alcohol
Ethylic alcohol cháy với ngọn lửa xanh mờ, tỏa nhiều nhiệt tạo ra CO2 và H2O theo phương trình hóa học:
C2H5OH + 3O2 2CO2 + 3H2O
2. Phản ứng của ethylic alcohol với natri
Ethylic alcohol tác dụng với Na tạo ra H2 theo phương trình hóa học:
2C2H5OH + 2Na 2C2H5ONa + H2
Trong phản ứng trên, nguyên tử H trong nhóm – OH đã được thay thế bởi nguyên tử Na
Nhóm – OH trong phân tử đã tạo ra những tính chất hóa học đặc trưng của ethylic alcohol.
IV. Điều chế ethylic alcohol
1. Điều chế từ tinh bột
Tinh bột glucose ethylic alcohol
2. Điều chế từ C2H4
CH2 = CH2 + HOH CH3 – CH2 – OH
V. Ứng dụng của ethylic alcohol
Ethylic alcohol được ứng dụng trong nhiều lĩnh vực của đời sống và sản xuất.

Sơ đồ tư duy Ethylic alcohol
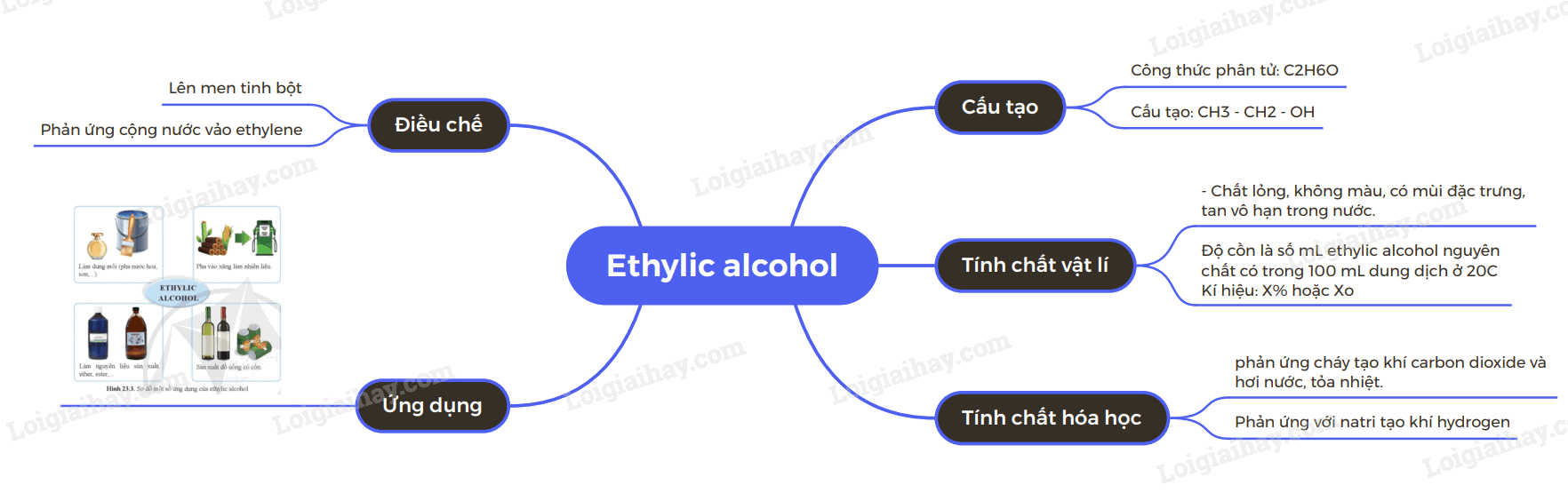
Xem thêm các bài giải SBT Khoa học tự nhiên 9 Cánh diều hay, chi tiết khác: