Với tóm tắt lý thuyết Hóa học lớp 12 Bài 16: Hợp kim – Sự ăn mòn kim loại sách Chân trời sáng tạo hay, chi tiết cùng với 10 bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 12.
Lý thuyết Hóa học 12 Bài 16: Hợp kim – Sự ăn mòn kim loại
A. Lý thuyết Hợp kim – Sự ăn mòn kim loại
1. Hợp kim
- Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim. - Hợp kim có nhiều tính chất cơ học, tính chất vật lí vượt trội so với kim loại, ngày càng được sử dụng phổ biến trong các ngành kinh tế quốc dân
Tính chất của hợp kim
- Hợp kim có nhiều tính chất hóa học tương tự tính chất hóa học của các đơn chất thành phần, tuy nhiên tính chất vật lí và tính chất cơ học của hợp kim khác so với tính chất của các đơn chất thành phần.
Thành phần, tính chất và ứng dụng một số hợp kim quan trọng của sắt và nhôm
- Gang là hợp kim của Fe và C, trong đo C chiếm khoảng 2 – 5% về khối lượng. Trong gang có một lượng nhỏ các nguyên tố khác như: Si, S, Mn, P,…
- Thép là hợp kim của Fe và C, trong đó C chiếm dưới 2% về khối lượng. Trong thép còn có thể có một nguyên tố khác như: Si. Mn, Cr, Ni,…
- Hợp kim của nhôm quan trọng là dural với thành phần chính là Al, Cu và một số nguyên tố khác như Mg, Mn, Fe,… Hợp kim này có nhiều ưu điểm như bền, nhẹ trong không khí và nước nên được sử dụng làm vật liệu chế tạo máy bay, ô tô, tên lửa,…
2. Ăn mòn kim loại
- Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường.
a) Ăn mòn hóa học
Ăn mòn hóa học là quá trình oxi hóa – khử, trong đó các electron của kim loại chuyển trực tiếp đến các chất trong môi trường
b) Ăn mòn điện hóa
Ăn mòn điện hóa là quá trình ăn mòn kim loại do sự tạo thành pin điện hóa
Điều kiện xảy ra sự ăn mòn điện hóa
1. Có hai kim loại khác nhau hoặc kim loại với phi kim,…
2. Tiếp xúc trực tiếp với nhau hoặc gián tiếp qua dây dẫn điện
3. Cùng tiếp xúc với một dung dịch chất điện li
Thiếu một trong ba điều kiện trên sẽ không xảy ra sự ăn mòn điện hóa
3. Chống ăn mòn kim loại
a) Phương pháp phủ bề mặt
Phương pháp bảo vệ bề mặt là phủ lên bề mặt của kim loại một lớp sơn, dầu, mỡ, chất dẻo hoặc tráng, mạ bằng một kim loại khác
b) Phương pháp điện hóa
Trong phương pháp điện hóa, để bảo vệ kim loại, người ta nối kim loại cần bảo vệ với một kim loại hoạt động hóa học mạnh hơn
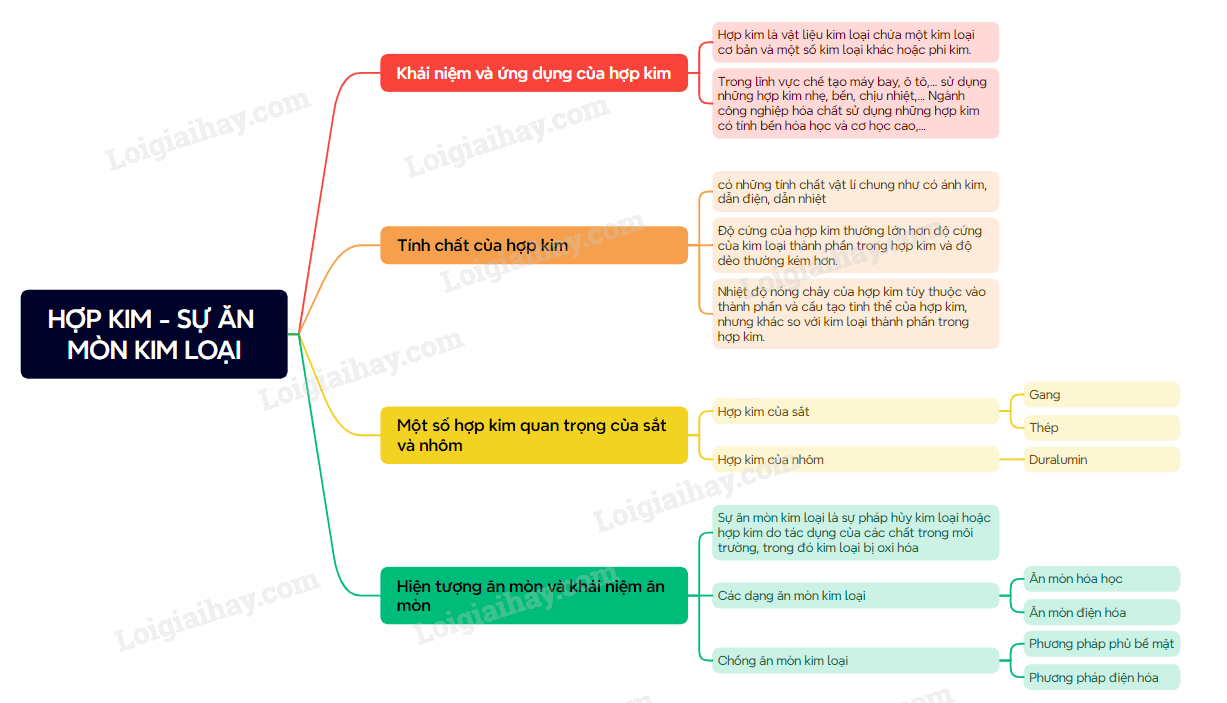
Sơ đồ tư duy Hợp kim - Sự ăn mòn kim loại
B. Trắc nghiệm Hợp kim – Sự ăn mòn kim loại
Câu 1. Trong hiện tượng ăn mòn kim loại xảy ra quá trình nào sau đây?
A. Quá trình oxi hoá kim loại.
B. Quá trình khử kim loại.
C. Quá trình điện phân.
D. Sự mài mòn kim loại.
Đáp án đúng là: A
Trong hiện tượng ăn mòn kim loại xảy ra quá trình oxi hóa kim loại.
Câu 2. Đinh sắt bị ăn mòn khi gắn với kim loại nào sau đây?
A. Magnesium.
B. Nhôm.
C. Kẽm.
D. Đồng.
Đáp án đúng là: D
Fe là kim loại mạnh hơn Cu nên khi gắn với Cu, Fe sẽ bị ăn mòn trước.
Câu 3. Trường hợp nào sau đây kim loại bị ăn mòn điện hoá học?
A. Đốt dây sắt trong khí oxygen khô.
B. Thép carbon để trong không khí ẩm.
C. Kim loại kẽm trong dung dịch HCl.
D. Kim loại sắt trong dung dịch HNO3 loãng.
Đáp án đúng là: B
Thép carbon để trong không khí ẩm thỏa mãn 3 điều kiện của ăn mòn điện hóa.
Câu 4. Khi một vật bằng sắt tây (sát tráng thiếc) bị xây sát sâu tới lớp sắt bên trong để lâu trong không khí ẩm sẽ xảy ra quá trinh nào sau đây?
A. Sn bị ăn mòn điện hoá.
B. Fe bị ăn mòn điện hoá.
C. Fe bị ăn mòn hoá học.
D. Sn bị ăn mòn hoá học.
Đáp án đúng là: B
Sắt mạnh hơn thiếc nên sẽ bị ăn mòn điện hoá.
Câu 5. Phương pháp nào sau đây không dùng để bảo vệ vật làm sắt thép khỏi bị ăn mòn?
A. Gắn thêm kẽm.
B. Gắn thêm magnesium.
C. Gắn thêm chì.
D. Phủ sơn hoặc dầu mỡ.
Đáp án đúng là: C
Sắt mạnh hơn chì nên gắn thêm chì thì sắt mạnh hơn vẫn bị ăn mòn trước.
Câu 6: Hợp kim là
A. một kim loại tinh khiết.
B. hỗn hợp các kim loại có thành phần tùy ý.
C. hỗn hợp của kim loại nền với kim loại khác hoặc phi kim, có thành phần xác định.
D. hỗn hợp hai phi kim.
Đáp án đúng là: C
Hợp kim là hỗn hợp của kim loại nền với kim loại khác hoặc phi kim, có thành phần xác định.
Câu 7. Đồng thau là một hợp kim của
A. đồng và thiếc.
B. đồng và nickel.
C. đồng và aluminium.
D. đồng và kẽm.
Đáp án đúng là: D
Đồng thau là hợp kim của đồng và kẽm.
Câu 8. Khi chế tạo thép từ gang, có thể làm giảm tỉ lệ phần trăm carbon trong gang bằng cách nào sau đây?
A. Sử dụng oxygen để đốt cháy carbon trong gang nóng chảy.
B. Lọc carbon ra khỏi gang.
C. Hoà tan carbon trong dung dịch sulfuric acid.
D. Cạo carbon ra khỏi bề mặt kim loại.
Đáp án đúng là: A
Khi chế tạo thép từ gang, có thể làm giảm tỉ lệ phần trăm carbon trong gang bằng cách sử dụng oxygen để đốt cháy carbon trong gang nóng chảy.
Câu 9. Hiện tượng nào sau đây không phải là hiện tượng ăn mòn kim loại?
A. Ống thép bị gỉ sắt màu nâu đỏ.
B. Vòng bạc bị xỉn màu.
C. Công trình bằng đá bị ăn mòn bởi mưa acid.
D. Chuông đồng bị gỉ đồng màu xanh.
Đáp án đúng là: C
Công trình bằng đá không phải kim loại.
Câu 10. Phát biểu về hiện tượng ăn mòn kim loại nào sau đây đúng?
A. Khi kim loại bị ăn mòn, các đặc tính hữu ích của kim loại như tính dẻo, dễ dát mỏng, dễ kéo sợi và tính dẫn điện bị suy giảm.
B. Khi kim loại bị ăn mòn, các đặc tính hữu ích của kim loại như tính dẻo, dễ dát mỏng, dễ kéo sợi và tính dẫn điện không bị ảnh hưởng.
C. Khi kim loại bị ăn mòn, các đặc tính hữu ích của kim loại như tính dẻo, dễ dát mỏng, dễ kéo sợi và tính dẫn điện được tăng cường.
D. Khi kim loại bị ăn mòn, các kim loại không phản ứng với dung dịch acid.
Đáp án đúng là: A
Khi kim loại bị ăn mòn, các đặc tính hữu ích của kim loại như tính dẻo, dễ dát mỏng, dễ kéo sợi và tính dẫn điện bị suy giảm.
Câu 11: Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim dưới tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hóa.
|
Phát biểu |
Đúng |
Sai |
|
a. Trong quá trình ăn mòn, kim loại bị oxi hoá thành ion của nó. |
||
|
b. Ngâm một lá nhôm trong dung dịch NaOH, xảy ra hiện tượng ăn mòn hóa học. |
||
|
c. Bôi dầu mỡ, sơn, mạ, tráng men lên bề mặt vật dụng bằng kim loại để chống sự ăn mòn kim loại. |
||
|
d. Sự ăn mòn vỏ tàu trong nước biển là ăn mòn hóa học. |
a – Đúng.
b – Đúng.
c – Đúng.
d – Sai. Vì sự ăn mòn vỏ tàu trong nước biển là ăn mòn điện hóa học
Câu 12: Ăn mòn kim loại xảy ra phổ biến và gây thiệt hại về mặt kinh tế, nhất là ăn mòn thép tạo gỉ sắt. Khoảng 25% thép được sản xuất tại Mỹ chỉ để thay thế thép bị ăn mòn khi sử dụng.
|
Phát biểu |
Đúng |
Sai |
|
a. Một miếng vỏ đồ hộp làm bằng sắt tây (sắt tráng thiếc) bị xây xát bên trong, để trong không khí ẩm thì thiếc sẽ bị ăn mòn trước. |
||
|
b. Ngâm một lá nhôm trong dung dịch NaOH loãng, xảy ra hiện tượng ăn mòn hóa học. |
||
|
c. Để chống sự ăn mòn sắt, người ta tráng thiếc, kẽm lên sắt. |
||
|
d. Gỉ sắt có thành phần chủ yếu là Fe2O3.nH2O. |
a – Sai. Vì sắt mạnh hơn nên sắt sẽ bị ăn mòn trước
b – Đúng.
c – Đúng.
d – Đúng.
Câu 13: Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim dưới tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hóa.
Cho các phát biểu sau:
a. Về bản chất, ăn mòn hoá học cũng là một dạng của ăn mòn điện hoá.
b. Nối thanh kẽm với vỏ tàu biển bằng thép thì vỏ tàu được bảo vệ.
c. Vàng (Au) là kim loại dẻo nhất.
d. Trong một chu kì, kim loại có độ âm điện bé hơn phi kim.
Số phát biểu đúng là?
Đáp án đúng là: 3
Giải thích:
Các phát biểu b, c, d đúng.
Phát biểu a sai. Vìvề bản chất, ăn mòn hoá học không phải là một dạng của ăn mòn điện hoá.
Câu 14. Cho các thí nghiệm sau:
(1). Đốt cháy dây sắt trong không khí khô.
(2). Cho hợp kim Fe – Cu vào dung dịch CuSO4.
(3). Đặt mẫu gang lâu ngày trong không khí ẩm.
(4). Cho kim loại Fe vào dung dịch AgNO3.
Số thí nghiệmkhông xảy ra ăn mòn điện hoá là?
Đáp án đúng là: 1
Giải thích:
Đốt cháy dây sắt trong không khí khô xảy ra ăn mòn hóa học.
Câu 15. Để các hợp kim: Fe – Cu; Fe – C; Zn – Fe; Mg – Fe lâu ngày trong không khí ẩm. Số hợp kim mà trong đó Fe bị ăn mòn điện hoá là?
Đáp án đúng là: 2
Giải thích:
Fe bị ăn mòn điện hóa học trong các hợp kim Fe – Cu, Fe – C..
Xem thêm các bài tóm tắt lý thuyết Hóa học lớp 12 Chân trời sáng tạo hay, chi tiết khác: