Lời giải bài tập Hóa học lớp 12 Bài 19: Tính chất vật lí và tính chất hoá học của kim loại sách Kết nối tri thức hay, chi tiết sẽ giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập môn Hóa học 12. Mời các bạn đón xem:
Giải bài tập Hóa học 12 Bài 19: Tính chất vật lí và tính chất hoá học của kim loại
Lời giải:
- Nhờ tính dẫn điện tốt mà kim loại được sử dụng làm dây dẫn điện; nhờ tính dẫn nhiệt tốt mà kim loại được dùng để chế tạo dụng cụ đun nấu; nhờ tính cứng và bền mà kim loại được dùng trong các công trình xây dựng.
- Kim loại có các tính chất hoá học đặc trưng: tác dụng với phi kim, tác dụng với nước, tác dụng với dung dịch acid, tác dụng với dung dịch muối.
Câu hỏi 1 trang 90 Hóa học 12: Vì sao kim loại có tính dẻo?
Lời giải:
Kim loại có tính dẻo do các ion dương trong mạng tinh thể kim loại có thể trượt lên nhau mà không tách rời nhau nhờ lực hút tĩnh điện giữa chúng với các electron hoá trị tự do.
b) Vì sao kim loại có tính dẫn điện, trong khi hầu hết các phi kim không dẫn điện?
Lời giải:
a) Sự khác biệt giữa liên kết kim loại và liên kết cộng hoá trị:
- Liên kết kim loại: sự dùng chung electron giữa các nguyên tử kim loại.
- Liên kết cộng hoá trị: sự dùng chung electron giữa hai nguyên tử tham gia liên kết.
b) Khi một hiệu điện thế được áp vào thanh kim loại, các electron tự do trong mạng tinh thể sẽ di chuyển thành dòng từ phía cực âm về cực dương. Hệ quả là thanh kim loại trở thành vật dẫn điện.
Lời giải:
Tính dẫn nhiệt của các kim loại được giải thích bằng sự có mặt của các electron tự do trong mạng tinh thể. Khi đốt nóng một đầu của thanh kim loại thì động năng của các electron trong vùng đó tăng lên. Các electron này truyền động năng của chúng cho các ion dương ở nút mạng và các electron khác trong toàn thanh kim loại thông qua va chạm, làm cho nhiệt được lan truyền trong toàn bộ thanh kim loại.
Một số ứng dụng của kim loại dựa trên tính dẫn nhiệt của chúng: chế tạo dụng cụ đun nấu, chế tạo bộ phận tản nhiệt trong các thiết bị …
Lời giải:
Các electron tự do trong tinh thể kim loại phản xạ hầu hết những tia sáng nhìn thấy được, do đó kim loại có vẻ sáng lấp lánh, gọi là ánh kim.
Nhờ tính ánh kim mà kim loại được dùng để chế tạo trang sức, đồ vật trang trí …
Lời giải:
- Do có nhiệt độ nóng chảy cao, tungsten (vonfram) được sử dụng làm dây tóc bóng đèn trong bóng đèn sợi đốt.
- Vì rất cứng nên chromium là kim loại được mạ bên ngoài các sản phẩm để bảo vệ sản phẩm và hạn chế sự mài mòn.
Hoạt động thí nghiệm trang 91 Hóa học 12: Kim loại tác dụng với phi kim
Chuẩn bị:
Hoá chất: dây magnesium (Mg), nhôm bột, lưu huỳnh bột.
Dụng cụ: kẹp sắt, ống nghiệm chịu nhiệt, đũa thuỷ tinh, đèn cồn.
Tiến hành:
1. Magnesium tác dụng với oxygen. Dùng kẹp sắt kẹp một mẩu dây magnesium (Mg) và đốt trên ngọn lửa đèn cồn.
2. Nhôm tác dụng với lưu huỳnh: Trộn đều bột nhôm và bột lưu huỳnh theo tỉ lệ khối lượng tương ứng khoảng 1 : 2. Lấy một thìa thuỷ tinh (khoảng 0,3 g) hỗn hợp vào ống nghiệm khô chịu nhiệt. Hơ nóng đều ống nghiệm trên ngọn lửa đèn cồn, sau đó đun tập trung vào phần ống nghiệm chứa hỗn hợp.
Thực hiện yêu cầu sau:
Hãy mô tả hiện tượng quan sát được và viết phương trình hoá học của các phản ứng xảy ra.
Lời giải:
|
Thí nghiệm |
Hiện tượng |
Phương trình hoá học |
|
Magnesium tác dụng với oxygen |
Sợi dây magnesium cháy mãnh liệt cho ngọn lửa sáng chói. |
2Mg + O2 2MgO |
|
Nhôm tác dụng với lưu huỳnh |
Hỗn hợp cháy sáng, phản ứng toả nhiều nhiệt. |
2Al + 3S Al2S3 |
Lời giải:
Khi tác dụng với phi kim, kim loại thể hiện tính khử.
Ví dụ:
Lời giải:
Những kim loại có thế điện cực chuẩn nhỏ hơn -0,414 có thể đẩy được hydrogen ra khỏi nước.
Quan sát Bảng 15.1 xác định được: Li, K, Ba, Ca, Na, Mg, Al, Zn, Cr, Fe có thể phản ứng với nước ở nhiệt độ thường giải phóng khí hydrogen.
Tuy nhiên chỉ có các kim loại Li, K, Ba, Ca, Na phản ứng nhanh với nước ở điều kiện thường, các kim loại còn lại phản ứng rất chậm hoặc gần như không xảy ra.
Hoạt động thí nghiệm trang 92 Hóa học 12: Kim loại tác dụng với dung dịch acid loãng
Chuẩn bị:
Hoá chất: dung dịch H2SO4 10%, kẽm hạt.
Dụng cụ: ống nghiệm, kẹp gỗ.
Tiến hành:
Cho vài hạt kẽm vào ống nghiệm. Thêm tiếp khoảng 2 mL dung dịch H2SO4 10%.
Thực hiện yêu cầu sau:
Hãy mô tả hiện tượng quan sát được và viết phương trình hoá học.
Lời giải:
Hiện tượng: Hạt kẽm tan dần, có khí thoát ra.
Phương trình hoá học:
Zn(s) + H2SO4(aq) → ZnSO4(aq) + H2(g)
Lời giải:
Ta có:
Nhận thấy thế điện cực chuẩn của các cặp oxi hóa – khử này lớn hơn rất nhiều so với thế điện cực chuẩn của hydrogen nên các kim loại từ Cu đến Au trong dãy điện hóa không đẩy được H2 ra khỏi dung dịch của các acid như HCl, H2SO4 loãng.
Hoạt động thí nghiệm trang 93 Hóa học 12: Kim loại tác dụng với dung dịch muối
Chuẩn bị:
Hoá chất: đinh sắt mới (đã rửa sạch lớp dầu mỡ), dung dịch CuSO4 1 M.
Dụng cụ: cốc thuỷ tinh, kẹp sắt.
Tiến hành:
Cho đinh sắt vào cốc. Thêm tiếp 2 - 3 ml dung dịch CuSO4 1M.
Sau 5 phút dùng kẹp lấy đinh sắt ra khỏi dung dịch.
Thực hiện yêu cầu sau:
Mô tả hiện tượng xảy ra, giải thích và viết phương trình hoá học.
Lời giải:
Hiện tượng: Dung dịch nhạt màu dần, có lớp kim loại màu đỏ đồng bám ngoài đinh sắt.
Giải thích: Kim loại sắt hoạt động hoá học mạnh hơn kim loại đồng nên có thể đẩy được đồng ra khỏi dung dịch muối của nó.
Phương trình hoá học: Fe + CuSO4 → FeSO4 + Cu.
- Giải thích được vì sao các vật bằng sắt thép bị phá huỷ nhanh hơn trong môi trường acid loãng, còn vật bằng đồng thì khó bị phá huỷ hơn.
Lời giải:
- Nhờ tính dẫn điện tốt kim loại được sử dụng làm dây dẫn điện; nhờ tính dẫn nhiệt tốt mà kim loại được dùng để chế tạo dụng cụ đun nấu; nhờ tính ánh kim mà kim loại được sử dụng để làm đồ trang sức, nhờ tính cứng và bền mà kim loại được dùng trong các công trình xây dựng…
- Sắt hoạt động hoá học mạnh hơn đồng; ngoài ra, sắt tác dụng được với dung dịch acid như HCl, H2SO4 loãng… ở điều kiện thường còn đồng thì không, do đó các vật bằng sắt thép bị phá huỷ nhanh hơn trong môi trường acid loãng, còn vật bằng đồng thì khó bị phá huỷ hơn.
Lý thuyết Tính chất vật lí và tính chất hoá học của kim loại
I. Tính chất vật lí
1. Tính dẻo
Kim loại có tính dẻo: dễ rèn, dễ dát mỏng và dễ kéo sợi. Nhờ có tính dẻo mà kim loại có thể được uốn cong, ép khuôn thành nhiều hình dạng và kích thước khác nhau.
2. Tính dẫn điện
Tất cả các kim loại đều có tính dẫn điện.
3. Tính dẫn nhiệt
Tính dẫn nhiệt của các kim loại cũng được giải thích bằng sự có mặt của các electron tự do trong mạng tinh thể. Các kim loại dẫn điện tốt thường dẫn nhiệt tốt. Do có tính dẫn nhiệt tốt, các kim loại hoặc hợp kim được sử dụng làm các dụng cụ đun nấu như xoong, nồi, chảo,…
4. Tính ánh kim
Các elctron tự do trong tinh thể kim loại phản xạ hầu hết những tia sáng nhìn thấy được. Do đó, kim loại có vẻ sáng lấp lánh, gọi là ánh kim
5. Một số tính chất vật lí khác của kim loại
a) Khối lượng riêng
Khối lượng riêng của các kim loại rất khác nhau. Kim loại nhẹ nhất là lithium, kim loại nặng nhất là osium. Kim loại có D < 5g/cm3, được gọi là kim loại nhẹ, những kim loại có D > 5g/cm3, được gọi là kim loại nặng.
b) Nhiệt độ nóng chảy
Nhiệt độ nóng chảy của các kim loại biến đổi trong khoảng rộng: có kim loại nóng chảy ở nhiệt độ rất cao như tungsten (W), kim loại duy ở trạng thái lỏng trong điều kiện thường là thủy ngân.
c) Tính cứng
Các kim loại có độ cứng rất khác nhau. Kim loại cứng nhất là Cr, có thể cắt được kính, các kim loại mềm nhất là kim loại kiềm như potassium, rubidium, sodium.
II. Tính chất hóa học
1. Tác dụng với phi kim
a) Tác dụng với oxygen
Hầu hết các kim loại (trừ vàng, bạc, platinum,…) đều tác dụng với oxygen tạo thành oxide.
Ví dụ:
b) Tác dụng với chlorine
Hầu hết các kim loại đều tác dụng với khí chlorine khi đun nóng, thu được muối chloride tương ứng.
Ví dụ: 2Fe(s) + 3Cl2(g) 2FeCl3 (s)
c) Tác dụng với lưu huỳnh
Nhiều kim loại có thể khử lưu huỳnh khi đun nóng (trừ thủy ngân phản ứng ngay ở nhiệt độ thường)
Ví dụ:
2. Tác dụng với nước
Hầu hết các kim loại nhóm IA, IIA có tính khử mạnh, tác dụng với nước ở nhiệt độ thường giải phóng H2.
Ví dụ: 2Na(s) + H2O(l) 2NaOH(aq) + H2(g)
Những kim loại có thế điện cực chuẩn
3. Tác dụng với dung dịch acid
a) Với dung dịch HCl, H2SO4 loãng
Ở điều kiện chuẩn, những kim loại có có thể tác dụng với các dung dịch acid như HCl, H2SO4 tạo thành H2
Ví dụ: Zn(s) + 2H+(aq) Zn2+ (aq) + H2(g)
b) Với dung dịch H2SO4 đặc
Hầu hết các kim loại (trừ Au và Pt) phản ứng được với dung dịch sulfuric acid đặc. Phản ứng này thường tạo thành muối sulfate, nước và sulfur dioxide. Phản ứng diễn ra mạnh hơn khi hỗn hợp phản ứng được đun nóng
Ví dụ: Cu(s) + 2H2SO4 (aq) đặcCuSO4(aq) + SO2(g) + 2H2O(l)
4. Tác dụng với dung dịch muối
Kim loại hoạt động mạnh hơn có thể đẩy kim loại hoạt động yếu hơn ra khỏi dung dịch muối của nó.
Ví dụ: Zn(s) + CuSO4(aq) ZnSO4(aq) + Cu(s)
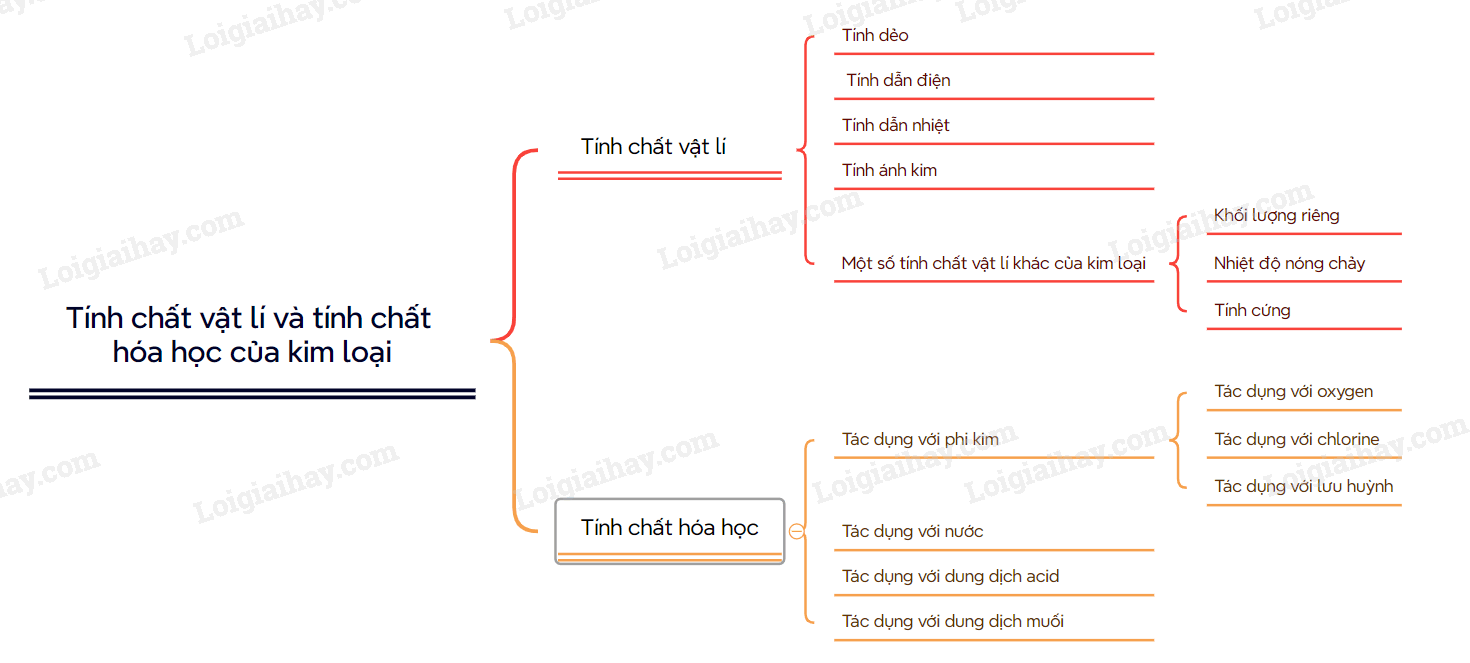
Sơ đồ tư duy Tính chất vật lí và tính chất hoá học của kim loại
Xem thêm các bài giải bài tập Hóa Học lớp 12 Kết nối tri thức hay, chi tiết khác:
Bài 18. Cấu tạo và liên kết trong tinh thể kim loại
Bài 19. Tính chất vật lí và tính chất hoá học của kim loại
Bài 20. Kim loại trong tự nhiên và phương pháp tách kim loại