Tailieumoi.vn giới thiệu giải bài tập Chuyên đề Hóa học 10 Bài 10: Thực hành thí nghiệm hóa học ảo sách Kết nối tri thức hay, chi tiết giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập Chuyên đề học tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Chuyên đề Hóa học 10 Bài 10: Thực hành thí nghiệm hóa học ảo
Giải Chuyên đề Hóa học 10 trang 60
Lời giải:
Để thực hiện các thí nghiệm hóa học ảo trên máy tính ta có thể sử dụng phần mềm mô phỏng thí nghiệm ảo như Portable Virtual Chemistry Lab hay ChemLab, Yenka, …
Yenka là tập hợp các phòng thí nghiệm ảo, trong đó có phòng thí nghiệm hóa học với các hóa chất, dụng cụ phổ biến để thực hiện các thí nghiệm hóa học vô cơ và điện hóa. Yenka mô phỏng các thí nghiệm ảo dễ dàng, nhanh chóng và hiệu quả. Có thể sử dụng Yenka để tiến hành một số thí nghiệm với những chất độc hại hay những thí nghiệm không an toàn.
Giải Chuyên đề Hóa học 10 trang 62
Lời giải:
Từ đồ thị ta thấy, sau 20s thì thể tích khí thoát ra là 86,5 cm3.
⇒ Tốc độ trung bình của phản 1) trong khoảng thời gian từ 0 đến 20 giây theo thể tích CO2 là: cm3/s
Lời giải:
- Quả bóng bay ở ống nghiệm chứa dung dịch acid 2M to dần lên nhanh nhất và nổ sớm nhất. Chứng tỏ tốc độ thoát khí CO2 ở ống nghiệm có nồng độ acid 2M là nhanh nhất.
- Quả bóng bay ở ống nghiệm chứa dung dịch acid 1M to lên chậm nhất và nổ muộn nhất. Chứng tỏ tốc độ thoát khí CO2 ở ống nghiệm có nồng độ acid 1M là chậm nhất.
⇒ Nồng độ của các chất tham gia càng lớn thì tốc độ phản ứng càng lớn.
Giải Chuyên đề Hóa học 10 trang 63
Câu hỏi 3 trang 63 Chuyên đề Hóa 10: Sử dụng thẻ Open-local để mô phỏng các thí nghiệm sau:
- Thí nghiệm ảnh hưởng của nhiệt độ đến tốc độ của phản ứng (giữa CaCO3(s) và HCl(aq)).
- Thí nghiệm ảnh hưởng của chất xúc tác MnO2 đến tốc độ phản ứng phân hủy H2O2(aq).
Lời giải:
- Thí nghiệm ảnh hưởng của nhiệt độ đến tốc độ của phản ứng (giữa CaCO3(s) và HCl(aq)).
Bước 1: Khởi động phần mềm Yenka.
Bước 2: Chọn Open - local ⟶ Temperature and rate
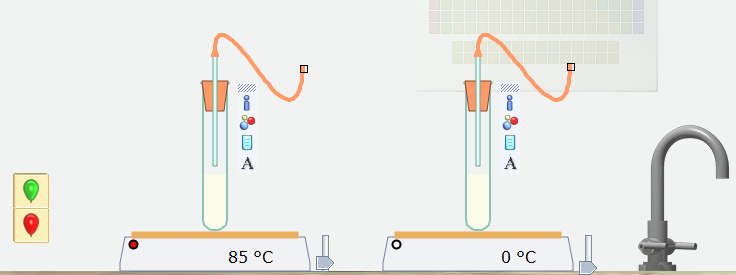
Bước 3: Nháy chuột vào các quả bóng có màu khác nhau, kéo thả vào cuối ống dẫn khí ở các ống nghiệm có nồng độ khác nhau.
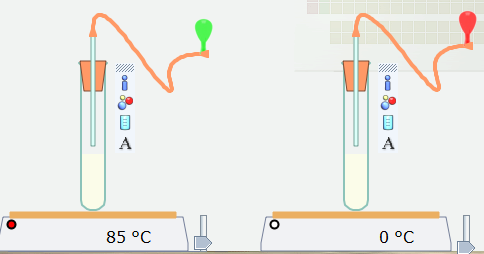
Bước 4. Nháy chuột vào nút Pause để thực hiện mô phỏng. Sau khoảng 6 giây nháy chuột lại vào nút Pause để dừng mô phỏng.
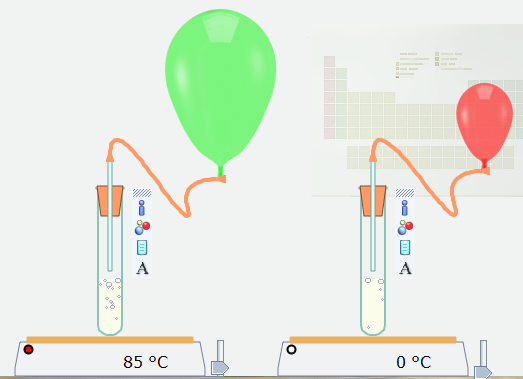
Kết quả:
Phương trình hóa học của phản ứng:
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + CO2(g) + H2O(l)
Quả bóng ở ống nghiệm được đun nóng đến 85oC to lên nhanh hơn. Chứng tỏ nhiệt độ càng cao thì tốc độ phản ứng càng lớn.
- Thí nghiệm ảnh hưởng của chất xúc tác MnO2 đến tốc độ phản ứng phân hủy H2O2(aq).
Bước 1: Khởi động phần mềm Yenka.
Bước 2: Chọn Open -local ⟶ Catalysts and rate.
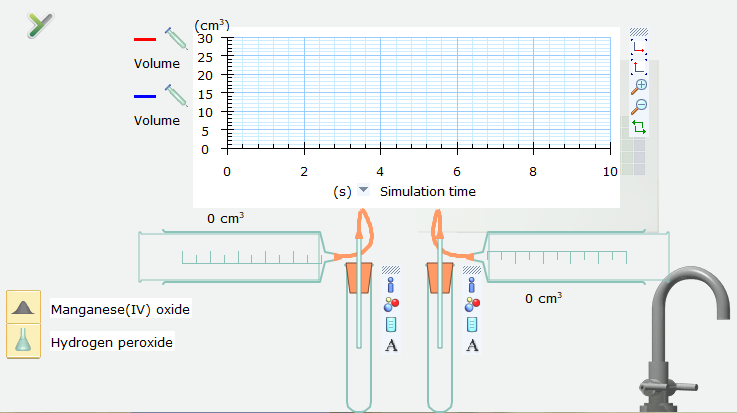
Bước 3: Nháy chuột trái vào dòng chữ chỉ hóa chất Hydrogen peroxide rồi kéo thả lần lượt vào 2 ống nghiệm (Test tube), sau đó kéo thả hoá chất Manganeses(IV) oxide vào 1 trong 2 ống nghiệm.
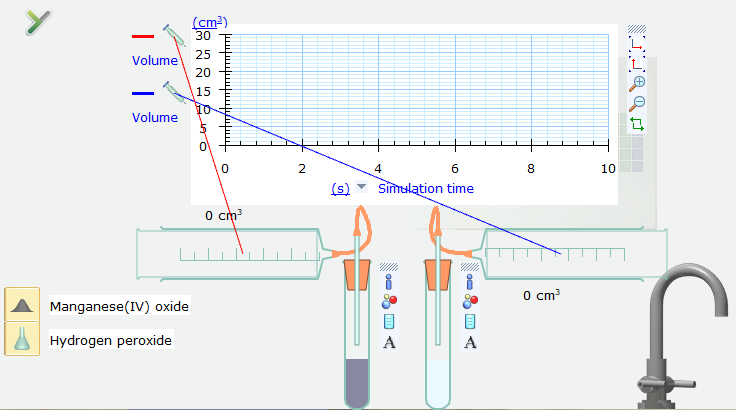
Bước 4. Nháy chuột vào nút Pause ở góc dưới bên phải của màn hình mô phỏng để thực hiện mô phỏng. Sau khoảng 1 giây trên trục thời gian mô phỏng, nháy chuột lại vào nút Pause để dừng mô phỏng.
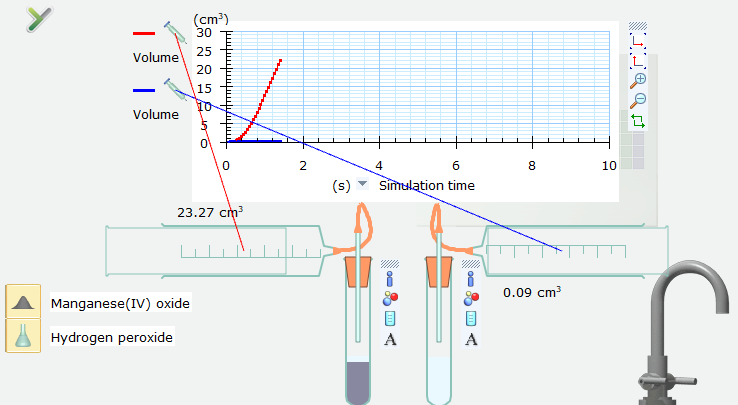
Kết quả cho thấy có khí thoát ra ngay ở ống nghiệm chứa xúc tác manganeses(IV) oxide. Còn ống nghiệm không có xúc tác manganeses(IV) oxide chưa có khí thoát ra. Chứng tỏ chất xúc tác làm tăng tốc độ phản ứng.
Giải Chuyên đề Hóa học 10 trang 66
Lời giải:
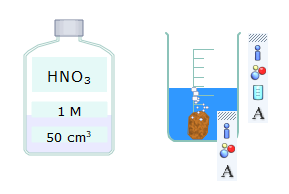
Mô phỏng phản ứng
Hiện tượng: Có khí thoát ra và dung dịch có màu xanh.
Phương trình hóa học: 8HNO3 + 3Cu ⟶ 3Cu(NO3)2 + 2NO + 4H2O
Lời giải:
|
|
Thí nghiệm thật |
Thí nghiệm ảo |
|
Khái niệm |
Là các thí nghiệm được thực hiện bằng các dụng cụ thí nghiệm thật, các hoá chất thật.
|
Là các thí nghiệm được thực hiện trên máy vi tính, thí nghiệm ảo thực chất là mô hình của thí nghiệm thật trên máy vi tính.
|
|
Ưu điểm |
Cả hai đều là thí nghiệm trực quan, cùng làm sáng tỏ lý thuyết, gây hứng thú học tập cho học sinh, giáo dục tính tò mò khoa học, làm cho học sinh nhận thức dễ dàng hơn, kiến thức thu được của các em rõ ràng và sâu sắc, đồng thời lớp học sôi nổi, hào hứng, …
|
|
|
|
Trực quan hơn, học sinh có thể quan sát trực tiếp, gây nên tính tò mò, hứng thú cho học sinh. Rèn kĩ năng thao tác thí nghiệm. Thúc đẩy tinh thần yêu khoa học. |
Dễ dàng quan sát thí nghiệm trên màn hình chiếu; không cần chuẩn bị dụng cụ, hóa chất; thí nghiệm ảo luôn thành công; an toàn với các hóa chất độc hại hoặc cháy nổ. |
|
Nhược điểm |
- Hầu như các dụng cụ thí nghiệm đều nhỏ, lớp học đông, phòng học rộng. ⇒ Khi làm thí nghiệm thì không phải tất cả các học sinh trong lớp đều có thể quan sát dễ dàng được. - Không phải thí nghiệm hóa học thật nào cũng tiến hành thành công. - Mất thời gian và công sức để chuẩn bị dụng cụ, hóa chất thí nghiệm. - Đôi khi trong quá trình thí nghiệm sẽ xảy ra vấn đề ngoài ý muốn như cháy nổ, nhiễm hóa chất độc hại, bỏng, … |
- Giáo viên và học sinh không cần tiến hành thí nghiệm nên dẫn đến kĩ năng thao tác thí nghiệm kém. - Khó khăn khi sử dụng chưa thành thạo máy tính và công nghệ thông tin.
|