Với lời giải SBT Hóa học 11 trang 80 chi tiết trong Bài 16: Alcohol sách Chân trời sáng tạo giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 16: Alcohol
Bài 16.20 trang 80 Sách bài tập Hóa học 11: Diethyl ether là hợp chất hữu cơ có công thức C2H5OC2H5 (viết tắt là Et2O) thường được sử dụng làm dung môi không proton phổ biến trong phòng thí nghiệm, dung môi đặc biệt quan trọng trong sản xuất nhựa cellulose như cellulose acetate. Et2O có chỉ số cetane (đại lượng quy ước cho khả năng tự bốc cháy của nhiên liệu, có trị số từ 0 - 100) cao, khoảng 85 - 96, làm chất kích nổ cho một số động cơ; Et2O kết hợp với các sản phẩm chưng cất dầu mỏ như xăng, dầu diesel, giúp khởi động lại động cơ ở nhiệt độ dưới 0°C.
Et2O được sản xuất bằng phương pháp loại nước ở thể hơi ethyl alcohol với xúc tác alumina (Al2O3), hiệu suất lên đến 95%. Et2O cũng được điều chế trong phòng thí nghiệm và quy mô công nghiệp bằng hỗn hợp ethyl alcohol và sulfuric acid đặc, phản ứng thực hiện ở nhiệt độ thấp hơn 150 °C để tránh tạo ra ethylene.
Theo tính toán lí thuyết, để sản xuất 1 tấn diethyl ether, cần khối lượng ethyl alcohol tối thiểu là bao nhiêu?
Lời giải:
Phương trình hoá học của phản ứng:
2C2H5OH C2H5OC2H5 + H2O
Số mol của diethyl ether :
Khối lượng ethyl alcohol tối thiểu cần dùng là:
(tấn) = 1 309 (kg)
Bài 16.21 trang 80 Sách bài tập Hóa học 11: Hoá chất gây tác hại đến sức khoẻ con người và động vật. Các hoá chất khác nhau gây độc tính trên các bộ phận sẽ khác nhau, ví dụ, 2 gam chất (A) gây tổn thương cho gan, nhưng không hẳn 2 gam chất (A) sẽ gây tổn thương cho thận. Để so sánh độc tính giữa các hoá chất, người ta thực hiện thử nghiệm LD50. LD50 (Lethal Dose, 50%) là liều lượng hoá chất phơi nhiễm trong cùng một thời điểm, gây tử vong cho 50% cá thể của nhóm thử nghiệm. LD50 của ethanol đối với người trưởng thành trong khoảng 5 gam - 8 gam trên 1 kg trọng lượng cơ thể. Trung bình, một người trưởng thành nặng 60 kg, khi sử dụng đồ uống có cồn, lượng ethanol có thể gây ra tình trạng nguy kịch cho sức khoẻ là bao nhiêu?
Lời giải:
LD50 của ethanol đối với người trưởng thành trong khoảng 5 gam - 8 gam trên 1 kg trọng lượng cơ thể. Lượng ethanol trung bình có thể gây tử vong cho 50% đối tượng là người trưởng thành nặng 60 kg khoảng:
5×60 = 300 (g).
Lưu ý: Đây là lượng ethanol có thể gây nguy kịch trung bình cho 50% đối tượng, có nghĩa là sẽ có lượng ethanol gây tử vong cho 1% - 100% (LD1 – LD100).
Bài 16.22 trang 80 Sách bài tập Hóa học 11: Cho các liên kết và giá trị năng lượng liên kết (Eb) của một số liên kết cộng hoá trị như sau:
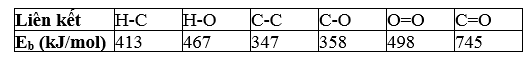
a) Tính biến thiên enthalpy chuẩn của phản ứng đốt cháy hơi ethanol.
b) Khi đốt cháy cùng số mol ethanol và methanol, nhiệt năng của phản ứng nào tạo ra nhiều hơn?
Lời giải:
a) Phương trình hoá học của phản ứng đốt cháy hơi ethanol:
C2H5OH(g) + 3O2(g) →2CO2(g) + 3H2O(g)
Công thức tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết như sau:
= 5×Eb(C-H) + Eb(C-C) + Eb(C-O) + Eb(O-H) + 3×Eb(O=O) - 2×2×Eb(C=O) - 3×2×Eb(O-H)
= 5×413+ 347+ 358+ 467+ 3×498-4×745-6×467 = -1 051 (kJ).
b) Phương trình hoá học của phản ứng đốt cháy hơi methanol:
CH3OH(g) + O2(g) →CO2(g) + 2H2O(g)
Công thức tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết như sau :
ArH°298 = 3×Eb(C-H) + Eb(C-O) + Eb(O-H) + 1,5×Eb(O=O) - 2×Eb(C=O) - 4×Eb(O-H)
= 3×413 + 358 + 467+ 1,5×498 - 2×745 - 4×467 = -547 (kJ).
Vậy khi đốt cháy cùng số mol methanol và ethanol thì ethanol giải phóng nhiệt năng lớn hơn.
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 16.1 trang 75 Sách bài tập Hóa học 11: Alcohol no, đơn chức, mạch hở có công thức chung là...
Bài 16.2 trang 75 Sách bài tập Hóa học 11: Hợp chất thuộc loại polyalcohol là...
Bài 16.3 trang 75 Sách bài tập Hóa học 11: Saccharose là một loại đường phổ biến, sản xuất chủ yếu từ cây mía. Saccharose có cấu trúc phân tử:..
Bài 16.4 trang 76 Sách bài tập Hóa học 11: Ethyl alcohol có công thức cấu tạo là..
Bài 16.5 trang 76 Sách bài tập Hóa học 11: Tên của alcohol có công thức cấu tạo:...
Bài 16.6 trang 76 Sách bài tập Hóa học 11: Trong các alcohol sau, alcohol nào có nhiệt.. độ sôi cao nhất?...
Bài 16.7 trang 76 Sách bài tập Hóa học 11: Methyl alcohol, ethyl alcohol tan vô hạn trong nước là do...
Bài 16.8 trang 76 Sách bài tập Hóa học 11: Alcohol có phản ứng đặc trưng với Cu(OH)2 là..
Bài 16.9 trang 76 Sách bài tập Hóa học 11: Nhóm chức alcohol không bị phá vỡ bởi tác nhân nào?..
Bài 16.10 trang 77 Sách bài tập Hóa học 11: Alcohol bị oxi hoá bởi CuO, t° tạo thành ketone là.....
Bài 16.11 trang 77 Sách bài tập Hóa học 11: Theo Nghị định 100/2019/NĐ-CP của Chính phủ quy định, nồng độ cồn trong 1 L hơi thở ở mức bao nhiêu là vi phạm luật khi tham gia giao thông?...
Bài 16.12 trang 77 Sách bài tập Hóa học 11: Trên phổ hồng ngoại (IR) cho các tín hiệu ở các số sóng khác nhau. Cho biết tín hiệu nào đặc trưng của nhóm chức alcohol.....
Bài 16.13 trang 78 Sách bài tập Hóa học 11: Albuterol được sử dụng như một loại thuốc cho đường hô hấp, trị hen suyễn, có công thức:...
Bài 16.14 trang 78 Sách bài tập Hóa học 11: Một thí nghiệm của ethanol được tiến hành như sau:....
Bài 16.15 trang 78 Sách bài tập Hóa học 11: Mô tả thí nghiệm tìm hiểu phản ứng tách hydrogen trong nhóm -OH của alcohol đơn chức với polyalcohol như sau:.....
Bài 16.16 trang 78 Sách bài tập Hóa học 11: Biểu đồ dưới đây biểu diễn nhiệt độ sôi (°C) của một số alcohol. Nhận xét nhiệt độ sôi của các alcohol trên. Giải thích......
Bài 16.17 trang 79 Sách bài tập Hóa học 11: Cơm rượu (hay còn gọi là rượu nếp cái) là món ăn đặc sản trong dịp lễ Tết của người Việt, được truyền lại qua những nét đặc trưng riêng về khẩu vị của từng miền. Cơm rượu được chế biến từ gạo nếp, thành phần chủ yếu là tinh bột, nấu chín thành xôi, để nguội và ủ với men thích hợp trong khoảng 3-5 ngày. Sản phẩm có mùi thơm đặc trưng, vị thanh ngọt, cay nhẹ, hơi nồng, giúp kích thích tiêu hoá, ... Tuy nhiên, sử dụng nhiều có thể gây nên sự không tỉnh táo. Giải thích và viết phương trình chuyển hoá các chất trong quá trình ủ men thành cơm rượu....
Bài 16.18 trang 79 Sách bài tập Hóa học 11: Khi đến trạm bơm nhiên liệu và nhìn thấy dòng chữ quen thuộc như xăng E5 (hay xăng E5 RON 92, E5 A92), em hãy cho biết ý nghĩa của kí hiệu E5. Theo Quyết định số 53/2012/QĐ-TTg của Thủ tướng Chính phủ về lộ trình áp dụng tỉ lệ phối trộn nhiên liệu sinh học với nhiên liệu truyền thống, từ ngày 01/12/2017, xăng E10 được khuyến khích sản xuất, kinh doanh để sử dụng cho phương tiện cơ giới đường bộ trên toàn quốc. Khi xăng E10 được đưa vào tiêu thụ, trong các loại nhiên liệu như xăng E5, xăng E10, xăng A95, theo em, dùng nhiên liệu nào sẽ thân thiện với môi trường.....
Bài 16.19 trang 79 Sách bài tập Hóa học 11: Trong công nghiệp chế biến đường từ mía, nho, củ cải đường sẽ tạo ra sản phẩm phụ, gọi là rỉ đường hay rỉ mật, sử dụng rỉ đường để lên men tạo ra ethanol trong điều kiện thích hợp, hiệu suất cả quá trình là 90%. Tính khối lượng ethanol thu được từ 1 tấn rỉ đường mía theo 2 phương trình:...
Bài 16.20 trang 80 Sách bài tập Hóa học 11: Diethyl ether là hợp chất hữu cơ có công thức C2H5OC2H5 (viết tắt là Et2O) thường được sử dụng làm dung môi không proton phổ biến trong phòng thí nghiệm, dung môi đặc biệt quan trọng trong sản xuất nhựa cellulose như cellulose acetate. Et2O có chỉ số cetane (đại lượng quy ước cho khả năng tự bốc cháy của nhiên liệu, có trị số từ 0 - 100) cao, khoảng 85 - 96, làm chất kích nổ cho một số động cơ; Et2O kết hợp với các sản phẩm chưng cất dầu mỏ như xăng, dầu diesel, giúp khởi động lại động cơ ở nhiệt độ dưới 0°C.....
Bài 16.21 trang 80 Sách bài tập Hóa học 11: Hoá chất gây tác hại đến sức khoẻ con người và động vật. Các hoá chất khác nhau gây độc tính trên các bộ phận sẽ khác nhau, ví dụ, 2 gam chất (A) gây tổn thương cho gan, nhưng không hẳn 2 gam chất (A) sẽ gây tổn thương cho thận. Để so sánh độc tính giữa các hoá chất, người ta thực hiện thử nghiệm LD50. LD50 (Lethal Dose, 50%) là liều lượng hoá chất phơi nhiễm trong cùng một thời điểm, gây tử vong cho 50% cá thể của nhóm thử nghiệm. LD50 của ethanol đối với người trưởng thành trong khoảng 5 gam - 8 gam trên 1 kg trọng lượng cơ thể. Trung bình, một người trưởng thành nặng 60 kg, khi sử dụng đồ uống có cồn, lượng ethanol có thể gây ra tình trạng nguy kịch cho sức khoẻ là bao nhiêu?....
Bài 16.22 trang 80 Sách bài tập Hóa học 11: Cho các liên kết và giá trị năng lượng liên kết (Eb) của một số liên kết cộng hoá trị như sau:...
Bài 16.23 trang 81 Sách bài tập Hóa học 11: Hoạt động trải nghiệm......
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác: