Tailieumoi.vn xin giới thiệu bộ đề thi học kì 1 môn Hoá học lớp 11 sách Kết nối tri thức năm 2024 – 2025. Tài liệu gồm 4 đề thi có ma trận chuẩn bám sát chương trình học và đáp án chi tiết, được biên soạn bởi đội ngũ giáo viên THPT dày dặn kinh nghiệm sẽ giúp các em ôn tập kiến thức và rèn luyện kĩ năng nhằm đạt điểm cao trong bài thi học kì 1 Hoá học 11. Mời các bạn cùng đón xem:
Chỉ từ 50k mua trọn bộ Đề thi học kì 1 Hóa học 11 Kết nối tri thức bản word có lời giải chi tiết (chỉ từ 20k cho 1 đề thi lẻ bất kì):
B1: Gửi phí vào tài khoản 0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận tài liệu.
Xem thử tài liệu tại đây: Link tài liệu
Đề thi học kì 1 Hoá học 11 Kết nối tri thức có đáp án năm 2025
Đề thi học kì 1 Hoá học 11 Kết nối tri thức có đáp án - Đề 1
Sở Giáo dục và Đào tạo ...
Đề thi Học kì 1 - Kết nối tri thức
Năm học 2024 - 2025
Môn: Hoá học lớp 11
Thời gian làm bài: phút
(Đề số 1)
I. PHẦN TRẮC NGHIỆM (7,0 điểm)
Câu 1. Phản ứng nào sau đây là phản ứng thuận nghịch?
A. N2 + 3H2 ⇌ 2NH3.
B. Fe + 2HCl → FeCl2 + H2.
C. 2H2 + O2 ⟶ 2H2O.
D. 2KClO3 → 2KCl + 3O2.
Câu 2. Phát biểu nào sau đây về một phản ứng thuận nghịch tại trạng thái cân bằng là đúng?
A. Tốc độ của phản ứng thuận lớn hơn tốc độ của phản ứng nghịch.
B. Nồng độ của tất cả các chất trong hỗn hợp phản ứng là không đổi.
C. Nồng độ mol của chất phản ứng luôn bằng nồng độ mol của chất sản phẩm.
D. Phản ứng thuận và phản ứng nghịch đều dừng lại.
Câu 3. Trong các chất sau, chất không điện li là
A. KHCO3.
B. HCl.
C. KOH.
D. CH4.
Câu 4. Một dung dịch có nồng độ H+ bằng 0,01M thì pH và [OH−]của dung dịch này là
A. pH = 2; [OH-]=10-12 M.
B. pH = 2; [OH-]=10-10 M.
C. pH = 10-2; [OH-]=10-11 M.
D. pH = 2; [OH-]=10-11 M.
Câu 5. Trong không khí, chất nào sau đây chiếm phần trăm thể tích lớn nhất?
A. O2.
B. NO.
C. CO2.
D. N2.
Câu 6. Trong các phát biểu sau, phát biểu nào không đúng?
A. NH3 là chất khí không màu, không mùi, tan ít trong nước.
B. Khí NH3 nặng hơn không khí.
C. Khí NH3 dễ hoá lỏng, tan nhiều trong nước.
D. Phân tử NH3 chứa các liên kết cộng hoá trị phân cực.
Câu 7. Thành phần chính của quặng pyrite là
A. FeS.
B. FeS2.
C. CaSO4.
D. BaSO4.
Câu 8. Tính chất nào sau đây là tính chất vật lí của sulfur?
A. Chất khí, không màu.
B. Chất rắn, màu nâu đỏ.
C. Không tan trong benzene.
D. Không tan trong nước.
Câu 9. Bước sơ cứu đầu tiên cần làm ngay khi một người sulfuric acid đậm đặc đổ vào tay gây bỏng là
A. rửa với nước lạnh nhiều lần.
B. trung hoà acid bằng NaHCO3.
C. băng bó tạm thời vết bỏng.
D. đưa đến cơ sở y tế gần nhất.
Câu 10. Chất nào sau đây được dùng để bổ sung khoáng chất cho phân bón, thức ăn gia súc …?
A. BaSO4.
B. CaSO4.
C. MgSO4.
D. NH4SO4.
Câu 11. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu về
A. hợp chất của carbon.
B. hydrocarbon.
C. dẫn xuất hydrocarbon.
D. hợp chất hữu cơ.
Câu 12. Trong thành phần phân tử hợp chất hữu cơ nhất định phải có nguyên tố nào sau đây?
A. Hydrogen.
B. Carbon.
C. Carbon, hydrogen và oxygen.
D. Oxygen.
Câu 13. Để tách dầu ăn ra khỏi hỗn hợp dầu ăn và nước nên sử dụng phương pháp tách chất nào sau đây?
A. Phương pháp chưng cất.
B. Phương pháp chiết.
C. Phương pháp kết tinh.
D. Sắc kí cột.
Câu 14. Phương pháp chưng cất thường được dùng để tách riêng từng chất trong hỗn hợp nào sau đây?
A. Nước và dầu ăn.
B. Bột mì và nước.
C. Cát và nước.
D. Nước và rượu.
Câu 15. Hydrocarbon là hợp chất hữu cơ có thành phần nguyên tố gồm
A. carbon và hydrogen.
B. hydrogen và oxygen.
C. carbon và oxygen.
D. carbon và nitrogen.
Câu 16. Cặp chất nào sau đây cùng dãy đồng đẳng?
A. CH4 và C2H4.
B. CH4 và C2H6.
C. C2H4 và C3H4.
D. C2H2 và C4H4.
Câu 17. Cho cân bằng hoá học sau:
H2(g) + I2(g) ⇌ 2HI(g)
Biểu thức hằng số cân bằng của phản ứng trên là
A. KC = .
B. KC = .
C. KC = .
D. KC = .
Câu 18. Cho phản ứng thuận nghịch sau:
Trong phản ứng thuận, chất đóng vai trò là base theo thuyết Bronsted – Lowry là
A. .
B. H2O.
C. .
D. OH−.
Câu 19. Ammonia tan nhiều trong nước là do
A. phân tử có liên kết cộng hoá trị không cực.
B. có khả năng tạo liên kết hydrogen với nước.
C. phân tử có liên kết ion.
D. NH3 là một chất khí, mùi khai.
Câu 20. Trong khí quyển, khi có sấm sét nitrogen bị oxi hóa để tạo thành oxide của nitrogen. Oxide được tạo thành bởi quá trình này có công thức là
A. NO.
B. N2O5.
C. N2O.
D. N2O4.
Câu 21. Dãy gồm các kim loại không tác dụng với dung dịch HNO3 đặc, nguội là
A. Zn, Cu, Au, Pt.
B. Al, Fe, Au, Pt.
C. Mg, Cu, Au, Pt.
D. Mg, Ag, Au, Pt.
Câu 22. Cho phản ứng hoá học sau:
SO2 + 2H2S → 3S + 2H2O
Vai trò của của SO2 trong phản ứng trên là
A. chất khử.
B. acid.
C. base.
D. chất oxi hoá.
Câu 23. Cho kim loại Cu tác dụng với acid H2SO4 đặc, nóng. Khí sinh ra có tên gọi là
A. khí oxygen.
B. khí hydrogen.
C. khí carbonic.
D. khí sulfur dioxide.
Câu 24. Cho phổ hồng ngoại của chất X như hình dưới đây:
Phân tử chất X có chứa nhóm chức?
A. – CHO.
B. – COOH.
C. – OH.
D. –NH2.
Câu 25. Cho hình vẽ mô tả quá trình chiết hai chất lỏng không trộn lẫn vào nhau:
Phát biểu nào sau đây là sai?
A. Chất lỏng nhẹ hơn sẽ nổi lên trên trên phễu chiết.
B. Chất lỏng nhẹ hơn sẽ được chiết trước.
C. Chất lỏng nặng hơn sẽ ở phía dưới đáy phễu chiết.
D. Chất lỏng nặng hơn sẽ được chiết trước.
Câu 26. Phổ khối lượng của hợp chất hữu cơ X được cho như hình vẽ bên dưới:
Phân tử khối của hợp chất hữu cơ X là
A. 80.
B. 78.
C. 76.
D. 50.
Câu 27. Công thức hoá học nào sau đây không phù hợp với thuyết cấu tạo hoá học?
A. CH3 – CH2 – OH.
B. CH3–O=CH–CH3.
C. CH3 – CH2 – CH2 – NH2.
D. CH3Cl.
Câu 28. Cặp chất nào sau đây là đồng phân của nhau?
A. CH3C6H4Cl và C6H5Cl.
B. CH3OH và CH3CH2OH.
C. CH3OCH3 và CH3 CH2OH.
D. C6H5OH và C2H5OH.
II. PHẦN TỰ LUẬN. (3,0 điểm)
Câu 29. Kết quả phân tích nguyên tố cho thấy thành phần phần trăm khối lượng các nguyên tố có trong hợp chất X như sau: carbon là 52,17%; hydrogen là 13,04%; còn lại là oxygen.
Biết phân tử khối của X là 46. Xác định công thức phân tử của hợp chất X.
Câu 30. Viết đồng phân cấu tạo mạch carbon hở của hợp chất hữu cơ có công thức phân tử: C4H10O.
Câu 31. Sulfur dioxide là chất khí, không màu, có mùi hắc, độc,… Đặc biệt, khí sulfur dioxide là một trong những tác nhân gây mưa acid. Hãy đề xuất các biện pháp nhằm giảm lượng khí sulfur dioxide thải vào bầu khí quyển?
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
Phần I: Trắc nghiệm
|
1 - A |
2 - B |
3 - D |
4 - A |
5 - D |
6 - B |
7 - B |
8 - D |
9 - A |
10 - C |
|
11 - D |
12 - B |
13 - B |
14 - D |
15 - A |
16 - B |
17 - C |
18 - A |
19 - B |
20 - A |
|
21 - B |
22 - D |
23 - D |
24 - B |
25 - B |
26 - B |
27 - B |
28 - C |
|
|
Phần II. Tự luận
Câu 29:
Gọi công thức tổng quát của X là CxHyOz.
%O = 100% - %C - %H = 34,79%.
Ta có tỉ lệ: x : y : z = = 2 : 6 : 1
Vậy công thức đơn giản nhất của X là C2H6O.
Mối liên hệ giữa công thức phân tử và công thức đơn giản nhất của X là:
CxHyOz = (C2H6O)n.
Theo bài ra, phân tử khối của X là 46 nên: 46n = 46 Þ n = 1.
Công thức phân tử của X là: C2H6O.
Câu 30:
Các đồng phân:
Câu 31:
Mội số biện pháp nhằm giảm lượng khí sulfur dioxide thải vào bầu khí quyển là:
- Tăng cường sử dụng các nguồn năng lượng mới, năng lượng sạch, năng lượng tái tạo;
- Sử dụng tiết kiệm, hiệu quả nguồn tài nguyên thiên nhiên;
- Cải tiến công nghệ sản xuất, có biện pháp xử lí khí thải và tái chế các sản phẩm phụ có chứa sulfur.
---HẾT---
Đề thi học kì 1 Hoá học 11 Kết nối tri thức có đáp án - Đề 2
Sở Giáo dục và Đào tạo ...
Đề thi Học kì 1 - Kết nối tri thức
Năm học 2024 - 2025
Môn: Hoá học lớp 11
Thời gian làm bài: phút
(Đề số 2)
I. PHẦN TRẮC NGHIỆM (7,0 điểm)
Câu 1. Phản ứng thuận nghịch là phản ứng
A. xảy ra theo hai chiều ngược nhau trong cùng điều kiện.
B. có phương trình hoá học được biểu diễn bằng mũi tên một chiều.
C. chỉ xảy ra theo một chiều nhất định.
D. xảy ra giữa hai chất khí.
Câu 2. Cho các nhận xét sau:
(a) Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản nghịch.
(b) Ở trạng thái cân bằng, các chất không phản ứng với nhau.
(c) Ở trạng thái cân bằng, nồng độ chất sản phẩm luôn lớn hơn nồng độ chất ban đầu.
(d) Ở trạng thái cân bằng, nồng độ các chất không thay đổi.
Các nhận xét đúng là
A. (a) và (b).
B. (b) và (c).
C. (a) và (c).
D. (a) và (d).
Câu 3. Cho dãy các chất sau: NaOH, KCl, H2SO3, CuO, C6H12O6 (glucose). Số chất điện li có trong dãy là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 4. Dung dịch NaOH 0,01M có pH là
A. 1.
B. 2.
C. 11.
D. 12.
Câu 5. Ở nhiệt độ thường, nitrogen khá trơ về mặt hoạt động hóa học là do
A. nitrogen có bán kính nguyên tử nhỏ.
B. nitrogen có độ âm điện lớn.
C. phân tử nitrogen có liên kết ba bền vững.
D. phân tử nitrogen không phân cực.
Câu 6. Trong các phát biểu sau, phát biểu nào không đúng?
A. NH3 là chất khí không màu, không mùi, tan nhiều trong nước.
B. Khí NH3 nặng hơn không khí.
C. Khí NH3 dễ hoá lỏng, tan nhiều trong nước.
D. Phân tử NH3 chứa các liên kết cộng hoá trị phân cực.
Câu 7. Thành phần chính của quặng pyrite là
A. PbS.
B. FeS2.
C. CaSO4.
D. BaSO4.
Câu 8. Ứng dụng nào sau đây không là ứng dụng của sulfur?
A. Lưu hoá cao su.
B. Sản xuất diêm, thuốc nổ.
C. Sản xuất nitric acid.
D. Sản xuất thuốc trừ sâu, thuốc diệt nấm.
Câu 9. Lưu ý bắt buộc để đảm bảo an toàn khi sử dụng dung dịch sulfuric acid đặc là
A. bảo quản sulfuric acid trong lọ bằng chất dẻo.
B. đè chai đựng acid lên miệng cốc khi rót acid.
C. lượng acid dư thừa sau khi sử dụng phải đổ xuống cống thoát nước.
D. không đổ nước vào dung dịch acid đặc.
Câu 10. Chất nào sau đây được dùng làm chất phụ gia để làm đông các sản phẩm như đậu hũ, đậu non…?
A. BaSO4.
B. CaSO4.
C. MgSO4.
D. (NH4)2SO4.
Câu 11. Nhận xét nào dưới đây về đặc điểm chung của các chất hữu cơ không đúng?
A. Các hợp chất hữu cơ thường khó bay hơi, bền với nhiệt và khó cháy.
B. Liên kết hoá học chủ yếu trong các phân tử hợp chất hữu cơ là liên kết cộng hoá trị.
C. Các hợp chất hữu cơ thường không tan hoặc ít tan trong nước, tan trong dung môi hữu cơ.
D. Các phản ứng hoá học của hợp chất hũu cơ thường xảy ra chậm và theo nhiều hướng khác nhau tạo ra một hỗn hợp các sản phẩm.
Câu 12. Hợp chất nào sau đây không là hợp chất hữu cơ?
A. CH4.
B. HCN.
C. CH3OH.
D. CH3Cl.
Câu 13. Phương pháp chiết là sự tách chất dựa vào sự khác nhau
A. về kích thước phân tử.
B. ở mức độ nặng nhẹ về khối lượng.
C. về khả năng bay hơi.
D. về khả năng tan trong các dung môi khác nhau.
Câu 14. Phương pháp kết tinh được ứng dụng trong trường hợp nào dưới đây?
A. Tinh chế đường đỏ thành đường trắng.
B. Tách β – carotene từ nước ép cà rốt.
C. Nấu rượu để uống.
D. Ngâm rượu thuốc.
Câu 15. Chất nào sau đây là dẫn xuất của hydrocarbon?
A. CO2.
B. CH4.
C. CH3Cl.
D. HCN.
Câu 16. Các chất hữu cơ có tính chất hoá học tương tự nhau và thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 được gọi là các chất
A. đồng phân của nhau.
B. đồng đẳng của nhau.
C. đồng vị của nhau.
D. đồng khối của nhau.
Câu 17. Cho phản ứng sau: 2C(s) + O2(g) ⇌ 2CO(g). Biểu thức hằng số cân bằng KC của phản ứng là
A. KC = \(\frac{{{{\left[ {CO} \right]}^2}}}{{{{\left[ C \right]}^2}.\left[ {{O_2}} \right]}}\)
B. KC = \(\frac{{{{\left[ {CO} \right]}^2}}}{{\left[ {{O_2}} \right]}}\)
C. KC = \(\frac{{{{\left[ C \right]}^2}.\left[ {{O_2}} \right]}}{{{{\left[ {CO} \right]}^2}}}\)
D. KC = \(\frac{{\left[ {{O_2}} \right]}}{{{{\left[ {CO} \right]}^2}}}\)
Câu 18. Cho phản ứng thuận nghịch sau:
NH3 + H2O ⇌ \[NH_4^ + + O{H^ - }\]
Trong phản ứng nghịch, theo thuyết Bronsted – Lowry chất nào là acid?
A. NH3. B. H2O.
C. OH−. D. NH4+.
Câu 19. Phân biệt được dung dịch NH4NO3 và NaNO3 bằng thuốc thử là dung dịch
A. NaCl. B. KNO3.
C. NaOH. D. K2SO4.
Câu 20. Trong phản ứng với chất nào sau đây, nitrogen thể hiện tính khử?
A. H2. B. O2.
C. NH3. D. Mg.
Câu 21. Nitric acid thể hiện tính acid khi tác dụng với chất nào sau đây?
A. S. B. Mg.
C. Fe2O3. D. FeO.
Câu 22. Chất khí (X) tan trong nước tạo ra dung dịch làm quỳ tím hoá đỏ và khí (X) có thể được dùng làm chất tẩy màu. Khí (X) là
A. NH3. B. CO2.
C. SO2. D. O3.
Câu 23. Để phân biệt hai dung dịch NaCl và Na2SO4 có thể dùng thuốc thử là
A. BaSO4. B. BaCl2.
C. BaCO3. D. HNO3.
Câu 24. Phổ hồng ngoại là phương pháp vật lí rất quan trọng và phổ biến để nghiên cứu về
A. thành phần nguyên tố chất hữu cơ.
B. thành phần phân tử hợp chất hữu cơ.
C. cấu tạo hợp chất hữu cơ.
D. cấu trúc không gian hợp chất hữu cơ.
Câu 25. Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36 °C), heptane (sôi ở 98 °C), octane (sôi ở 126 °C) và nonane (sôi ở 151 °C). Có thể tách riêng các chất đó bằng cách nào sau đây?
A. Chiết.
B. Kết tinh.
C. Bay hơi.
D. Chưng cất.
Câu 26. Phổ khối lượng của hợp chất hữu cơ X được cho như hình vẽ bên dưới:
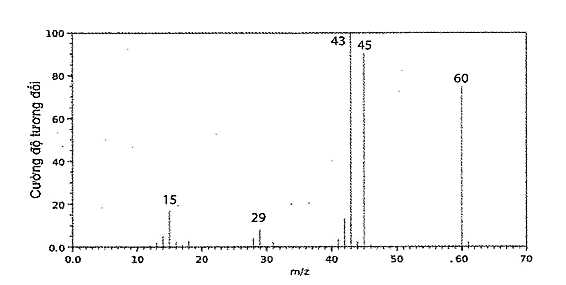
Phân tử khối của hợp chất hữu cơ X là
A. 45. B. 60.
C. 43. D. 15.
Câu 27. Công thức hoá học nào sau đây phù hợp với thuyết cấu tạo hoá học?
A. CH3 – CH2 = OH.
B. CH3–O=CH–CH3.
C. CH3 – CH2 – CH2 – N.
D. CH3CH2Cl.
Câu 28. Cặp chất nào dưới đây là đồng phân loại nhóm chức?
A. CH3OH và C2H5OH.
B. CH3CH2OH và CH3OCH3.
C. CH2 = CH – CH3 và CH≡CH2 – CH3.
D. CH3CH2CH2OH và CH3CH(OH)CH3.
II. PHẦN TỰ LUẬN. (3,0 điểm)
Câu 29. Acetone là một hợp chất hữu cơ dùng để làm sạch dụng cụ trong phòng thí nghiệm, tẩy rửa sơn móng tay và là chất đầu trong nhiều quá trình tổng hợp hữu cơ. Kết quả phân tích nguyên tố của acetone như sau: 62,07% C; 27,59% O về khối lượng, còn lại là hydrogen. Phân tử khối của acetone được xác định thông qua phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất bằng 58. Lập công thức phân tử của acetone.
Câu 30. Viết công thức cấu tạo (đầy đủ và thu gọn) của các chất có công thức phân tử như sau: C4H10, C2H6O.
Câu 31. Em hãy đề xuất một số giải pháp phù hợp với lứa tuổi học sinh giúp giảm thiểu lượng sulfur dioxide thải vào không khí.
ĐÁP ÁN VÀ HƯỚNG DẪN
Phần I. Trắc nghiệm
|
1 - A |
2 - D |
3 - C |
4 - D |
5 - C |
6 - B |
7 - B |
8 - C |
9 - D |
10 - B |
|
11 - A |
12 - B |
13 - D |
14 - A |
15 - C |
16 - B |
17 - B |
18 - D |
19 - C |
20 - B |
|
21 - C |
22 - C |
23 - B |
24 - C |
25 - D |
26 - B |
27 - D |
28 - B |
|
|
Phần II: Tự luận
Câu 29:
%mH = 100% - 62,07% - 27,59% = 10,34%.
Đặt công thức phân tử của acetone là: CxHyOz.
Ta có:
x : y : z = \[\frac{{\% {m_C}}}{{12}}:\frac{{\% {m_H}}}{1}:\frac{{\% {m_O}}}{{16}} = \frac{{62,07}}{{12}}:\frac{{10,34}}{1}:\frac{{27,59}}{{16}} = 3:6:1\]
Công thức đơn giản nhất của acetone là: C3H6O.
Công thức phân tử của acetone theo công thức đơn giản nhất có dạng: (C3H6O)n.
Từ phổ khối lượng của acetone xác định được Macetone = 58 Þ n = 1.
Công thức phân tử của acetone là: C3H6O.
Câu 30:
|
Công thức phân tử |
Công thức cấu tạo đầy đủ |
Công thức cấu tạo thu gọn |
|
C4H10 |
|
CH3 – CH2 – CH2 – CH3 |
|
|
CH3 – CH(CH3) – CH3 |
|
|
C2H6O |
|
CH3 – CH2 – OH |
|
|
CH3 – O – CH3 |
Câu 31:
Một số biện pháp phù hợp với lứa tuổi học sinh giúp giảm thiểu lượng sulfur dioxide thải vào không khí:
- Sử dụng tiết kiệm nhiên liệu khi đun nấu …
- Tuyên truyền vận động mọi người sử dụng các nguồn nhiên liệu sinh học thân thiện với môi trường.
- Tuyên truyền vận động mọi người sử dụng các nguồn năng lượng tái tạo như năng lượng mặt trời, năng lượng gió …
Đề thi học kì 1 Hoá học 11 Kết nối tri thức có đáp án - Đề 3
Sở Giáo dục và Đào tạo ...
Đề thi Học kì 1 - Kết nối tri thức
Năm học 2024 - 2025
Môn: Hoá học lớp 11
Thời gian làm bài: phút
(Đề số 3)
Câu 1 : Chất nào sau đây không có cùng công thức đơn giản nhất là C2H2?
C4H4
C6H6
C8H8
C3H4
Câu 2 : Theo thuyết Bronsted – Lowry, chất nào sau đây là acid?
NH3
NaOH
C2H5OH
CH3COOH
Câu 3 : Cặp chất nào sau đây là hợp chất hữu cơ
CO, NaHCO3
C2H5Br, CH5N
NaCN, K2CO3
CaC2, CaCO3
Câu 4 : Cặp chất nào sau đây là đồng đẳng của nhau?
CH3OH, C2H5OH
CH3OCH3, CH3CHO
C2H5OH, C2H4(OH)2
C2H5Cl, CH3Br
Câu 5 : Khi cháy, sulfur cũng như hợp chất của sulfur tạo khí SO2. Khí SO2 làm mất tím dung dịch thuốc tím theo sơ đồ phản ứng: SO2 + KMnO4 + H2O ⟶ H2SO4 + MnSO4 + K2SO4. Hàm lượng sulfur cho phép trong xăng là dưới 0,30%. Để kiểm tra hàm lượng lưu hùynh trong một loại xăng, người ta đốt cháy hoàn toàn 10,0 gam xăng này, tạo sản phẩm cháy coi như chỉ gồm CO2, SO2 và H2O. Thấy lượng sản phẩm cháy này làm mất màu vừa đủ dung dịch có hòa tan 3,5.10-4 mol KMnO4. Hàm lượng sulfur có trong mẫu xăng trên là
0,27%
0,72%.
0,35%.
0,28%.
Câu 6 : Dựa vào các số sóng hấp thụ đặc trưng trên phổ IR ta có thể dự đoán được?
thành phần cấu tạo nên hợp chất hữu cơ.
màu sắc của các hợp chất hữu cơ.
nhóm chức trong phân tử hợp chất hữu cơ.
tính chất của các hợp chất hữu cơ.
Câu 7 : Phương pháp dùng để tách các chất hữu cơ có hàm lượng nhỏ và khó tách ra khỏi nhau là phương pháp nào sau đây?
Phương pháp chưng cất.
Phương pháp chiết
Phương pháp kết tinh.
Sắc kí cột.
Câu 8 : Giã lá cây chàm, cho vào nước, lọc lấy dung dịch màu để nhuộm sợi, vải thuộc loại phản ứng tách biệt và tinh chế nào?
Phương pháp chưng cất.
Phương pháp chiết
Phương pháp kết tinh.
Sắc kí cột.
Câu 9 : Glucose là hợp chất hữu cơ có nhiều trong các loại quả chín, đặc biệt là quả nho. Công thức phân tử của glucose là C6H12O6. Công thức đơn giản nhất của glucose là
C1,5H3O1,5.
CH2O.
C3H4O3.
CHO2.
Câu 10 : Để xác định phân tử khối của hợp chất hữu cơ, người ta sử dụng phổ khối lượng MS, trong đó phân tử khối của chất là giá trị m/z của
peak [M+] lớn nhất.
peak [M+] nhỏ nhất.
peak xuất hiện nhiều nhất.
nhóm peak xuất hiện nhiều nhất.
Câu 11 : Hợp chất hữu cơ X có 82,76 % khối lượng là carbon, còn lại là hydrogen. Công thức đơn giản nhất của X là
CH5.
C5H.
C2H5.
C5H2.
Câu 12 : Xác định công thức cấu tạo thu gọn của hợp chất sau:
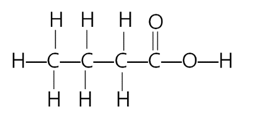
CH3CH2CH2COOH.
CH3CH2COOH.
CH3CH2CH2OH.
CH3CH2CHOHCHO.
Câu 13 : Hiện tượng các chất có cấu tạo và tính chất hoá học tương tự nhau, phân tử hơn kém nhau một hay nhiều nhóm methylen (–CH2–) được gọi là hiện tượng
đồng phân.
đồng vị.
đồng đẳng.
đồng khối.
Câu 14 : Trong những dãy chất sau đây, dãy nào có các chất là đồng phân của nhau?
C2H5OH, CH3OCH3.
CH3OCH3, CH3CHO.
CH3CH2CH2OH, C2H5OH.
C4H10, C6H6.
Câu 15 : Công thức cấu tạo thu gọn nhất của một hợp chất X như sau:
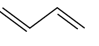
Công thức cấu tạo thu gọn của X là
CH2=CH−CH2−CH=CH2.
CH2=C=CH2.
CH2=CH−CH=CH2.
CH3−CH=CH−CH3.
Câu 16 : Dựa vào phổ hồng ngoại (IR) của hợp chất X có công thức CH3COCH3 dưới đây, hãy chỉ ra peak nào giúp dự đoán X có nhóm C=O?
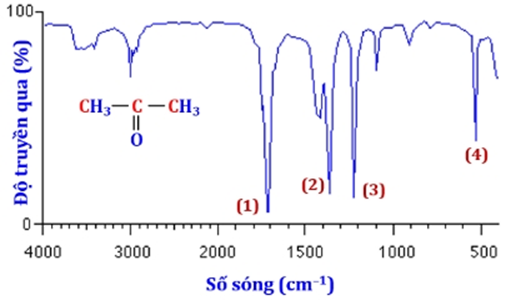
(1).
(2).
(3).
(4).
Câu 17 : Số lượng đồng phân mạch hở, có hai liên kết đôi, ứng với công thức phân tử C4H6 là
3
4
5
2
Câu 18 : Cặp chất nào dưới đây là đồng phân vị trí nhóm chức?
CH3OCH3 và CH3OH
CH3COOH và CH3CH2COOH
CH3CH2CH2OH và CH3CH(OH)CH3
CH≡CCH2CH3 và CH3CH2 = CH – CH = CH2
Câu 1 : Khói thuốc lá làm tăng khả năng bị ung thư phổi, hoạt chất có độc trong thuốc lá là nicotine. Kết quả phân tích nguyên tố của nicotine cho thành phần phần trăm khối lượng như sau: 74,07%C, 8,65%H, 17,28%N. Phân tử khối của nicotine được xác định thông qua phổ khối lượng thấy có phân tử khối là 162.
a. Nicotine thuộc loại dẫn xuất hydrocarbon.
b. Trên phổ khối lượng của nicotine xuất hiện peak ion phân tử [M+] tại giá trị m/z = 162.
c. Công thức đơn giản của nicotine là C5H7N
d. Công thức phân tử của nicotine trùng với công thức đơn giản nhất.
Câu 2 : Thành phần phần trăm về khối lượng nguyên tố có trong hợp chất X là 90% C và 10% H. Phổ MS cho thấy X có phân tử khối là 40.
a. Công thức thực nghiệm của X là CH2.
b. Công thức phân tử của X là C3H6
c. Trong X có 1 liên kết π.
d. X có đồng phân mạch thẳng và mạch nhánh.
Câu 3 : Phương trình hóa học của phản ứng tổng hợp ammonia từ nitrogen và hydrogen bằng quá trình Habber như sau:
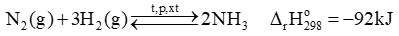
a. Phản ứng trên là phản ứng thuận nghịch nên tại thời điểm cân bằng, hỗn hợp trong buồng phản ứng gồm ammonia, nitrogen và hydrogen.
b. Nếu giảm áp suất của hệ thì phản ứng sẽ chuyển dịch theo chiều thuận
c. Phản ứng thuận là phản ứng tỏa nhiệt. Vì vậy, để phản ứng chuyển dịch theo chiều thuận, cần phải giảm nhiệt độ. Tuy nhiên, nếu giảm nhiệt độ xuống thấp thì tốc độ phản ứng lại nhỏ.
d. Từ giá trị biến thiên enthalpy chuẩn của phản ứng trên và năng lượng liên kết H-H, N-H lần lượt là 436 kJ mol-1 và 389 kJ mol-1 sẽ xác định được năng lượng liên kết trong phân tử N2 ở cùng điều kiện là 934 kJ mol-1.
Câu 4 : Phú dưỡng là hiện tượng dư thừa quá nhiều các nguyên tố dinh dưỡng (N, P) trong các nguồn nước làm cho các sinh vật trong nước như vi khuẩn, tảo, rong, rêu,… phát triển nhanh.
a. Nguyên nhân gây ra hiện tượng phú dưỡng do nguồn nước thải nông nghiệp, công nghiệp, sinh hoạt, ... chưa xử lí triệt để thải vào ao hồ.
b. Hiện tượng phú dưỡng làm giảm sự quang hợp của thực vật thủy sinh và làm tăng nguồn oxygen của tôm, cá, … gây mất cân bằng hệ sinh thái.
c. Các loại tôm, cá, … ở ao hồ có hiện tượng phú dưỡng thường khỏe mạnh và béo tốt vì có nguồn chất dinh dưỡng phong phú.
d. Để khắc phục hiện tượng phú dưỡng ta cần xử lí nước thải trước khi thải vào môi trường, sử dụng phân bón đúng liều lượng, khơi thông kênh rạch, ao hồ, lưu thông dòng nước.
Câu 1 : Điều chế NH3 từ hỗn hợp gồm N2 và H2 (tỉ lệ mol tương ứng là 1: 3). Tỉ khối của hỗn hợp trước so với hỗn hợp sau phản ứng là 0,6. Hiệu suất phản ứng là?
Câu 2 : Hòa tan hết 5,07 gam oleum có công thức H2SO4.3SO3 vào nước dư. Trung hòa dung dịch thu được cần V mL dung dịch NaOH 1 M. Giá trị của V là bao nhiêu?
Câu 3 : Cho các chất sau: CH4, CH3-CH2-NH2, CH2=CH2, CH3-COOH, CH2=C(CH3)-CH=CH2, C3H5(OH)3, CH≡CH, C6H5OH, CH3CHO, CH3COOCH2CH3, H2N-CH(CH3)-COOH. Có bao nhiêu chất thuộc dẫn xuất của hydrocarbon?
Câu 4 : Phân tích định lượng Atabrine, một loại thuốc chống sốt rét, người ta xác định được chất này chứa 69,1% carbon, 7,5% hydrogen, 10,5% nitrogen, 8,9% chlorine và 4,0% oxygen về khối lượng. Số nguyên tử nitrogen trong Atabrine là?
ĐÁP ÁN VÀ HƯỚNG DẪN
Phần I. Trắc nghiệm
| 1. D | 2. D | 3. B | 4. A | 5. D | 6. C |
| 7. D | 8. B | 9. B | 10. A | 11. C | 12. A |
| 13. C | 14. A | 15. C | 16. A | 17. D | 18. C |
a. đúng
b. đúng
c. đúng
d. sai, công thức phân tử nicotine là C10H14N2.
Câu 2 :
Số nguyên tử C:
Số nguyên tử H:
a. sai, công thức thực nghiệm của X là C3H4.
b. sai, công thức phân tử X là C3H4
c. sai, trong X có 2 liên kết pi
d. sai, X không có đồng phân mạch nhánh.
Câu 3 :
a. đúng
b. sai, tăng áp suất của hệ thì phản ứng sẽ chuyển dịch theo chiều thuận
c. đúng
d. đúng
Câu 4 :
a. đúng
b. sai, làm giảm nguồn oxygen của tôm, cá,…
c. sai, các loại tôm cá,… ở ao hồ có hiện tượng phú dưỡng sẽ chết hàng loạt do thiếu oxygen hòa tan trong nước.
d. đúng
Giả sử số mol N2 và H2 ban đầu lần lượt là 1 và 3 mol
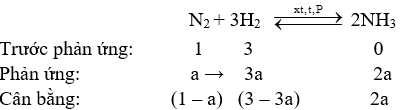
Vì tỉ khối của hỗn hợp trước phản ứng so với hỗn hợp sau phản ứng là 0,6 nên ta có:
Hiệu suất phản ứng:
Câu 2 :
n oleum = 5,07 : 338 = 0,015 mol
H2SO4.3SO3 + 3H2O → 4H2SO4
0,015 → 0,06
H2SO4 + 2NaOH → Na2SO4 + H2O
0,06 → 0,12
V NaOH = 0,12 : 1 = 0,12L
Câu 3 :Có 7 chất CH3-CH2-NH2, CH3-COOH, C3H5(OH)3, C6H5OH, CH3CHO, CH3COOCH2CH3, H2N-CH(CH3)-COOH thuộc dẫn xuất hydrocarbon
Câu 4 :
C : H : N : Cl : O =
Số nguyên tử N trong Atabrine là 3.