Tailieumoi.vn sưu tầm và biên soạn chuyên đề Ancol gồm đầy đủ lý thuyết, các dạng bài tập chọn lọc và ví dụ minh họa từ cơ bản đến nâng cao giúp học sinh ôn luyện kiến thức, biết cách làm bài tập môn Hóa học 11.
Chuyên đề Ancol
I. LÍ THUYẾT TRỌNG TÂM
1. Cấu tạo, đồng đẳng, đồng phân, danh pháp
a. Đặc điểm cấu tạo
“Nhóm OH” gắn ở C no và mỗi C no chỉ được gắn 1 nhóm OH. Công thức phân tử chung của một số dãy đồng đẳng ancol:
Ví dụ:
b. Đồng phân
Ví dụ: C3H7OH có một dạng mạch C không nhánh, hở, nhưng có hai đồng phân vị trí OH và có một đồng phân dạng ete.
c. Danh pháp
Tên thông thường: Ancol + tên gốc hiđrocacnol + ic.
Tên theo IUPAC: Tên IUPAC của hiđrocacbon + số chỉ vị trí OH + ol (1)/ điol (2)/ triol (3)…
(ưu tiên đánh số thứ tự cacbon mạch chính sao cho các chỉ số nhóm OH là nhỏ nhất).
Ví dụ:
n-C3H7OH:
Tên: Ancol n-proylic/propan-1-ol.
C2H4(OH)2:
Tên: Etylenglicol/etan-1,2-điol.
CH2=CHCH2OH:
Tên: Ancol anlylic/propen-1-ol.
2. Tính chất vật lí và liên kết hiđro
Các phân tử có nhóm OH (nước, ancol, axit axetic…) có liên kết liên phân tử: – O – H…O – H làm tăng nhiệt độ sôi và độ tan trong nước hơn so với chất không có nhóm OH.
Ví dụ:
Dựa vào bảng hằng số vật lí của một số ancol (trang 181 SGK):
Ví dụ: Bảng nhiệt độ sôi (ts) một số ancol như sau:
|
Ancol |
Khối lượng phân tử |
ts (oC) |
|
CH3OH |
32 |
64,5 |
|
C3H7OH |
60 |
82,4 |
|
C2H4(OH)2 |
62 |
197,6 |
Công thức tính độ rượu:
Độ rượu =
Ví dụ: Cồn 96o nghĩa là
Trong 100 ml cồn này thì có 96 ml C2H5OH.
3. Tính chất hoá học
· Phản ứng thế H của nhóm OH (phản ứng với kim loại kiềm, phản ứng tạo phức với đồng(II) hiđroxit của glixerol).
Ví dụ: Glixerol – một ancol no, đa chức mạch hở: phản ứng được với Na, hoà tan Cu(OH)2.
· Phản ứng thế nhóm OH ancol (phản ứng với HX tạo dẫn xuất halogen, phản ứng giữa hai phân tử ancol tạo ete).
· Phản ứng este hoá với axit cacboxylic R – COOH.
· Phản ứng tách nước tạo thành anken.
· Phản ứng oxi hoá không hoàn toàn:
+ Ancol bậc I Anđehit, axit.
+ Ancol bậc II Xeton.
+ Ancol bậc III Không phản ứng.
· Phản ứng oxi hoá hoàn toàn (Phản ứng cháy).
Ví dụ: Etanol có phản ứng với các chất: Na, K, HCl, HBr, CH3COOH, CuO, lên men giấm, tách nước ở trên 170oC tạo etilen, dưới 170oC tạo đietyl ete.
Khi cháy:
Chú ý: Ancol no, mạch hở khi cháy:
4. Điều chế
Phương pháp điều chế etanol: thuỷ phân dẫn xuất halogen, hiđrat hoá etilen, lên men rượu glucozơ.
II. CÁC DẠNG BÀI TẬP
Dạng 1: Cấu tạo, đồng phân, danh pháp, tính chất vật lí, ứng dụng
Kiểu hỏi 1: Ancol có tồn tại hay không? Công thức dãy đồng đẳng ancol
Phương pháp giải
Ancol là hợp chất chứa nhóm OH gắn ở nguyên tử C no.
Chú ý: OH gắn ở cacbon không no sẽ không bền, không tồn tại chuyển thành chất khác.
Mỗi C no chỉ chứa tối đa 1 nhóm OH. Nếu có trên 1 nhóm thì tách nước tạo anđehit hoặc axit.
Ví dụ: Ancol nào sau đây không tồn tại?
A. Xiclohexanol C6H11OH.
B. CH2 = CHOH.
C. C2H4(OH)2.
D. (CH3)3C – OH.
Hướng dẫn giải
A, C, D đúng.
B sai vì OH gắn vào C không no nên không tồn tại, chuyển thành chất khác.
Chọn B.
Ví dụ mẫu
Ví dụ 1: Cho các chất có công thức cấu tạo:
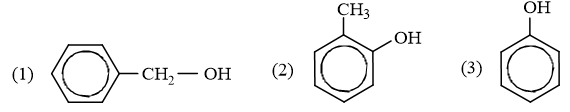
Chất thuộc loại ancol là
A. (1) và (2). B. chỉ có (1).
C. (1) và (3). D. cả (1), (2) và (3).
Hướng dẫn giải
Ancol là hợp chất chứa nhóm OH gắn ở nguyên tử C no.
Chỉ có (1) là ancol.
Chọn B.
Kiểu hỏi 2: Đếm số đồng phân ancol no mạch hở
Phương pháp giải
Viết các dạng mạch C; sau đó gắn OH vào những vị trí C khác nhau, chú ý tính đối xứng của mạch.
Chú ý: Cách viết đồng phân ete: Cũng mạch C như trên, ta đặt nguyên tử O vào giữa hai C.
Ví dụ: Viết các đồng phân ancol có công thức phân tử C4H10O.
Hướng dẫn giải
C4H10O có 4 đồng phân ancol:
CH3 – CH2 – CH2 – CH2 – OH
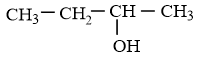
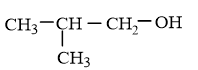
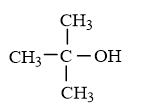
Ví dụ mẫu
Ví dụ 1: Số đồng phân của hợp chất hữu cơ có công thức C4H10O là
A. 2 đồng phân. B. 4 đồng phân.
C. 7 đồng phân. D. 9 đồng phân.
Hướng dẫn giải
Hợp chất hữu cơ có công thức phân tử CxH2x+2O có độ bội liên kết bằng 0.
Do đó công thức cấu tạo đồng phân dạng ete và ancol no đơn chức mạch hở.
Với dạng mạch C – C – C – C: có 2 ancol + 2 ete.
Với dạng mạch C – C(CH3) – C: có 2 ancol + 1 ete.
Do đó, có tất cả 7 đồng phân.
Chọn C.
Kiểu hỏi 3: So sánh nhiệt độ sôi, tính tan của ancol với các chất
Phương pháp giải
Các phân tử có nhóm OH (nước, ancol, axit axetic…) có liên kết liên phân tử: – OH…OH làm tăng độ sôi và độ tan trong nước hơn so với chất không có nhóm OH.
Chú ý: Nhiệt độ sôi của: R – COOH > C6H5OH (phenol) > Ancol > Các hợp chất không chứa nhóm OH.
Khối lượng phân tử tăng thì nhiệt độ sôi tăng, độ tan trong nước giảm.
Ví dụ: So sánh nhiệt độ sôi và tính tan trong nước của các chất sau: etan, etyl clorua, etanol và propanol.
Hướng dẫn giải
Nhiệt độ sôi:
C2H6 < C2H5Cl < C2H5OH < C3H7OH.
Độ tan trong nước:
C2H6 < C2H5Cl < C3H7OH < C2H5OH.
Ví dụ mẫu
Ví dụ 1: Trong dãy đồng đẳng ancol no đơn chức, khi mạch cacbon tăng, nói chung
A. nhiệt độ sôi tăng, khả năng tan trong nước giảm.
B. nhiệt độ sôi tăng, khả năng tan trong nước tăng.
C. nhiệt độ sôi giảm, khả năng tan trong nước giảm.
D. nhiệt độ sôi giảm, khả năng tan trong nước tăng.
Hướng dẫn giải
Khi mạch cacbon tăng: nhiệt độ sôi tăng, độ tan trong nước giảm.
Chọn A.
Ví dụ 2: Trong các chất sau, chất nào có nhiệt độ sôi cao nhất?
A. CH3OCH3. B. C6H5OH.
C. CH3COOH. D. CH3CH2OH.
Hướng dẫn giải
Nhiệt độ sôi của: R – COOH > C6H5OH > Ancol > Các hợp chất không chứa nhóm OH.
Chất có nhiệt độ sôi cao nhất là CH3COOH.
Chọn C.
Ví dụ 3: Dung dịch rượu loãng, có độ rượu 5o – 10o chủ yếu dùng để
A. lên men giấm. B. làm cồn y tế.
C. làm dung môi. D. làm chất đốt.
Hướng dẫn giải
Dung dịch rượu loãng 5o – 10o dùng để lên men giấm ăn.
Chọn A.
III. Bài tập tự luyện dạng 1
Bài tập cơ bản
Câu 1: Cho các chất sau:
|
(1) HO – CH2 – CH2OH (3) HOCH2 – CHOH – CH2OH |
(2) HO – CH2 – CH2 – CH2OH (4) C2H5 – O – C2H5 |
Những chất thuộc loại ancol đa chức là
A. (1), (2) và (3). B. (3) và (2).
C. (4) và (3). D. (4), (1) và (3).
Câu 2: Những chất trong dãy nào sau đây đều tác dụng được với ancol metylic?
A. HCl; HBr; CH3COOH; NaOH.
B. HCl; CH3COOH; Na; CH3OCH3.
C. CH3COOH; Na; HCl; CaCO3.
D. HCl; HBr; CH3COOH; Na.
Câu 3: Số đồng phân ancol có công thức phân tử C5H12O là
A. 8 đồng phân. B. 5 đồng phân.
C. 14 đồng phân. D. 12 đồng phân.
Câu 4: Nhiệt độ sôi của các hợp chất giảm dần theo thứ tự là:
A. CH3COOH, C2H5OH, C6H6.
B. CH3COOH, C6H6, C2H5OH.
C. C2H5OH, C6H6, CH3COOH.
D. C6H6, CH3COOH, C2H5OH.
Câu 5: Số đồng phân ancol của hợp chất hữu cơ có công thức C4H10O là
A. 2 đồng phân. B. 4 đồng phân.
C. 7 đồng phân. D. 9 đồng phân.
Câu 6: Số đồng phân ancol bậc một của hợp chất hữu cơ có công thức C4H10O là
A. 2 đồng phân. B. 4 đồng phân.
C. 7 đồng phân. D. 9 đồng phân.
Câu 7: Chất nào sau đây có nhiệt độ sôi thấp nhất?
A. CH3OCH3. B. CH3COOH.
C. C2H5OH. D. CH3OH.
Bài tập nâng cao
Câu 8: Một ancol no có công thức thực nghiệm (C2H5O)n. Công thức phân tử của ancol là
A. C2H5O. B. C4H10O2.
C. C6H15O3. D. C8H20O4.
Câu 9: Số công thức cấu tạo ancol bền, có không quá ba nguyên tử cacbon trong phân tử là
A. 3. B. 6.
C. 10. D. 8.
Câu 10: Số hợp chất hữu cơ có công thức C4H10O là
A. 2 chất. B. 4 chất.
C. 7 chất. D. 9 chất.
Câu 11: So sánh và giải thích nhiệt độ sôi, độ tan trong nước của: propan, propan-1-ol và metanol.
Câu 12: Viết công thức cấu tạo và gọi tên tất cả các chất hữu cơ công thức phân tử C4H10O.
Dạng 2: Phản ứng hoá học, nhận biết, điều chế
Kiểu hỏi 1: Phản ứng ancol với kim loại kiềm
Phương pháp giải
Phản ứng xảy ra ở nhóm OH.
Phương trình hoá học:
Tính theo phương trình hoá học.
Công thức tính nhanh:
(trong đó x là số nhóm OH).
Hiện tượng: thoát khí không màu, có thể gây nổ.
Ví dụ: Tính khối lượng glixerol phản ứng, biết thể tích khí thoát ra ở đktc là 560 ml.
Hướng dẫn giải
Phương trình hoá học:
0,0167 0,025 mol
Ví dụ mẫu
Ví dụ 1: Cho 4,600 ml cồn tuyệt đối phản ứng hết với kim loại Na (dư), thu được V lít khí H2 (đktc). Biết khối lượng riêng của ancol etylic nguyên chất bằng 0,800 g/ml. Giá trị của V là
A. 0,336. B. 0,896.
C. 0,448. D. 1,120.
Hướng dẫn giải
Ta có:
Ancol etylic đơn chức:
Chọn B.
Ví dụ 2: Cho 10 ml dung dịch ancol etylic 92o phản ứng hết với kim loại Na dư, thu được V lít khí H2 (đktc). Biết khối lượng riêng của ancol etylic nguyên chất bằng 0,8 g/ml, khối lượng riêng của nước là 1 g/ml. Giá trị của V là
A. 1,120. B. 0,493.
C. 1,792. D. 2,285.
Hướng dẫn giải
Phương trình hoá học:
0,16 0,08 mol
0,044 0,022 mol
Ta có:
Chọn D.
|
Chú ý: Dung dịch rượu chứa C2H5OH và H2O đều phản ứng được với Na sinh ra khí H2. |
Kiểu hỏi 2: Phản ứng riêng của ancol đa chức (poliol), nhận biết poliol
Phương pháp giải
Ancol có ít nhất hai nhóm OH liền kề hoà tan kết tủa Cu(OH)2 (màu xanh nhạt) thành dung dịch phức xanh lam đậm.
Ta luôn có:
Chú ý: Ancol đơn chức hoặc ancol có nhiều nhóm OH không liền kề thì không hoà tan được Cu(OH)2.
Ví dụ: Tính khối lượng Cu(OH)2 bị hoà tan bởi dung dịch chứa 9,2 gam glixerol.
Hướng dẫn giải
Phương trình hoá học:
Ta có:
Ví dụ mẫu
Ví dụ 1: Để phân biệt ancol n-propylic với glixerol người ta dùng thuốc thử là
A. dung dịch brom. B. dung dịch thuốc tím.
C. dung dịch AgNO3. D. Cu(OH)2.
Hướng dẫn giải
Glixerol có nhóm OH liền kề nên có phản ứng đặc trưng với Cu(OH)2 tạo dung dịch phức màu xanh lam đậm.
Ancol n-propylic là ancol đơn chức nên không phản ứng với Cu(OH)2.
Sử dụng thuốc thử là Cu(OH)2.
Chọn D.
Ví dụ 2: Cho các chất sau:
|
(1) HO – CH2 – CH2OH; (3) HOCH2 – CHOH – CH2OH; |
(2) HO – CH2 – CH2 – CH2OH; (4) C2H5 – O – C2H5. |
Những chất hoà tan được Cu(OH)2 là
A. (1), (2) và (3). B. (3) và (2).
C. (4) và (3). D. (1) và (3).
Hướng dẫn giải
Ancol có ít nhất hai nhóm OH kề nhau có khả năng tạo phức tan trong nước có màu xanh lam đậm với Cu(OH)2.
Do đó chất (1) và (3) hoà tan được Cu(OH)2.
Chọn D.
Ví dụ 3: Cho m gam glixerol tác dụng vừa đủ 9,8 gam Cu(OH)2. Giá trị của m là
A. 9,2. B. 18,4.
C. 13,8. D. 23,0.
Hướng dẫn giải
Mà:
Chọn B.
Kiểu hỏi 3: Đun ankanol với H2SO4 đặc
Phương pháp giải
· Tách nước tạo ete:
Nhiệt độ dưới 170oC, cứ hai phân tử ancol đơn chức tách nước tạo một ete.
Phương trình tổng quát:
Chú ý: Với a ancol đơn chức khác nhau tạo ete.
Ví dụ: Đun nóng hỗn hợp metanol và etanol với H2SO4 đặc ở nhiệt độ dưới 170oC.
Hướng dẫn giải
Cách 1: Xảy ra những phản ứng sau:
Do đó thu được 3 ete.
Cách 2: Sử dụng công thức tính nhanh:
Thu được ete
· Tách nước tạo anken:
Nhiệt độ trên 170oC, phân tử ankanol có từ 2C trở lên (trừ metanol) tách nước tạo anken.
Đối với anken đơn chức, phương trình tổng quát:
Quy tắc tách Zaixep: Nhóm OH tách ra cùng với H ở C bên cạnh có bậc cao hơn tạo sản phẩm chính.
Chú ý: Nếu đun ankanol X với H2SO4 đặc tách nước tạo sản phẩm Y, ta có:
Tạo sản phẩm ete.
Tạo sản phẩm anken.
Ví dụ: Đun nóng hỗn hợp metanol và etanol với H2SO4 đặc ở nhiệt độ trên 170oC.
Hướng dẫn giải
Ta có: metanol không tách nước tạo anken.
Chỉ có etanol tách nước tạo anken.
Phương trình hoá học:
Do đó thu được một anken.
Ví dụ mẫu
Ví dụ 1: Đun nóng từ từ hỗn hợp etanol và propanol-2 với xúc tác là axit sunfuric đặc ta có thể thu được tối đa bao nhiêu sản phẩm hữu cơ?
A. 2. B. 3.
C. 4. D. 5.
Hưỡng dẫn giải
Ở nhiệt độ dưới 170oC, hỗn hợp hai ancol đơn chức tách nước tạo ete
Ở nhiệt độ trên 170oC, hỗn hợp ancol đơn chức tách nước tạo anken:
Phương trình hoá học:
Tạo 2 anken.
Do đó, có tối đa 3 + 2 = 5 sản phẩm hữu cơ được tạo thành.
Chọn D.
Ví dụ 2: Cho chất X có công thức cấu tạo như sau:
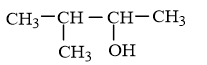
Sản phẩm chính của phản ứng tách một phân tử nước ở nhiệt độ cao là
A. 2-metylbut-1-en. B. 3-metylbut-1-en.
C. 2-metylbut-2-en. D. 3-metylbut-2-en.
Hướng dẫn giải
Quy tắc tách Zaixep: Nhóm OH tách ra cùng với H ở C bên cạnh có bậc cao hơn tạo sản phẩm chính.
Phương trình hoá học tạo ra sản phẩm chính:
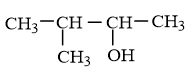
|
|
(sản phẩm chính) |
Do đó, tên gọi của sản phẩm chính là: 2-metylbut-2-en.
Chọn C.
Kiểu hỏi 4: Phản ứng oxi hoá ancol
Phương pháp giải
Phản ứng oxi hoá không hoàn toàn
· Phản ứng oxi hoá ancol bằng CuO:
Ancol bậc I Anđehit
Ancol bậc II Xeton
Ancol bậc III Không phản ứng
· Phản ứng riêng (Phản ứng lên men giấm)
Phản ứng oxi hoá hoàn toàn (phản ứng cháy)
· Đối với ancol no đơn chức, mạch hở:
Phương trình tổng quát:
Ta luôn có:
Ví dụ: Viết phương trình hoá học biểu diễn phản ứng oxi hoá không hoàn toàn (bởi CuO) các đồng phân ancol C3H8O và phản ứng đốt cháy của chúng.
Hướng dẫn giải
Ứng với công thức phân tử là C3H8O có 2 đồng phân ancol là:
CH3 – CH2 – CH2OH
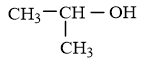
Khi bị oxi hoá bởi CuO.
Phương trình hoá học:
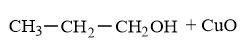
|
|
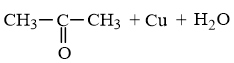
|
|
|
|
|
|
|
||
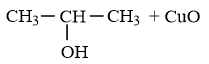 |
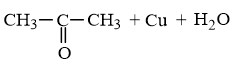 |
|||
Ví dụ mẫu
Ví dụ 1: Cho ancol X (no, đơn chức) có tỉ khối so với heli bằng 15. Biết X tác dụng với CuO, đun nóng thu được xeton. Tên gọi của X là
A. propan-1-ol. B. propan-2-ol.
C. butan-2-ol. D. 2-metylpropan-2-ol.
Hướng dẫn giải
Ancol X là C3H7OH.
X tác dụng với CuO, đun nóng thu được xeton X là ancol bậc II.
X là propan-2-ol: CH3CH(OH)CH3
Phương trình hoá học:
propan-2-ol axeton
Chọn B.
Ví dụ 2: Đốt cháy hoàn toàn 14,8 gam C4H9OH cần vừa đủ V lít (đktc) khí O2. Giá trị của V là
A. 26,88. B. 22,40.
C. 53,76. D. 44,80.
Hướng dẫn giải
Phương trình hoá học:
0,2 1,2 mol
Chọn A.
Ví dụ 3: Đốt cháy hoàn toàn m gam hỗn hợp ancol đơn chức, thuộc cùng dãy đồng đẳng thu được 3,808 lít khí CO2 (đktc) và 5,4 gam H2O. Giá trị của m là
A. 5,42. B. 5,72.
C. 4,72. D. 7,42.
Hướng dẫn giải
Có:
Ta thấy: Hỗn hợp X chứa ba ancol thuộc dãy đồng đẳng ancol no, đơn chức, mạch hở nên
Bảo toàn nguyên tố O:
Bảo toàn khối lượng:
Chọn C.
Kiểu hỏi 5: Tổng hợp, điều chế ancol, etanol
Phương pháp giải
· Tổng hợp ankanol từ anken:
Cộng nước (xúc tác axit, đun nóng) tuân theo quy tắc cộng Mac-côp-nhi-côp.
· Tổng hợp ancol từ dẫn xuất halogen:
Thuỷ phân dẫn xuất halogen no ta được ancol tương ứng.
· Tổng hợp ancol etylic từ phản ứng lên men:
Phản ứng lên men glucozơ hoặc tinh bột ta thu được ancol etylic.
Luôn có:
Ví dụ: Viết phương trình hoá học điều chế trực tiếp ra ancol từ các chất ban đầu sau: propen, isopropyl bromua, glucozơ.
Hướng dẫn giải
Phương trình hoá học:
Ví dụ mẫu
Ví dụ 1: Cho hợp chất X có công thức cấu tạo là:
Sản phẩm chính (theo quy tắc Mac-côp-nhi-côp) của phản ứng giữa X và nước là
A. 2-metylbutan-3-ol. B. 3-metylbutan-2-ol.
C. 3-metylbutan-1-ol. D. 2-metylbutan-4-ol.
Hướng dẫn giải
Quy tắc Mac-côp-nhi-côp: H cộng vào C nối đôi bậc thấp, OH cộng vào C nối đôi bậc cao.
Phương trình hoá học:
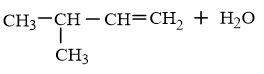
|
|
(sản phẩm chính) |
Tên gọi của sản phẩm chính là: 3-metylbutan-2-ol.
Chọn B.
IV. Bài tập tự luyện dạng 2
Bài tập cơ bản
Câu 1: Để phân biệt ancol etylic với glixerol người ta dùng thuốc thử là
A. dung dịch brom. B. dung dịch thuốc tím.
C. dung dịch AgNO3. D. Cu(OH)2.
Câu 2: Khi khử nước một ancol M với H2SO4 đặc ở 170oC thu được một anken duy nhất. Công thức tổng quát đúng nhất của M là
A. CnH2n+1CH2OH. B. RCH2OH.
C. CnH2n+1OH. D. CnH2n-1CH2OH.
Câu 3: Đun nóng từ từ hỗn hợp methanol, etanol và propanol-2 với xúc tác là axit sunfuric đặc ở trên 170oC ta có thể thu được tối đa bao nhiêu anken?
A. 2. B. 3.
C. 4. D. 5.
Câu 4: Đun nóng từ từ hỗn hợp methanol, etanol và propanol-2 với xúc tác là axit sunfuric đặc ở dưới 170oC ta có thể thu được tối đa bao nhiêu ete?
A. 2. B. 3.
C. 4. D. 6.
Câu 5: Loại nước một ancol X cho hai olefin (anken). Ancol X có thể là
A. ancol isopropylic. B. ancol n-butylic.
C. ancol secbutylic. D. ancol etylic.
Câu 6: Số đồng phân ancol của hợp chất hữu cơ có công thức C4H10O mà khi bị oxi hoá bởi CuO tạo hợp chất anđehit là
A. 2 đồng phân. B. 4 đồng phân.
C. 7 đồng phân. D. 9 đồng phân.
Câu 7: Đồng phân nào của C4H9OH khi tách nước sẽ cho hai olefin là đồng phân của nhau?
A. 2-metylpropan-1-ol. B. 2-metylpropan-2-ol.
C. Butan-1-ol. D. Butan-2-ol.
Bài tập nâng cao
Câu 8: Cho sơ đồ chuyển hoá sau: Hai chất hữu cơ X và Y lần lượt có thể là
A. C2H4 và CH3 – CH2 – OH. B. C2H2 và CH3 – CH2 – OH.
C. C2H4 và C2H2. D. CH3CHO và CH3 – CH2 – OH.
Câu 9: Cho 1,84 gam hỗn hợp gồm ancol etylic và glixerol phản ứng hết với Na dư thu được 0,56 lít H2 (đktc). Thành phần phần trăm về khối lượng ancol etylic và glixerol lần lượt là
A. 27,7% và 72,3%. B. 60,2% và 39,8%.
C. 50,0% và 50,0%. D. 32,0% và 68,0%.
Câu 10: Cho các ancol có công thức cấu tạo như sau:
|
(1) |
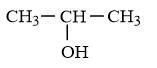
|
(2) |
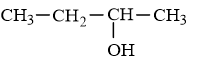
|
|
(3) |
CH3 – CH2 – CH2 – CH2 – OH |
(4) |
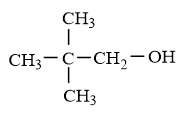
|
Đun nóng một ancol X trong số các ancol có công thức cho trên với H2SO4 đậm đặc ở nhiệt độ thích hợp thu được một anken duy nhất. Các công thức phù hợp với X là
A. (1), (2), (3). B. (1), (2), (3), (4).
C. (1), (2), (4). D. (1), (3).
Câu 11: Viết các phương trình phản ứng (dạng công thức cấu tạo, ghi rõ điều kiện của phản ứng) để thực hiện biến hoá sau:
Etan Eten Etanol Axit axetic Etyl axetat
Câu 12: Trình bày phương pháp hoá học để nhận biết các chất đựng riêng trong các lọ mất nhãn: glixerol, stiren, etanol và hexan.
Dạng 3: Bài toán định lượng và xác định công thức phân tử, công thức cấu tạo của ancol trong dãy đồng đẳng
Bài toán 1: Xác định công thức phân tử, công thức cấu tạo của ancol dựa vào phản ứng cháy
Phương pháp giải
Phản ứng đốt cháy ancol X:
Nếu: Ancol no, mạch hở.
Công thức phân tử tổng quát: CnH2n+2Ox
Phương trình hoá học tổng quát:
Nhận xét:
Bảo toàn nguyên tố C: Số C = n =
Hoặc lập tỉ số dựa vào hệ số phương trình hoá học.
Ví dụ:
Ví dụ: Đốt cháy hoàn toàn a gam một ancol X đơn chức, thu được 11,2 lít khí CO2 ở đktc và 11,25 gam nước. Tìm phân tử của ancol X.
Hướng dẫn giải
Ta có: X là ancol no, đơn chức, mạch hở.
Công thức phân tử tổng quát: CnH2n+2O
Phương trình hoá học:
Do đó:
Bảo toàn nguyên tố C:
Số C = n =
Do đó, công thức phân tử của ancol X là: C4H10O.
Ví dụ mẫu
Ví dụ 1: Đốt cháy hoàn toàn 1,52 gam một ancol X thu được 1,344 lít CO2 (đktc) và 1,44 gam H2O. Công thức phân tử của X là
A. C3H8O. B. C2H6O.
C. C2H6O2. D. C3H8O2.
Hướng dẫn giải
Ta có: Ancol X no, mạch hở.
Gọi công thức của ancol X là CnH2n+2Ox
Số C = n =
Công thức phân tử của X có dạng C3H8Ox (0,02 mol) Loại B và C.
Ta có:
Vậy công thức phân tử của X là C3H8O2.
Chọn D.
Ví dụ 2: Đốt cháy hoàn toàn hai ancol đơn chức X, Y đồng đẳng kế tiếp nhau người ta thấy tỉ số mol CO2 và H2O là 5 : 7. Công thức của X, Y là
A. CH3OH và C2H5OH. B. C2H5OH và C4H9OH.
C. C2H5OH và C3H7OH. D. C4H9OH và C3H7OH.
Hướng dẫn giải
Nhận thấy: Ancol no, đơn chức, mạch hở.
Gọi công thức chung của hai ancol là CxH2x+2O
Phương trình hoá học:
Lập tỉ số
Mặt khác, hai ancol kế tiếp nhau trong dãy đồng đẳng Hai ancol là C2H5OH và C3H7OH.
Chọn C.
Ví dụ 3: Đốt cháy hoàn toàn a gam một ancol X, thu được 8,96 lít khí CO2 ở đktc và 9,0 gam nước. Cho a gam ancol này tác dụng hoàn toàn với Na dư, thu được 4,48 lít khí hiđro (đktc). Tìm công thức phân tử của ancol và cho biết ancol X này có thể hoà tan đồng (II) hiđroxit không?
Hướng dẫn giải
Nhận thấy Ancol no, mạch hở.
Gọi công thức phân tử của ancol là CnH2n+2Ox
Ta có:
Bảo toàn nguyên tố C:
Số C =
Mặt khác: Khi phản ứng với Na.
Số nhóm OH =
Do đó, công thức phân tử của X là C4H10O4.
Công thức cấu tạo của X chỉ có thể là: HOCH2CH(OH)CH(OH)CH2OH.
X hoà tan được đồng (II) hiđroxit vì có nhiều nhóm OH liền kề.
Bài toán 2: Xác định công thức phân tử của ancol dựa vào phản ứng với Na
Phương pháp giải
Ta luôn có:
(trong đó x là số nhóm OH).
Ví dụ: Cho 3,7 gam một ancol đơn chức tác dụng với Na dư thu được 700 cm3 H2 (đo ở 27,3oC và 0,88 atm). Công thức phân tử của ancol là
A. C2H5OH. B. C3H7OH.
C. C4H9OH. D. CH3OH.
Hướng dẫn giải
700 cm3 = 0,7 lít
Ta có:
Ancol đơn chức:
Vậy ancol là C4H9OH.
Chọn C.
Ví dụ mẫu
Ví dụ 1: Cho 1,56 gam hỗn hợp X gồm hai ancol A và B đơn chức, mạch hở kế tiếp nhau trong dãy đồng đẳng (MA < MB) tác dụng hết với 0,92 gam Na, thu được 2,45 gam chất rắn. Ancol B có công thức là
A. C2H5OH. B. C3H7OH.
C. C4H9OH. D. CH3OH.
Hướng dẫn giải
Bảo toàn khối lượng:
Ancol đơn chức:
Vậy hai ancol là C2H5OH và C3H7OH B là C3H7OH.
Chọn B.
Bài toán 3: Xác định công thức phân tử, công thức cấu tạo của ancol dựa vào phản ứng tạo ete hoặc tạo anken
Phương pháp giải
Nếu đun ankanol X với H2SO4 đặc tách nước tạo sản phẩm Y, ta có:
· Tạo sản phẩm anken.
Biểu thức tính tỉ khối:
Ta luôn có:
Bảo toàn khối lượng:
· Tạo sản phẩm ete.
Biểu thức tính tỉ khối:
Ta luôn có:
Bảo toàn khối lượng:
Ví dụ: Đun nóng một ancol đơn chức X với H2SO4 đặc ở nhiệt độ thích hợp thu được hợp chất hữu cơ Y. Biết tỉ khối của Y so với X bằng 0,7. Công thức của X là
A. C2H5OH. B. C3H7OH.
C. C4H9OH. D. CH3OH.
Hướng dẫn giải
Nhận thấy Y là anken.
Phản ứng:
Ta có:
Vậy X là C3H7OH.
Chọn B.
Ví dụ mẫu
Ví dụ 1: Đun nóng một ancol đơn chức X với H2SO4 đặc ở nhiệt độ thích hợp thu được hợp chất hữu cơ Y. Biết tỉ khối của Y so với X bằng 1,4375. Công thức của X là
A. C2H5OH. B. C3H7OH.
C. C4H9OH. D. CH3OH.
Hướng dẫn giải
Nhận thấy Y là ete.
Phản ứng:
Ta có:
Vậy: X là CH3OH.
Chọn D.
Ví dụ 2: Một ancol no, đơn chức, bậc I bị tách một phân tử nước tạo anken X. Cứ 0,525 gam anken X tác dụng vừa đủ với 2 gam brom. Tên IUPAC của ancol này là
A. butan-1-ol. B. pentan-1-ol.
C. etanol. D. propan-1-ol.
Hướng dẫn giải
Ta có:
Mặt khác, ancol tách 1 phân tử nước tạo anken
Do đó, công thức phân tử của ancol là C3H8O.
Công thức cấu tạo: CH3 – CH2 – CH2OH
Tên gọi: propan-1-ol.
Chọn D.
Ví dụ 3: Hỗn hợp X gồm hai ancol đơn chức, đồng đẳng kế tiếp. Đun nóng 16,6 gam X với H2SO4 đặc ở 140oC, thu được 13,9 gam hỗn hợp ete (không có sản phẩm hữu cơ nào khác). Biết các phản ứng xảy ra hoàn toàn. Công thức của hai ancol trong X là
A. C3H5OH và C4H7OH. B. CH3OH và C2H5OH.
C. C3H7OH và C4H9OH. D. C2H5OH và C3H7OH.
Hướng dẫn giải
Bảo toàn khối lượng:
Vậy công thức phân tử của hai ancol là C2H5OH và C3H7OH.
Chọn D.
Bài toán 4: Xác định công thức phân tử, công thức cấu tạo của ancol dựa vào phản ứng oxi hoá bởi CuO
Phương pháp giải
Phản ứng oxi hoá ancol bằng CuO:
Ancol bậc I Anđehit
Ancol bậc II Xeton
Ancol bậc III Không phản ứng
Chú ý:
1. Khối lượng chất rắn giảm chính là khối lượng O bị tách ra khỏi CuO.
2. Số mol hơi và khí sau phản ứng tăng một lượng bằng số mol ancol bị oxi hoá.
Ví dụ: Oxi hoá 3,0 gam một ankanol bằng CuO, khi phản ứng kết thúc (hiệu suất 100%), thấy khối lượng chất rắn giảm so với ban đầu là 0,8 gam. Công thức của ancol bị oxi hoá là
A. CH3OH. B. C3H7OH.
C. C2H5OH. D. C4H9OH.
Hướng dẫn giải
Khối lượng chất rắn giảm bằng khối lượng O bị tách ra khỏi CuO.
Ta có:
Dựa vào đáp án ta thấy ancol là ancol đơn chức nên ta có:
Do đó:
Công thức của ancol là C3H7OH.
Chọn B.
Ví dụ mẫu
Ví dụ 1: Cho 11,28 gam hỗn hợp X gồm hai ancol đơn chức, bậc I là đồng đẳng kế tiếp qua CuO dư, nung nóng (phản ứng hoàn toàn). Sau phản ứng thấy khối lượng chất rắn giảm 4,8 gam. Cho hỗn hợp sản phẩm tác dụng với AgNO3 dư trong NH3, đun nóng thu được m gam kết tủa. Giá trị của m là
A. 97,20. B. 43,20.
C. 64,80. D. 103,68.
Hướng dẫn giải
Ta có:
Ancol đơn chức nên ta có:
Hai ancol là CH3OH (a mol) và C2H5OH (b mol).
Ta có hệ phương trình:
Vậy hai anđehit tương ứng là HCHO (0,18 mol) và CH3CHO (0,12 mol).
Lại có:
0,18 0,72 mol
0,12 0,24 mol
Chọn D.
|
Chú ý:
|
Bài toán 5: Định lượng liên quan đến phản ứng lên men tinh bột, glucozơ hoặc lên men giấm
Phương pháp giải
Sơ đồ chuyển hoá
Tinh bột Glucozơ Ancol etylic Axit axetic
Luôn có:
Chú ý 1: Với các bài khối lượng lớn thì ta cần sử dụng tỉ lệ khối lượng.
Chú ý 2: Với các bài có hiệu suất:
1. Tính hiệu suất
Hiệu suất tính theo chất đầu:
Hiệu suất tính theo chất sản phẩm:
thường đề bài cho, là tính theo phương trình hoá học.
2. Tính lượng chất ban đầu và chất sản phẩm
Chú ý 3: Công thức tính độ rượu:
Ví dụ: Bằng phương pháp lên men rượu từ gạo chứa 80% tinh bột ta thu được 0,1 lít ancol etylic (có khối lượng riêng 0,8 gam/ml). Biết hiệu suất lên men của cả quá trình là 80%. Xác định khối lượng gạo phải dùng?
Hướng dẫn giải
Nếu H = 100% sơ đồ chuyển hoá (coi n = 1):
0,87 1.74 mol
Khối lượng tinh bột phản ứng là:
Khối lượng tinh bột phải dùng là:
Khối lượng gạo là:
Ví dụ mẫu
Ví dụ 1: Thuỷ phân hoàn toàn m gam tinh bột, thu lấy toàn bộ lượng glucozơ đem lên men thành ancol etylic với hiệu suất 50%, thu được V lít (đktc) khí CO2. Hấp thụ hết lượng CO2 trên vào nước vôi trong dư thu được 40 gam kết tủa. Giá trị của m là
A. 72,0. B. 32,4.
C. 36,0. D. 64,8.
Hướng dẫn giải
Hấp thụ CO2 vào nước vôi trong dư:
Nếu H = 100%:
Coi n = 1, ta có sơ đồ:
0,2 0,4 mol
Với H = 50% ta có:
Chọn D.
Ví dụ 2: Ancol etylic được điều chế từ tinh bột bằng phương pháp lên men với hiệu suất toàn bộ quá trình là 90%. Hấp thụ toàn bộ lượng CO2 sinh ra khi lên men m gam tinh bột vào nước vôi trong dư, thu được 330 gam kết tủa và dung dịch X. Biết khối lượng X giảm đi so với khối lượng nước vôi trong ban đầu là 132 gam. Giá trị của m là
A. 486. B. 297.
C. 405. D. 324.
Hướng dẫn giải
Hấp thụ lượng CO2 vào nước vôi trong dư:
Nếu H = 100%:
Coi n = 1, ta có sơ đồ:
(C6H10O5) C6H12O6 2C2H5OH + 2CO2
2,25 4,5 mol
Với H = 90% ta có:
Chọn C.
V. Bài tập tự luyện dạng 3
Bài tập cơ bản
Câu 1: Đốt cháy 1,48 gam một hỗn hợp hai ancol no, đơn chức kế tiếp nhau trong dãy đồng đẳng, cần 2,016 lít O2 (đktc). Công thức hai ancol đó là
A. CH3OH và C2H5OH. B. C2H5OH và C4H9OH.
C. C2H5OH và C3H7OH. D. C4H9OH và C3H7OH.
Câu 2: Đốt cháy hoàn toàn hai ancol đơn chức X, Y đồng đẳng kế tiếp nhau người ta thấy tỉ số mol CO2 và H2O là 3 : 5. Công thức của X, Y là
A. CH3OH và C2H5OH. B. C2H5OH và C4H9OH.
C. C2H5OH và C3H7OH. D. C4H9OH và C3H7OH.
Câu 3: X là đồng đẳng của ancol etylic có tỉ khối hơi so với nitơ bằng 2,643. Đun các đồng phân của X với H2SO4 đặc ở dưới 170oC, thu được số ete là
A. 6. B. 2.
C. 3. D. 4.
Câu 4: Một ancol no, đơn chức, bậc I bị tách một phân tử nước tạo anken X duy nhất. Cứ 1,12 gam anken X tác dụng vừa đủ với 3,2 gam brom. Tên gọi của ancol là
A. butan-1-ol. B. butan-2-ol.
C. etanol. D. propan-1-ol.
Câu 5: Đun 1,34 gam hai ancol (H2SO4 đặc) thu được hai anken là đồng đẳng kế tiếp nhau. Đốt hỗn hợp hai anken cần 2,13815 lít O2 (25oC; 1,2 atm). Công thức của hai ancol là
A. CH3OH và C3H7OH. B. CH3OH và C2H5OH.
C. C2H5OH và C3H5OH. D. C3H7OH và C4H9OH.
Câu 6: Cho 5,3 gam hỗn hợp hai ankanol đồng đẳng liên tiếp tác dụng với natri dư thu được 1,12 lít H2 (đktc). Công thức của hai ankanol trên là
A. CH3OH và C2H5OH. B. C2H5OH và C3H7OH.
C. C3H7OH và C4H9OH. D. C4H9OH và C5H11OH.
Câu 7: Cho 1,66 gam hỗn hợp gồm ancol etylic và ancol n-propylic phản ứng hoàn toàn với CuO dư, kết thúc phản ứng, thấy khối lượng chất rắn giảm 0,48 gam. Thành phần phần trăm về khối lượng các ancol trong hỗn hợp là
A. 27,7% và 72,3%. B. 60,2% và 39,8%.
C. 40,0% và 60,0%. D. 32,0% và 68,0%.
Bài tập nâng cao
Câu 8: X là một ancol no, đa chức, mạch hở có số nhóm OH nhỏ hơn 5. Cứ 7,6 gam ancol X phản ứng hết với natri cho 2,24 lít khí (đo ở đktc). Công thức hoá học của X là
A. C4H7(OH)3. B. C2H4(OH)2.
C. C3H6(OH)2. D. C3H5(OH)3.
Câu 9: Đun nóng một hỗn hợp gồm hai ancol no, đơn chức, kế tiếp trong dãy đồng đẳng với H2SO4 đặc ở 140oC thu được 2,16 gam nước và 7,2 gam hỗn hợp ba ete. Biết ba ete có số mol bằng nhau (phản ứng hoàn toàn). Công thức của hai ancol là
A. CH3OH và C2H5OH. B. C2H5OH và C3H7OH.
C. C3H7OH và C4H9OH. D. CH3OH và C3H7OH.
Câu 10: Đun nóng hỗn hợp hai ancol mạch hở với H2SO4 đặc ta được các ete. Lấy X là một trong các ete đó đốt cháy hoàn toàn được tỉ lệ mol của X, oxi cần dùng, cacbonic và nước tạo ra lần lượt là 0,25 : 1,375 : 1 : 1. Công thức hai ancol trên là
A. C2H5OH và CH3OH. B. C3H7OH và CH2 = CH – CH2 – OH.
C. C2H5OH và CH2 = CH – OH. D. CH3OH và CH2 = CH – CH2OH.
Câu 11: Đun nóng một hỗn hợp gồm hai ancol no đơn chức kế tiếp trong dãy đồng đẳng với H2SO4 đặc ở 140oC thu được 9,0 gam nước và 30,0 gam hỗn hợp ba ete. Biết ba ete có số mol bằng nhau (phản ứng hoàn toàn). Tính thành phần phần trăm khối lượng mỗi ancol trong hỗn hợp ban đầu?
Câu 12: Tính lượng glucozơ cần để điều chế 1 lít dung dịch rượu etylic 40o. Biết khối lượng riêng của ancol etylic nguyên chất 0,8 gam/ml và hiệu suất phản ứng là 80%.
ĐÁP ÁN BÀI TẬP TỰ LUYỆN
Dạng 1: Cấu tạo, đồng phân, danh pháp, tính chất vật lí, ứng dụng
|
1-A |
2-D |
3-A |
4-A |
5-B |
6-A |
7-A |
8-B |
9-D |
10-C |
Câu 11: Xem phần phương pháp giải dạng 1.
Câu 12: Có 4 công thức cấu tạo dạng ancol và 3 công thức cấu tạo dạng ete. Gọi tên danh pháp IUPAC hoặc danh pháp thông thường.
Dạng 2: Phản ứng hoá học, nhận biết, điều chế
|
1-D |
2-A |
3-A |
4-D |
5-C |
6-A |
7-D |
8-A |
9-C |
10-D |
Câu 11: Dùng các phản ứng: tách hiđro cho etan, cộng nước cho eten, lên men giấm etanol, este hoá axit axetic và etanol.
Câu 12: Dùng các thuốc thử: đồng (II) hiđroxit, nước brom và natri kim loại.
Dạng 3: Bài toán định lượng và xác định công thức phân tử, công thức cấu tạo của ancol trong dãy đồng đẳng
|
1-A |
2-A |
3-C |
4-A |
5-D |
6-B |
7-A |
8-C |
9-A |
10-D |
Câu 11: 41% và 59%.
Câu 12: 782,6 gam.