Tailieumoi.vn sưu tầm và biên soạn chuyên đề Phenol gồm đầy đủ lý thuyết, các dạng bài tập chọn lọc và ví dụ minh họa từ cơ bản đến nâng cao giúp học sinh ôn luyện kiến thức, biết cách làm bài tập môn Hóa học 11.
Chuyên đề Phenol
BÀI 23: PHENOL
I. LÍ THUYẾT TRỌNG TÂM
1. Cấu tạo, tính chất vật lí
Đặc điểm cấu tạo phenol: Có nhóm OH gắn trực tiếp với C của vòng benzen.
|
Ví dụ: |
|
Chú ý:
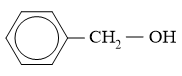 không phải là phenol mà là ancol thơm, vì nhóm OH không gắn trực tiếp với C của nhân thơm.
không phải là phenol mà là ancol thơm, vì nhóm OH không gắn trực tiếp với C của nhân thơm.
2. Tính chất
Phenol ít tan trong nước lạnh, tan nhiều trong nước nóng và etanol, có tính gây bỏng, bị oxi hoá bởi không khí.
Phản ứng thế H ở nhóm OH: tính axit, tác dụng với natri, natri hiđroxit (giải thích: do nhóm OH bị phân cực mạnh hơn nhờ tính hút e của vòng thơm).
Ví dụ: Phản ứng giữa phenol với Na, với NaOH, xảy ra ở nhóm OH, H trong nhóm OH dễ bị thế hơn so với ancol.
Phản ứng thế H ở vòng benzen: dễ dàng hơn các aren (tác dụng với nước brom), (giải thích do nhóm OH đẩy e mạnh vào vòng benzen và định hướng thế H ở vị trí ortho và para).
Ví dụ: Phản ứng giữa phenol với nước brom tạo kết tủa trắng; với dung dịch HNO3 đặc, tạo axit picric, chất kết tủa vàng cam. Phản ứng ưu tiên thế H trong vòng benzen ở vị trí ortho và para.
Phản ứng cộng H2 vào vòng benzen tạo ancol vòng no, tác dụng với anhiđric axit (RCOO)2O tạo este RCOOC6H5.
Kết luận: Nhờ có sự ảnh hưởng qua lại giữa các nhóm OH và vòng benzen trong phân tử phenol làm cho phenol có tính axit mạnh hơn ancol (H ở nhóm OH linh động hơn) và dễ tham gia phản ứng thế H ở vị trí o-, p- hơn aren.
3. Ứng dụng
Phenol là nguyên liệu để sản xuất chất dẻo, thuốc trừ sâu, dược phẩm…
II. CÁC DẠNG BÀI TẬP
Dạng 1: Công thức cấu tạo, tính chất vật lí, ứng dụng
Kiểu hỏi 1: Số đồng phân cấu tạo của phenol
Phương pháp giải
Phenol: có nhóm OH gắn ở C thơm.
· Khi vòng benzen có hai nhóm thế sẽ có đồng phân vị trí o-, p-, m-.
· Phenol có đồng phân khác chức với rượu thơm, ete thơm.
Ví dụ: Ứng với công thức C7H8O có bao nhiêu đồng phân phenol?
Hướng dẫn giải
Ứng với công thức C7H8O có ba đồng phân phenol ở các vị trí o-, p-, m- lần lượt là
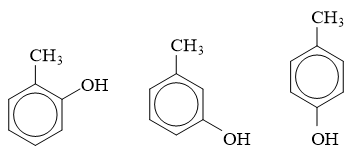
Ví dụ mẫu
Ví dụ 1: Chất X có công thức phân tử C7H8O, có số đồng phân chứa nhân thơm là
A. 6. B. 5.
C. 4. D. 3.
Hướng dẫn giải
Cấu tạo nhân thơm có 6C.
Đồng phân dạng phenol: CH3 – C6H4 – OH: o-, m-, p-
Đồng phân dạng ancol: C6H5 – CH2 – OH.
Đồng phân dạng ete: C6H5 – O – CH3.
Có tất cả 5 đồng phân của X.
Chọn B.
Kiểu hỏi 2: Tính chất vật lí, ứng dụng của phenol
Phương pháp giải
Nhóm OH của phenol phân cực hơn trong ancol và do đó có nhiệt độ sôi cao hơn, độ tan trong nước thì thấp hơn etanol.
Ví dụ: Nhiệt độ sôi của
C6H5 – OH > C2H5 – OH > C2H5 – O – C2H5
Phenol: là nguyên liệu để sản xuất chất dẻo, thuốc trừ sâu, dược phẩm…
Ví dụ: Ứng dụng nào sau đây không phải của phenol?
A. Nguyên liệu sản xuất chất dẻo.
B. Nguyên liệu sản xuất dược phẩm.
C. Nguyên liệu sản xuất thuốc trừ sâu.
D. Nguyên liệu sản xuất cao su.
Hướng dẫn giải
Phenol không được dùng làm nguyên liệu sản xuất cao su.
Chọn D.
Ví dụ mẫu
Ví dụ 1: Cho 0,1 gam phenol (C6H5OH) vào ống nghiệm chứa 2 ml nước cất ở nhiệt độ 20oC, lắc nhẹ, sau đó để yên. Hỗn hợp thu được ở dạng nào sau đây?
A. dung dịch B. huyền phù.
C. nhũ tương. D. gel.
Hướng dẫn giải
Phenol ít tan trong nước lạnh, do đó không tạo thành dung dịch. Phenol không phải là một chất lỏng ở điều kiện thường nên không tạo thành nhũ tương. Phenol và nước không tạo gel. Như vậy phenol dạng rắn lơ lửng trong nước tạo ra huyền phù.
Chọn B.
Ví dụ 2: Trong thực tế, phenol được dùng để sản xuất:
A. poli(phenol-fomanđehit), chất diệt cỏ 2,4-D và axit picric.
B. nhựa rezit, chất diệt cỏ 2,4-D và thuốc nổ TNT.
C. nhựa rezol, nhựa rezit và thuốc trừ sâu 666.
D. nhựa poli(vinyl clorua), nhựa novolac và chất diệt cỏ 2,4-D.
Hướng dẫn giải
Phenol không dùng để sản xuất thuốc nổ TNT, thuốc trừ sâu 666 và nhựa novolac.
Chọn A
III. Bài tập tự luyện dạng 1
Câu 1: Phát biểu nào sau đây sai khi nói về phenol?
A. Phenol có nhóm OH trong phân tử nên có tính chất hoá học giống ancol.
B. Phenol có tính axit nên phenol tan được trong dung dịch kiềm.
C. Tính axit của phenol yếu hơn axit cacbonic nhưng mạnh hơn ancol.
D. Dung dịch phenol trong nước không làm quỳ tím đổi màu sang đỏ.
Câu 2: Phenol đều tác dụng với cặp chất nào sau đây?
A. HCl và Na. B. Na và KOH.
C. NaOH và HCl. D. Na và Na2CO3.
Câu 3: Cho các chất có công thức cấu tạo:
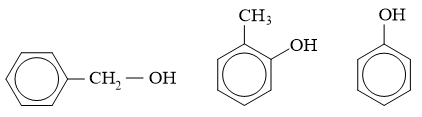
(1) (2) (3)
Chất thuộc loại phenol là
A. (1) và (2). B. (2) và (3).
C. (1) và (3). D. Cả (1), (2) và (3).
Câu 4: Ứng dụng nào sau đây không phải của phenol?
A. Nguyên liệu để sản xuất nhựa rezit.
B. Nguyên liệu sản xuất thuốc nổ.
C. Nguyên liệu sản xuất thuốc giảm đau, hạ sốt.
D. Nguyên liệu để sản xuất keo dán tổng hợp.
Câu 5: Cho các chất: (1) axit axetic; (2) ancol etylic; (3) phenol; (4) axit cacbonic. Tính axit tăng dần theo thứ tự
A. (1) < (3) < (2) < (4). B. (3) < (1) < (2) < (4).
C. (1) < (2) < (3) < (4). D. (2) < (3) < (4) < (1).
Dạng 2: Phản ứng hoá học, nhận biết
Kiểu hỏi 1: Các chất nào phản ứng/ không phản ứng với phenol
Phương pháp giải
Phenol (C6H5OH) tác dụng được với kim loại kiềm, bazơ kiềm, dung dịch brom và HNO3 đặc (xúc tác H2SO4 đặc).
Ví dụ: Cho các chất: etanol, nước brom, kim loại kali, kali hiđroxit. Số chất tác dụng được với phenol ở điều kiện thường là
A. 1. B. 2.
C. 3. D. 4.
Hướng dẫn giải
Các chất tác dụng được với phenol ở điều kiện thường là brom, kim loại kali, kali hiđroxit.
Chọn C.
Ví dụ mẫu
Ví dụ 1: Phenol (C6H5OH) có thể tác dụng với tất cả các chất trong dãy nào sau đây?
A. NaOH, HNO3, HCl, Na. B. Na2CO3, Br2, Na, NaOH.
C. HNO3, Br2, Na, NaOH. D. Br2, HBr, Na, KOH.
Hướng dẫn giải
Phenol (C6H5OH) tác dụng được với kim loại kiềm, bazơ kiềm, dung dịch brom và HNO3 đặc (xúc tác H2SO4 đặc).
Do đó, phenol có thể tác dụng được với: HNO3, Br2, Na, NaOH.
Chọn C.
Ví dụ 2: Khi thổi khí cacbonic vào dung dịch muối natri phenolat thấy dung dịch bị vẩn đục là do
A. phenol phản ứng cộng với brom tạo kết tủa.
B. phenol có tính axit yếu nên bị axit cacbonic đẩy ra khỏi muối tạo thành chất không tan trong nước ở nhiệt độ phòng.
C. phenol dễ cho phản ứng thế với CO2 ở các vị trí ortho và para tạo chất không tan.
D. CO2 kết hợp với phenol tách ra thành chất kết tủa.
Hướng dẫn giải
Phenol có tính axit yếu hơn cả H2CO3 (nấc 1) nên có bị đẩy ra khỏi muối phenolat, tạo phenol rất ít tan trong nước lạnh, làm dung dịch bị đục.
Phương trình hoá học:
Chọn B.
Kiểu hỏi 2: Nhận biết, hiện tượng phản ứng của phenol
Phương pháp giải
· Nhận biết phenol: Dùng phản ứng với nước brom.
Hiện tượng: Kết tủa trắng.
Phương trình hoá học:
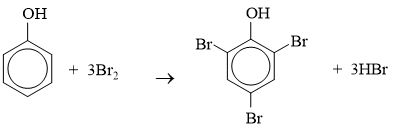
Ví dụ: Mô tả hiện tượng khi cho nước brom vào phenol.
Hướng dẫn giải
Dung dịch phenol ban đầu không màu, sau khi cho nước brom vào thấy xuất hiện kết tủa trắng.
Phương trình hoá học:
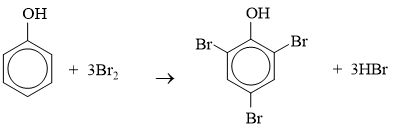
Ví dụ mẫu
Ví dụ 1: Hoá chất duy nhất dùng để nhận biết ba chất lỏng đựng riêng biệt trong lọ mất nhãn: phenol, stiren và ancol etylic là
A. natri kim loại. B. quỳ tím.
C. dung dịch NaOH. D. dung dịch brom.
Hướng dẫn giải
Nhận xét:
· Na: nhận ra chất có nhóm OH (tạo khí hiđro).
· Quỳ tím: nhận biết axit, bazơ.
· NaOH: nhận biết các ion kim loại (tạo kết tủa), muối amoni (tạo khí mùi khai).
· Dung dịch brom (màu vàng nâu): nhận biết được gốc không no (nhạt màu dung dịch), phenol (tạo kết tủa trắng), ancol no không phản ứng.
Do đó, hoá chất được sử dụng để nhận biết là dung dịch brom.
Chọn D.
IV. Bài tập tự luyện dạng 2
Bài tập cơ bản
Câu 1: Cho sơ đồ chuyển hoá sau: Toluen A1 A2 A3.
Biết A1, A2, A3 là các sản phẩm hữu cơ; A1 là hợp chất có cấu tạo para. Công thức A1, A2, A3 lần lượt là
A. p-CH3 – C6H5Br, C6H5ONa, C6H5OH.
B. p-CH3 – C6H4Br, p-CH3 – C6H4ONa, p-CH3 – C6H4OH.
C. p-CH3 – C6H4Br, o-CH3 – C6H4ONa, o-CH3 – C6H4OH.
D. p-CH3 – C6H4Br, p-CH3 – C6H4OH, C6H5OH.
Câu 2: Khi cho phenol tác dụng với nước brom, hiện tượng xảy ra là
A. mất màu nâu đỏ của nước brom.
B. tạo kết tủa đỏ gạch.
C. tạo kết tủa trắng.
D. tạo kết tủa xám bạc.
Câu 3: Hoá chất duy nhất dùng để nhận biết ba chất lỏng đựng riêng biệt trong ba bình mất nhãn: phenol, stiren và ancol benzylic là
A. natri kim loại. B. quỳ tím.
C. dung dịch NaOH. D. dung dịch brom.
Câu 4: Phản ứng nào sau đây chứng minh phenol có tính axit yếu hơn axit cacbonic và mạnh hơn ancol?
A.
B.
C.
D. Cả hai phản ứng A và C
Câu 5: Dùng phản ứng hoá học nào để chứng minh khả năng thế nguyên tử hiđro trong nhân thơm của phenol dễ hơn trong aren?
A. .
B. .
C. .
D. Cả hai phản ứng A và C.
Câu 6: Kết quả thí nghiệm của các chất lỏng X, Y, Z, T với thuốc thử được ghi ở bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Quỳ tím |
Chuyển màu hồng |
|
Y |
Cu(OH)2 |
Tan thành dung dịch xanh lam |
|
Z |
Nước brom |
Dung dịch brom nhạt màu |
|
T |
Nước brom |
Kết tủa trắng |
Các dung dịch X, Y, Z, T lần lượt là
A. Axit axetic, glixerol, stiren, phenol.
B. Axit axetic, stiren, glixerol, phenol.
C. Axit axetic, etanol, glixerol, stiren.
. Phenol, glixerol, ancol benzylic, benzen.
Câu 7: C7H8O có số đồng phân chứa nhân thơm và có thể tác dụng với NaOH là
A. 6. B. 5.
C. 4. D. 3.
Câu 8: Thực hiện bốn phản ứng trong bốn ống nghiệm sau:
|
(1) Dung dịch NaOH + phenol. (3) Phenol + dung dịch brom. |
(2) Natri phenolat + dung dịch HCl. (4) Phenol + natri kim loại. |
Các trường hợp phản ứng tạo kết tủa là:
A. (3), (4). B. (2), (3).
C. (1), (2), (3). D. (1), (4).
Câu 9: Cho các hợp chất thơm sau: C6H5CH3, C6H5OH, p-CH3C6H4OH, p-HOC6H4OH, C6H5CH2OH. Số chất vừa tác dụng được với Na, vừa tác dụng được với NaOH là
A. 2. B. 5.
C. 4. D. 3.
Câu 10: Cho các chất có công thức cấu tạo:
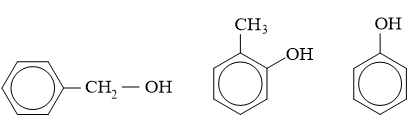
(1) (2) (3)
Chất vừa tác dụng được với Na, vừa tác dụng được với NaOH là
A. (1) và (2). B. (2) và (3).
C. (1) và (3). D. cả (1), (2) và (3).
Câu 11: Để nhận biết hai chất lỏng đựng riêng biệt trong hai lọ mất nhãn: phenol và glixerol, người ta không sử dụng hoá chất nào sau đây?
A. Natri kim loại. B. Cu(OH)2.
C. Dung dịch HNO3 đặc. D. Dung dịch brom.
Bài tập nâng cao
Câu 12: Hợp chất thơm X có công thức HO – CH2 – C6H4 – OH. Một phân tử X có thể tác dụng với
A. một nguyên tử Na và hai phân tử NaOH.
B. hai nguyên tử Na và một phân tử NaOH.
C. hai nguyên tử Na và hai phân tử NaOH.
D. một nguyên tử Na và một phân tử NaOH.
Câu 13: Cho a mol hợp chất hữu cơ X có công thức phân tử C7H8O2 tác dụng với natri dư thu được a mol khí H2 (đktc). Mặt khác, a mol X nói trên tác dụng vừa đủ với a mol NaOH. Trong phân tử X có thể chứa
A. một nhóm cacboxyl – COOH liên kết với nhân thơm.
B. một nhóm – CH2OH và một nhóm – OH liên kết với nhân thơm.
C. hai nhóm – OH liên kết trực tiếp với nhân thơm.
D. một nhóm – O – CH2OH liên kết với nhân thơm.
Câu 14: Từ benzen và các chất cần thiết, người ta có thể tổng hợp thuốc giảm đau, hạ sốt qua các bước sau:
Bước 1: Từ benzen tổng hợp cumen, phenol, axit salixylic (axit o-hiđroxibenzoic).
Bước 2: Từ axit salixylic điều chế metyl salixylat (một loại thuốc giảm đau, chống viêm).
Bước 3: Từ axit salixylic điều chế axit axetyl salixylic (một loại thuốc hạ sốt hay aspirin).
Dùng công thức cấu tạo viết sơ đồ tổng hợp nói trên.
Dạng 3: Bài toán liên quan đến lượng phenol trong phản ứng
Bài toán 1: Phenol phản ứng với kim loại kiềm, bazơ kiềm
Phương pháp giải
· Phenol phản ứng với dung dịch kiềm
Theo phương trình:
· Phenol tác dụng với kim loại kiềm
Phương trình hoá học:
Theo phương trình:
Ví dụ: Cho m gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với natri (dư), thu được 2,24 lít khí H2 (đktc). Mặt khác, để phản ứng hoàn toàn với m gam X cần 100 ml dung dịch NaOH 1M. Giá trị của m là
A. 7,00. B. 21,00.
C. 14,00. D. 10,50.
Hướng dẫn giải
X phản ứng với dung dịch NaOH:
Chỉ có phenol phản ứng được với dung dịch NaOH nên ta có:
X phản ứng với Na:
Phương trình hoá học:
0,1 0,05 mol
0,1 0,05 mol
Chọn C.
Ví dụ mẫu
Ví dụ 1: Cho m gam phenol C6H5OH tác dụng với natri dư thấy thoát ra 0,56 lít khí H2 (đktc). Khối lượng phenol cần dùng là
A. 4,7 gam. B. 9,4 gam.
C. 7,4 gam. D. 4,9 gam.
Hướng dẫn giải
Phương trình hoá học:
0,05 0,025 mol
Chọn A.
Ví dụ 2: Cho m gam hỗn hợp gồm phenol và glixerol tác dụng với Na dư, thu được 7,84 lít khí (đktc). Cũng m gam hỗn hợp trên tác dụng vừa hết với 100 ml NaOH 1M. Nếu cho m gam hỗn hợp trên tác dụng với dd nước brom dư, thu được a gam kết tủa.
a) Viết các phương trình hoá học xảy ra.
b) Tính giá trị m và a?
Hướng dẫn giải
a) Phương trình hoá học:
(1)
(2)
(3)
(4)
Không phản ứng
Không phản ứng
b) Ta có:
Theo phương trình hoá học (3):
Do đó:
Theo phương trình hoá học (1) và (2):
Khối lượng của hỗn hợp ban đầu là:
Vậy
Bài toán 2: Phenol phản ứng với dung dịch brom
Phương pháp giải
· Phenol phản ứng với dung dịch Br2:
Theo phương trình:
· Phenol phản ứng với dung dịch HNO3 tương tự với Br2.
Ví dụ: Cho 4,7 gam phenol tác dụng với nước Br2 dư, thu được m gam kết tủa. Giá trị của m là
A. 16,55. B. 15,56.
C. 15,65. D. 16,25.
Hướng dẫn giải
Phương trình hoá học:
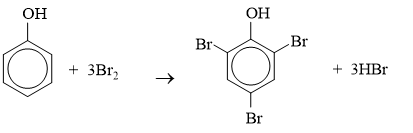
Chọn A.
Ví dụ mẫu
Ví dụ 1: Cho nước brom dư vào dung dịch phenol thu được 6,62 gam kết tủa trắng (phản ứng hoàn toàn). Khối lượng phenol có trong dung dịch là
A. 1,88 gam. B. 18,8 gam.
C. 37,6 gam. D. 3,76 gam.
Hướng dẫn giải
Phương trình hoá học:
0,02 0,02 mol
Chọn A
V. Bài tập tự luyện dạng 3
Bài tập cơ bản
Câu 1: Cho m gam hỗn hợp gồm phenol và etanol tác dụng với Na dư, thu được 33,6 lít khí (đktc). Nếu cho m gam hỗn hợp trên tác dụng với dung dịch nước brom vừa đủ, thu được 19,86 gam kết tủa trắng 2,4,6-tribromphenol. Giá trị của m là
A. 5,64. B. 19,86.
C. 11,04. D. 16,68.
Câu 2: Cho 18,6 gam hỗn hợp gồm phenol và glixerol tác dụng với Na dư, thu được 4,48 lít khí (đktc). Nếu hỗn hợp trên tác dụng với dung dịch nước brom vừa đủ, thu được m gam kết tủa trắng 2,4,6-tribromphenol. Giá trị của m là
A. 33,10. B. 19,86.
C. 11,04. D. 16,55.
Câu 3: Cho 4,7 gam phenol C6H5OH tác dụng với natri dư, kết thúc phản ứng thu được V lít khí H2 (đktc). Giá trị của V là
A. 4,700. B. 9,400.
C. 0,560. D. 0,224.
Câu 4: Cho nước brom dư vào dung dịch phenol thu được 6,62 gam kết tủa trắng (phản ứng hoàn toàn). Khối lượng brom đã phản ứng là
A. 9,6 gam. B. 18,8 gam.
C. 7,6 gam. D. 3,2 gam.
Bài tập nâng cao
Câu 5: Cho 47 gam phenol tác dụng với hỗn hợp gồm 200 gam HNO3 68% và 250 gam H2SO4 96% tạo axit picric (phản ứng hoàn toàn). Nồng độ phần trăm HNO3 còn dư sau khi tách kết tủa axit picric ra là
A. 10,850%. B. 1,085%.
C. 5,425%. D. 21,700%.
Câu 6: Axit picric (2,4,6-trinitrophenol) là một hoá chất dùng làm thuốc nổ nó có thể điều chế từ benzen và các chất vô cơ cần thiết khác, trong đó có axit nitric đặc. Tính khối lượng benzen và thể tích dung dịch HNO3 68% (D = 1,52 g/ml) cần dùng để tổng hợp 12 kg axit picric. Giả sử hiệu suất của quá trình điều chế là 85%.
ĐÁP ÁN BÀI TẬP TỰ LUYỆN
Dạng 1: Công thức cấu tạo, tính chất vật lí, ứng dụng
|
1-A |
2-B |
3-B |
4-D |
5-D |
Dạng 2: Phản ứng hoá học, nhận biết
|
1-B |
2-C |
3-D |
4-D |
5-B |
6-A |
7-D |
8-B |
9-D |
10-B |
|
11-A |
12-B |
13-B |
|
|
|
|
|
|
|
Câu 14:
a.
(axit salixylic)
b.
(metyl salixylat)
c.
(axit axetyl salixylic)
Dạng 3: Bài toán liên quan đến lượng phenol trong phản ứng
|
1-D |
2-A |
3-C |
4-C |
5-A |
Câu 6: 4,81 kg benzen và 11,27 lít dung dịch HNO3 68%.