Với tóm tắt lý thuyết Hóa học lớp 9 Etilen hay, chi tiết cùng với 22 câu hỏi trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học lớp 9.
Hóa học 9 Bài 37: Etilen
A. Lý thuyết Etilen
Etilen có công thức phân tử: C2H4
Phân tử khối: 28
Etilen là chất khí, không màu, không mùi, nhẹ hơn không khí 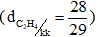
Trong phân tử etilen mỗi nguyên tử cacbon liên kết với 2 nguyên tử H, hai hóa trị còn lại dùng để liên kết hai nguyên tử cacbon với nhau.
Etilen có công thức cấu tạo: 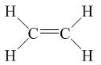
Như vậy, trong phân tử etilen C2H4, có một liên kết đôi giữa hai nguyên tử cacbon.
Chú ý: Trong liên kết đôi có một liên kết kém bền. Liên kêt này dễ đứt ra trong các phản ứng hóa học.
Hình 1: Mô hình phân tử etilen dạng rỗng và dạng đặc.
1. Tác dụng với oxi:
Khi đốt khí etilen cháy tạo thành khí CO2, hơi nước và tỏa nhiều nhiệt.
Phương trình hóa học:
Nhận xét: Khi đốt cháy khí etilen thu được số mol CO2 bằng số mol nước.
2. Tác dụng với dung dịch brom
Hình 2: Minh họa thí nghiệm etilen tác dụng với dung dịch brom.
Phương trình hóa học:
Viết gọn: CH2 = CH2 + Br2 → Br – CH2 – CH2 – Br
Nhận xét:
– Liên kết kém bền trong liên kết đôi bị đứt ra và mỗi phân tử etilen đã kết hợp thêm một phân tử brom.
– Phản ứng trên gọi là phản ứng cộng. Ngoài brom, trong những điều kiện thích hợp etilen có thể tham gia phản ứng cộng với Cl2, H2, HBr…
– Các chất có liên kết đôi như etilen dễ tham gia phản ứng cộng.
3. Các phân tử etilen kết hợp với nhau
Ở điều kiện thích hợp (nhiệt độ, áp suất, xúc tác) các phân tử etilen kết hợp với nhau tạo ra chất có kích thước và khối lượng rất lớn gọi là poli etilen (PE).
Phương trình hóa học:
Chú ý:
- Phản ứng trên là phản ứng trùng hợp.
- Poli etilen là chất không tan trong nước, không độc, là nguồn nguyên liệu quan trọng trong công nghiệp chất dẻo.
– Etilen dùng để điều chế axit axetic, rượu etylic, đicloetan, polime (PE, PVC)…
– Etilen dùng kích thích quả mau chín.
B. Trắc nghiệm Etilen
Bài 1: Hóa chất dùng để tách etilen khỏi hỗn hợp etan và etilen là
A. dung dịch NaOH.
B. dung dịch HCl
C. dung dịch brom.
D. dung dịch AgNO3.
Lời giải
Cho hỗn hợp khí qua dung dịch brom dư, etilen bị giữ lại, thu được etan không phản ứng thoát ra ngoài
CH2 = CH2 + Br2 → CH2Br = CH2Br
Đáp án: C
Bài 2: Chất nào sau đây vừa làm mất màu dung dịch brom, vừa tham gia phản ứng trùng hợp?
A. CH4.
B. CH3CH2OH.
C. CH3-CH3.
D. CH2=CH-CH3.
Lời giải
Chất vừa làm mất màu dung dịch brom, vừa tham gia phản ứng trùng hợp là chất có liên kết đôi (giống etilen)
=> CH2 = CH-CH3
Đáp án: D
Bài 3: Tính chất vật lí của etilen là
A. Chất lỏng, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
B. Chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
C. Chất khí, không màu, không mùi, ít tan trong nước và nặng hơn không khí.
D. Chất khí, không màu, không mùi, tan tốt trong nước và nhẹ hơn không khí.
Lời giải
Tính chất vật lí của etilen là: Chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
Đáp án: B
Bài 4: Ứng dụng nào sau đây không phải ứng dụng của etilen?
A. Điều chế PE.
B. Điều chế rượu etylic.
C. Điều chế khí ga.
D. Dùng để ủ trái cây mau chín.
Lời giải
Ứng dụng không phải của etilen là: Điều chế khí ga.
Đáp án: C
Bài 5: Phản ứng cháy giữa etilen và oxi thu được số mol CO2 và số mol H2O sinh ra theo tỉ lệ là:
A. 1 : 1 B. 2 : 1
C. 1 : 2 D. Kết quả khác
Lời giải
PTHH: C2H4 + 3O2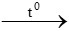 2CO2 + 2H2O
2CO2 + 2H2O
=> tỉ lệ số mol CO2 và số mol H2O là 1 : 1
Đáp án: A
Bài 6: Đốt cháy V lít etilen thu được 9 gam hơi nước. Thể tích không khí cần dùng (ở đktc), biết O2 chiếm 20% thể tích không khí?
A. 84,0 lít. B. 16,8 lít.
C. 56,0 lít. D. 44,8 lít
Lời giải
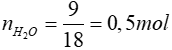
PTHH: C2H4 + 3O2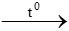 2CO2 + 2H2O
2CO2 + 2H2O
0,75 mol ← 0,5 mol
⇒ VO2 = 0,75.22,4 = 16,8 lít
Vì O2 chiếm 20% thể tích không khí => Vkhôngkhí = 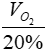 = 84 lít
= 84 lít
Đáp án: A
Bài 7: Dẫn 5,6 lít (đktc) khí metan và etilen đi qua bình đựng dung dịch nước brom, đã làm mất màu hoàn toàn dung dịch có chứa 4 gam brom. Thể tích khí metan (đktc) trong hỗn hợp là
A. 0,56 lít.
B. 5,04 lít.
C. 0,28 lít.
D. 3,36 lít
Lời giải
a) Dẫn 2 khí qua dung dịch nước brom chỉ có C2H4 phản ứng
C2H4 + Br2 → C2H4Br2
0,025 ← 0,025 mol
nCH4 = nhh - nC2H4 = 0,25 - 0,025 = 0,225 mol
VCH4 = 0,225.22,4 = 5,04 lít
Đáp án: B
Bài 8: Trong phân tử etilen có
A. 1 nguyên tử C
B. 2 nguyên tử C
C. 3 nguyên tử H
D. 6 nguyên tử H
Lời giải
Phân tử etilen có CTPT là C2H4
=> trong etilen có 2 nguyên tử C
Đáp án: B
Bài 9: CH4 và C2H4 giống nhau ở phản ứng nào sau đây?
A. tham gia phản ứng cộng với dung dịch brom.
B. tham gia phản ứng cộng với khí hiđro
C. tham gia phản ứng trùng hợp
D. tham gia phản ứng cháy với oxi.
Lời giải
CH4 và C2H4 có tính chất hóa học giống nhau là tham gia phản ứng cháy với oxi.
Đáp án: D
Bài 10: Cho các hợp chất sau: CH4, C2H6, C2H4, H2. Có bao nhiêu chất tác dụng với dung dịch nước brom ở nhiệt độ thường?
A. 1 B. 2
C. 3 D. 4
Lời giải
Chất tác dụng với dung dịch nước brom là C2H4 vì trong phân tử C2H4 có liên kết đôi
CH2 = CH2 + Br2 → CH2Br = CH2Br
Đáp án: A
Bài 11: Cho 2,8 lít hỗn hợp metan và etilen (đktc) lội qua dung dịch brom (dư), người ta thu được 4,7 gam đibroetan. Phần trăm thể tích của khí metan là
A. 20%. B. 40%.
C. 80%. D. 60%
Lời giải
![]()
PTHH: C2H4 + Br2 → C2H4Br2
0,025 ← 0,025
⇒ VC2H4 = 0,025.22,4 = 0,56 lít ⇒ VCH4 = 2,8 - 0,56 = 2,24 lít
![]()
Đáp án: C
Bài 12: Đốt cháy hết 36 gam hỗn hợp khí C3H6 và C2H6 trong O2 dư thu được 56 lít CO2 (đktc). Thể tích khí C3H6 ở đktc là
A. 11,2 lít B. 22,4 lít.
C. 33,6 lít. D. 44,8 lít.
Lời giải
Gọi số mol của C3H6 và C2H4 lần lượt là x và y mol
=> mhỗnhợp = 42x + 28y = 36 (1)
C3H6 + 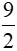 O2
O2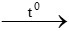 3CO2 + 3H2O
3CO2 + 3H2O
x mol → 3x mol
C2H6 + 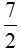 O2
O2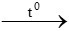 2CO2 + 3H2O
2CO2 + 3H2O
y mol → 2y mol
nCO2 = 3x + 2y = 2,5 mol (2)
Từ (1) và (2) ta có hệ:
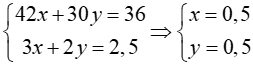
⇒VC3H6 = VC2H4 = 0,5.22,4 = 11,2 lít
Đáp án: A
Bài 13: Trong phân tử etilen giữa hai nguyên tử cacbon có
A. hai liên kết đôi.
B. một liên kết đôi.
C. một liên kết đơn.
D. một liên kết ba.
Đáp án: B
Bài 14: Etilen có tính chất vật lý nào sau đây?
A. là chất khí không màu, không mùi, tan nhiều trong nước, nhẹ hơn không khí.
B. là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. là chất khí màu vàng lục, mùi xốc, ít tan trong nước, nặng hơn không khí.
D. là chất khí không màu, mùi hắc, tan trong nước, nặng hơn không khí.
Đáp án: B
Bài 15: Khi đốt cháy khí etilen thì số mol CO2 và H2O được tạo thành theo tỉ lệ
A. 2 : 1.
B. 1 : 2.
C. 1 : 3.
D. 1 : 1.
Đáp án: D
Khi đốt cháy khí etilen thu được số mol CO2 bằng số mol nước.
Bài 16: Trong quá trình chín trái cây đã thoát ra một lượng nhỏ khí nào sau đây?
A. metan.
B. etan.
C. etilen.
D. axetilen.
Đáp án: C
Bài 17: Khí CH4 và C2H4 có tính chất hóa học giống nhau là
A. tham gia phản ứng cộng với dung dịch brom.
B. tham gia phản ứng thế với brom khi chiếu sáng.
C. tham gia phản ứng trùng hợp.
D. tham gia phản ứng cháy với khí oxi sinh ra khí cacbonic và nước.
Đáp án: D
Bài 18: Khí metan có lẫn một lượng nhỏ khí etilen. Để thu được metan tinh khiết, ta dẫn hỗn hợp khí qua
A. dung dịch brom.
B. dung dịch phenolphtalein.
C. dung dịch axit clohidric.
D. dung dịch nước vôi trong.
Đáp án: A
Dẫn hỗn hợp khí qua dung dịch brom. Khí etilen phản ứng với brom bị giữ lại trong dung dịch.
CH2 = CH2 + Br2 → Br – CH2 – CH2 – Br.
Khí metan không phản ứng thoát ra khỏi dung dịch, thu được metan tinh khiết.
Bài 19: Phản ứng đặc trưng của khí etilen là
A. phản ứng cháy.
B. phản ứng thế.
C. phản ứng cộng.
D. phản ứng phân hủy.
Đáp án: C
Bài 20: Trong phòng thí nghiệm, người ta đun rượu etylic với chất xúc tác là H2SO4 đặc, ở nhiệt độ 170°C để điều chế khí X. Khí X là
A. Cl2.
B. CH4.
C. C2H4.
D. C2H2.
Đáp án: C
Bài 21: Trùng hợp 1 mol etilen (với hiệu suất 100 %) ở điều kiện thích hợp thì thu được khối lượng polietilen là
A. 7 gam.
B. 14 gam.
C. 28 gam.
D. 56 gam.
Đáp án: C
Bảo toàn khối lượng có:
mtrước = msau ⇔ mpoli etilen = metilen = 1.28 = 28 gam.
Bài 22: Đốt cháy hoàn toàn 5,6 lít khí etilen ở đktc cần dùng lượng oxi (ở đktc) là
A. 11,2 lít.
B. 16,8 lít.
C. 22,4 lít.
D. 33,6 lít.
Đáp án: B