Tài liệu Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất tổng hợp từ đề thi môn Hóa học 11 của các trường THPT trên cả nước đã được biên soạn chi tiết giúp học sinh ôn luyện để đạt điểm cao trong bài thi học kì 1 Hóa học lớp 11. Mời các bạn cùng đón xem:
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 1
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 1)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Ba = 137)
I. TRẮC NGHIỆM
Câu 1: Dẫn luồng khí CO qua hỗn hợp Al2O3, CuO, MgO, Fe2O3 (nóng) sau khi phản ứng xảy ra hoàn toàn thu được chất rắn là
A. Al2O3, Fe2O3, Cu, MgO.
B. Al2O3, Cu, MgO, Fe.
C. Al, Fe, Cu, Mg.
D. Al2O3, Cu, Mg, Fe.
Câu 2: Cho 11,2 lít CO2 (đktc) lội chậm qua 200 ml dung dịch Ca(OH)2 2M. Sau phản ứng thu được số gam kết tủa là
A. 40 gam.
B. 50 gam.
C. 30 gam.
D. 15 gam.
Câu 3: Cho các chất gồm CH3OH (X); CH3CH2OH (Y); HOC6H4OH (Z); CH3CH2CH2OH (T). Các chất đồng đẳng là
A. X, Y, T.
B. X, Z, T.
C. X, Z.
D. Y, Z.
Câu 4: Hiện tượng các chất có cấu tạo và tính chất hóa học tương tự nhau, chúng chỉ hơn kém nhau một hay nhiều nhóm metylen (–CH2–) được gọi là hiện tượng
A. đồng phân.
B. đồng vị.
C. đồng đẳng.
D. đồng khối.
Câu 5: Hiệu ứng nhà kính là hiện tượng trái đất nóng lên. Hiệu ứng nhà kính gây ra một số hậu quả nghiêm trọng như gây biến đổi khí hậu, làm mất cân bằng sinh thái, dịch bệnh, … Khí gây ra hiệu ứng nhà kính là:
A. CO.
B. H2.
C. CO2.
D. N2.
Câu 6: Nhiệt phân hoàn toàn 9,4 gam muối nitrat của kim loại M thu được 4 gam chất rắn. Kim loại M là
A. Zn.
B. Mg.
C. Fe.
D. Cu.
Câu 7: Chọn cấu hình electron lớp ngoài cùng của nguyên tố nhóm IVA
A. ns2np4
B. ns2np2
C. ns2np3
D. ns2np5
Câu 8: Phương trình: \({S^{2 - }}\) + 2H+ H2S là phương trình ion rút gọn của phản ứng
A. 2HCl + K2S 2KCl + H2S.
B. FeS + 2HCl FeCl2 + H2S.
C. BaS + H2SO4 BaSO4 + H2S.
D. 2NaHSO4 + 2Na2S 2Na2SO4 + H2S.
Câu 9: Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400ml dung dịch (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch X. Giá tri pH của dung dịch X là:
A. 1
B. 2
C. 6
D. 7
Câu 10: Hiện tượng xảy ra khi cho giấy quỳ ẩm vào bình đựng khí amoniac là
A. giấy quỳ mất màu.
B. giấy quỳ không chuyển màu.
C. giấy quỳ chuyển sang màu đỏ.
D. giấy quỳ chuyển sang màu xanh
Câu 11: Để thu được muối trung hoà, phải lấy V(ml) dung dịch NaOH 1M trộn lẫn với 50 ml dung dịch H3PO4 1M. Giá trị V là
A. 200 ml.
B. 150 ml.
C. 300 ml
D. 250 ml.
Câu 12: Trong câu ca dao:
“Lúa chiêm lấp ló đầu bờ
Nghe tiếng sấm giật phất cờ mà lên”
Cây lúa lớn nhanh nguyên nhân chính là do:
A. khi có sấm chớp thường kèm theo mưa cung cấp nước cho cây.
B. quá trình oxi biến thành ozon làm cho không khí trong sạch hơn.
C. quá trình chuyển hóa nitơ trong không khí thành nitơ trong đất để nuôi cây.
D. do trời mưa cung cấp nước cho cây lúa.
Câu 13: Đốt cháy hoàn toàn 3,0 gam một hợp chất hữu cơ X, người ta thu được 4,40 gam CO2 và 1,80 gam H2O. Công thức đơn giản nhất của hợp chất hữu cơ X là:
A. C2H4O.
B. C2H5O.
C. CH2O.
D. CH2O2.
Câu 14: Trong các dãy chất sau đây, dãy có các chất là đồng phân
A. C2H5OH, CH3OCH3.
B. CH3OCH3, CH3CHO.
C. CH3CH2CH2OH, CH3CH2OH.
D. C4H10, C6H6.
Câu 15: Để phòng bị nhiễm độc người ta sử dụng mặt nạ phòng độc chứa hóa chất
A. CuO và MnO2
B. CuO và MgO
C. CuO và CaO
D. than hoạt tính
Câu 16: Trong các loại phân bón: NH4Cl, (NH2)2CO, (NH4)2SO4, NH4NO3. Phân có hàm lượng đạm cao nhất là
A. NH4NO3
B. NH4Cl
C. (NH4)2SO4
D. (NH2)2CO
Câu 17: Một dung dịch X chứa 0,02 mol Cu2+, 0,03 mol K+, x mol \(C{l^ - }\) và y mol \(SO_4^{2 - }\). Tổng khối lượng các muối tan trong dung dịch X là 5,435 gam. Giá trị của x và y lần lượt là
A. 0,03 và 0,02.
B. 0,05 và 0,01.
C. 0,02 và 0,05.
D. 0,01 và 0,03.
Câu 18: Để khắc chữ lên thủy tinh người ta dựa vào phản ứng
A. SiO2 + Mg 2MgO + Si
B. SiO2 + HF SiF4 + 2H2O
C. SiO2 + 2MaOH Na2SiO3 + CO2
D. SiO2 + Na2CO3 Na2SiO3 + CO2
Câu 19: Trong thực tế, người ta thường dùng chất nào sau đây để làm xốp bánh?
A. (NH4)2SO4.
B. K2SO4.
C. NaCl.
D. NH4HCO3.
Câu 20: Hai khoáng vật chính của photpho là:
A. đolomit và canxit.
B. photphorit và apatit.
C. apatit và đolomit.
D. apatit và cacnalit.
II. TỰ LUẬN
Câu 1 (2,5 điểm) Cho 25,5 gam hỗn hợp Mg và Al tác dụng vừa đủ với dung dịch HNO3 loãng thu được 5,6 lít khí N2 (đktc, sản phẩm khử duy nhất) và dung dịch X.
a) Tính khối lượng từng kim loại trong hỗn hợp?
b) Tính thể tích dung dịch NaOH 5M tối thiểu cần thêm vào để thu được lượng kết tủa lớn nhất, nhỏ nhất? Tính khối lượng kết tủa?
Bài 2 (1,5 điểm): Từ tinh dầu chanh người ta tách được chất limonen thuộc loại hiđrocacbon có hàm lượng nguyên tố H là 11,765%. Hãy tìm công thức phân tử của limonen, biết tỉ khối hơi của limonen so với heli bằng 34.
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 2
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 2)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag =108; Ba = 137)
I. TRẮC NGHIỆM (6 điểm)
Câu 1: Các nguyên tử thuộc nhóm IVA có cấu hình electron lớp ngoài cùng là
A. ns2np5.
B. ns2np3.
C. ns2np4.
D. ns2np2.
Câu 2: Kim loại bị thụ động trong HNO3 đặc, nguội là
A. Pt, Cu.
B. Al, Fe.
C. Ag, Fe.
D. Pb, Ag.
Câu 3: Chất khí nào sau đây được tạo ra từ bình chữa cháy và dùng để sản xuất nước đá khô?
A. H2O.
B. N2.
C. CO2.
D. CO.
Câu 4: Cho m gam Al phản ứng hoàn toàn với dung dịch HNO3 loãng (dư), thu được 4,48 lít khí NO (đktc, sản phẩm khử duy nhất). Giá trị của m là
A. 2,70.
B. 4,05.
C. 8,10.
D. 5,40.
Câu 5: Phương trình điện li nào sau đây không đúng?
A. Mg(OH)2 ⇄ Mg2+ + 2\(O{H^ - }\)
B. K2SO4 ⇄ 2K+ + \(SO_4^{2 - }\)
C. HNO3 → \({H^ + }\)+ \(NO_3^ - \)
D. \(HSO_3^ - \) ⇄ H+ + \(SO_3^{2 - }\)
Câu 6: Phương trình ion: \(O{H^ - } + HCO_3^ - \to CO_3^{2 - } + {H_2}O\) là của phản ứng xảy ra giữa cặp chất nào sau đây?
A. NaOH + Ba(HCO3)2.
B. Ba(HCO3)2 + Ba(OH)2.
C. NaHCO3 + Ba(OH)2
D. NaHCO3 + NaOH.
Câu 7: Khi nhiệt phân, dãy muối rắn nào dưới đây đều sinh ra kim loại, khí nitơ đioxit và oxi?
A. AgNO3, Hg(NO3)2.
B. Cu(NO3)2, Mg(NO3)2.
C. Hg(NO3)2, Mg(NO3)2.
D. AgNO3, Cu(NO3)2.
Câu 8: Độ dinh dưỡng của phân lân được tính bằng:
A. % P2O5.
B. % P.
C. %\(PO_4^{3 - }\).
D. Ca(H2PO4)2.
Câu 9: Chất phản ứng được với NH3 là:
A. Na2O.
B. AlCl3 (dd).
C. Na2CO3 (dd).
D. NaOH (dd).
Câu 10: Nồng độ mol của anion trong dung dịch BaCl2 0,20M là
A. 0,40M.
B. 0,20M.
C. 0,30M.
D. 0,10M.
Câu 11: Trong những nhận xét dưới đây về muối amoni, nhận xét nào là đúng?
A. Muối amoni là tinh thể ion, phân tử gồm cation amoni và anion hiđroxit.
B. Tất cả các muối amoni đều dễ tan trong nước, khi tan điện li hòa toàn thành cation amoni và anion gốc axit.
C. Dung dịch muối amoni tác dụng với dung dịch kiềm đặc, nóng cho thoát ra chất khí làm quỳ tím hóa đỏ.
D. Khi nhiệt phân muối amoni luôn luôn có khí amoniac thoát ra.
Câu 12: Cho P tác dụng với Mg, sản phẩm thu được là:
A. Mg2P2O7.
B. Mg3P2.
C. Mg(PO3)2.
D. Mg3(PO4)2.
Câu 13: Số công thức cấu tạo có thể có ứng với các công thức phân tử C3H8O là
A. 1
B. 2
C. 3
D. 4.
Câu 14: Cặp chất nào sau đây là đồng đẳng của nhau?
A. CH3OH, CH3OCH3
B. CH3OCH3, CH3CHO.
C. CH3OH, C2H5OH
D. CH3CH2OH, C3H6(OH)2.
Câu 15: Tỉ khối hơi cuả chất X so với hiđro bằng 44. Phân tử khối của X là
A. 44
B. 46
C. 22
D. 88.
Câu 16: Tìm phản ứng nhiệt phân sai:
A. 2AgNO3 Ag2O + 2NO2 + \(\frac{1}{2}\)O2
B. KNO3 KNO2 + \(\frac{1}{2}\)O2
C. Zn(NO3)2 ZnO + 2NO2 + \(\frac{1}{2}\)O2
D. Mg(NO3)2 MgO + 2NO2 + \(\frac{1}{2}\)O2
Câu 17: Theo thuyết cấu tạo hoá học, trong phân tử các chất hữu cơ, các nguyên tử liên kết hoá học với nhau theo cách nào sau đây:
A. đúng hoá trị.
B. đúng số oxi hoá.
C. một thứ tự nhất định.
D. đúng hoá trị và theo một thứ tự nhất định
Câu 18: Khí N2 tương đối trơ ở nhiệt độ thường là do
A. Trong phân tử N2 chứa liên kết 3 rất bền.
B. Nguyên tử nitơ có độ âm điện lớn nhất trong nhóm nitơ.
C. Nitơ có bán kính nguyên tử nhỏ, phân tử không phân cực.
D. Trong phân tử N2, mỗi nguyên tử còn một cặp electron chưa tham gia liên kết.
Câu 19: Cho 2,24 lít CO2 (đktc) vào 200 ml dung dịch Ca(OH)2 1M , khối lượng kết tủa thu được là
A. 10g B. 15g
C. 20g D. 25g
Câu 20: Phương trình hóa học nào viết sai so với phản ứng xảy ra?
A. CaCl2 + CO2 + H2O → CaCO3 + 2HCl
B. FeS + 2HCl → FeCl2 + H2S
C. BaCl2 + H2SO4 → BaSO4 + 2HCl
D. CH3COONa + HCl → CH3COOH + NaCl
II. TỰ LUẬN (4 điểm)
Câu 1 (1 điểm): Thêm 200 ml dung dịch KOH 1M vào 300 ml dung dịch H3PO4 1M thu được dung dịch X. Tính khối lượng muối trong dung dịch X.
Câu 2 (1,5 điểm): Cho 1,71 gam hỗn hợp gồm (Al, Mg, Cu) phản ứng hết với 200 ml dung dịch HNO3 1M. Sau phản ứng thu được 7,91 gam hỗn hợp gồm 3 muối khan và V lít hỗn hợp khí NO2 và NO. Nung muối này tới khối luợng không đổi được m gam chất rắn. Tính m?
Câu 3 (1,5 điểm): Đốt cháy hoàn toàn 100 ml hợp chất hữu cơ X, cần hết 300 ml O2, thu được 200 ml CO2 và 300 ml hơi nước. Các khí được đo ở cùng nhiệt độ, áp suất. Xác định công thức phân tử của X?
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 3
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 3)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag =108; Ba = 137)
Câu 1: Khi đun nóng dung dịch canxi hiđrocacbonat thì có kết tủa xuất hiện. Tổng các hệ số tỉ lượng trong phương trình phản ứng là:
A. 4
B. 5
C. 6
D. 7
Câu 2: Thành phần % của C, H, O trong hợp chất Z lần lượt là 54,5%; 9,1%; 36,4%. Công thức đơn giản nhất của Z là:
A. C2H4O
B. C4H8O2
C. C5H9O
D. C3H6O
Câu 3: Theo thuyết A-re-ni-ut axit là chất
A. khi tan trong nước phân li ra ion \(O{H^ - }\).
B. khi tan trong nước phân li ra ion H+.
C. khi tan trong nước chỉ phân li ra ion H+.
D. khi tan trong nước chỉ phân li ra ion \(O{H^ - }\).
Câu 4: Kết luận nào sau đây là đúng?
A. Các nguyên tử trong phân tử hợp chất hữu cơ liên kết với nhau không theo một thứ tự nhất định.
B. Các chất có cùng công thức phân tử nhưng khác nhau về công thức cấu tạo được gọi là các chất đồng đẳng của nhau.
C. Các chất khác nhau có cùng công thức phân tử được gọi là các chất đồng phân của nhau.
D. Các chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm -CH2-, do đó tính chất hóa học khác nhau là những chất đồng đẳng.
Câu 5: Đốt cháy hoàn toàn 1,605 gam hợp chất hữu cơ A thu được 4,62 gam CO2; 1,215 gam H2O và 168 ml N2 (đktc). Tỉ khối hơi của A so với không khí không vượt quá 4. Công thức phân tử của A là:
A. C5H5N.
B. C6H9N.
C. C7H9N.
D. C6H7N
Câu 6: Chất điện li mạnh là
A. H2O
B. HF.
C. HClO
D. NaCl
Câu 7: Trộn 100 ml dung dịch gồm (HCl 0,1M; HNO3 0,2M; H2SO4 0,1M) với V ml dung dịch Y gồm (NaOH 0,1M; Ba(OH)2 0,3 M). Sau phản ứng thu được dung dịch có pH = 13. Giá trị của V là:
A. 200
B. 150
C. 100
D. 300
Câu 8: Hòa tan hoàn toàn 0,1 mol khí CO2 vào 100ml dd NaOH 1,6 M thu được:
A. NaHCO3 và CO2 dư
B. Na2CO3 và NaHCO3
C. Na2CO3 và CO2 dư
D. Na2CO3 và NaOH dư
Câu 9: Trong những dãy chất sau đây, dãy nào có các chất là đồng phân của nhau?
A. C4H10, C6H6.
B. CH3CH2CH2OH, C2H5OH.
C. CH3OCH3, CH3CHO.
D. C2H5OH, CH3OCH3.
Câu 10: Để hòa tan SiO2 người ta sử dụng dung dịch:
A. HNO3 đặc.
B. HCl.
C. H2SO4 đặc nóng.
D. HF.
Câu 11: Phương trình ion rút gọn: 2H+ + \(SiO_3^{2 - }\) H2SiO3 ứng với phản ứng của chất nào sau đây?
A. Axit cacbonic và natri silicat
B. Axit cacboxilic và canxi silicat
C. Axit clohiđric và canxi silicat
D. Axit clohiđric và natri silicat
Câu 12: Trong rượu vang, [H+] = 3,2.10-4 M. pH của rượu đo được là:
A. 9,3
B. 4,7
C. 3,5
D. 10,5
Câu 13: Phân lân được đánh giá bằng hàm lượng % của chất nào sau đây?
A. H3PO4
B. P2O5
C. PO43-
D. P
Câu 14: Dung dịch A chứa 0,1 mol Ca2+, 0,1 mol Cu2+, 0,2 mol \(NO_3^ - \) và x mol \(C{l^ - }\). Giá trị của x là
A. 0,4
B. 0,3
C. 0,2
D. 0,5
Câu 15: Kim loại không tác dụng được với dung dịch HNO3 đặc, nguội:
A. Cu, Ag
B. Al, Cu.
C. Fe, Al
D. Zn, Fe
Câu 16: Cho các phát biểu:
(1). Liên kết hóa học chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
(2). Các chất có cấu tạo và tính chất tương tự nhau nhưng về thành phần phân tử khác nhau một hay nhiều nhóm -CH2- là đồng đẳng của nhau.
(3). Các chất có cùng khối lượng phân tử là đồng phân của nhau.
(4). Liên kết ba gồm hai liên kết p và một liên kết s.
Số phát biểu đúng là
A. 1
B. 2
C. 3
D. 4.
Câu 17: Hợp chất X có công thức đơn giản nhất là CH2O và có tỉ khối hơi so với hiđro bằng 90. Công thức phân tử của X là:
A. C2H4O2
B. C6H12O6
C. C4H8O4
D. CH2O
Câu 18: Phương trình phản ứng nhiệt phân nào sai?
A. NH4NO3 NH3 + HNO3
B. NH4Cl NH3 + HCl
C. NH4NO2 N2 + 2H2O
D. (NH4)2CO3 2NH3 + CO2 + H2O
Câu 19: Khi cho Mg dư tác dụng với dung dịch HNO3 thu được hỗn hợp khí X gồm N2O và N2. Khi phản ứng kết thúc, cho thêm NaOH vào thì giải phóng khí Y. Khí Y là:
A. NH3.
B. H2.
C. NO.
D. NO2.
Câu 20: Tính oxi hóa của C thể hiện ở phản ứng:
A. C + H2O CO + H2
B. 3C + 4Al Al4C3
C. C + 2CuO 2Cu + CO
D. C + O2 CO2
Câu 21: Dung dịch X gồm: 0,09 mol \(C{l^ - }\), 0,04 mol Na+, a mol Fe3+ và b mol \(SO_4^{2 - }\). Khi cô cạn dung dịch X thu được 7,715 gam muối khan. Giá trị của a và b lần lượt là:
A. 0.05 và 0,05.
B. 0,03 và 0,02.
C. 0,07 và 0,08.
D. 0,018 và 0,027.
Câu 22: Các tập hợp ion sau đây có thể tồn tại đồng thời trong cùng một dung dịch?
A. Na+, Cu2+, \(O{H^ - }\), \(NO_3^ - \).
B. Ca2+, Fe2+, \(NO_3^ - \), \(C{l^ - }\).
C. Na+, Ca2+, \(HCO_3^ - \), \(O{H^ - }\).
D. Fe2+, H+, \(O{H^ - }\), \(NO_3^ - \).
Câu 23: Có thể thu được nitơ từ phản ứng nào sau đây?
A. Đun nóng dung dịch bão hòa natri nitrit với amoni clorua.
B. Nhiệt phân muối bạc nitrat.
C. Cho bột Cu vào dung dịch HNO3 đặc nóng.
D. Cho muối amoni nitrat vào dung dịch kiềm.
Câu 24: Một loại phân supephotphat kép có chứa 69,62% muối canxi đihiđrophotphat, còn lại gồm các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là:
A. 48,52% B. 39,76%
C. 42,25% D. 45,75%
Câu 25: Trong các cặp chất sau đây, cặp chất nào cùng tồn tại trong dung dịch?
A. AlCl3 và Na2CO3.
B. HNO3 và NaHCO3.
C. NaAlO2 và KOH.
D. NaCl và AgNO3.
Câu 26: Trong phản ứng nào sau đây, nitơ thể hiện tính khử?
A. N2 + 3H2 2NH3
B. N2 + 6Li 2Li3N
C. N2 + O2 2NO
D. N2 + 3Mg Mg3N2
Câu 27: Cho 8 gam Cu tác dụng với 120 ml dung dịch X gồm HNO3 1M và H2SO4 0,5M thu được V lít khí NO (đktc). Tính V?
A. 1,244 lít
B. 1,68 lít
C. 1,344 lít
D. 1,12 lít
Câu 28: Thực hiện phản ứng giữa H2 và N2 (tỉ lệ mol 4 : 1) trong bình kín có xúc tác, thu được hỗn hợp khi có áp suất giảm 9% so với ban đầu (trong cùng điều kiện). Hiệu suất phản ứng là:
A. 20%.
B. 22,5%.
C. 25%.
D. 27%.
Câu 29: Cho P tác dụng với Ca, sản phẩm thu được là:
A. Ca3P2.
B. Ca2P3.
C. Ca3(PO4)2.
D. CaP2.
Câu 30: Đốt cháy hoàn toàn 3,72 gam chất hữu cơ A thu được 10,56 gam CO2 và 2,52 gam H2O; 0,448 lít N2 (đktc). Biết MA = 93 đvC. A có công thức phân tử là:
A. C3H7O2N.
B. C7H7N.
C. C6H7N.
D. C6H5ON.
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 4
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 4)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Ba = 137)
Câu 1: Có các dung dịch muối Al(NO3)3, (NH4)2SO4, NH4NO3, FeCl2 đựng trong các lọ riêng biệt bị mất nhãn. Nếu chỉ dùng một hoá chất làm thuốc thử để phân biệt các muối trên thì chọn chất nào sau đây:
A. Dung dịch NaOH.
B. Dung dịch Ba(OH)2.
C. Dung dịch Ba(NO3)2.
D. Dung dịch BaCl2.
Câu 2: Dãy các chất tác dụng được với cả dung dịch HCl và dung dịch NaOH là:
A. Zn(OH)2, NaHCO3, CuCl2
B. Na2SO4, ZnO, Zn(OH)2.
C. Na2SO4, HNO3, Al2O3.
D. Al(OH)3, Al2O3, NaHCO3.
Câu 3: Cho 200 ml dung dịch H3PO4 1,5M tác dụng với 200 ml dung dịch NaOH 2M. Sau phản ứng thu được muối nào?
A. NaH2PO4 và Na3PO4.
B. NaH2PO4 và Na2HPO4.
C. Na2HPO4 và Na3PO4.
D. NaH2PO4.
Câu 4: Một học sinh nghiên cứu một dung dịch X đựng trong lọ không dán nhãn và thu được kết quả sau:
- X đều có phản ứng với cả 3 dung dịch: NaHSO4, Na2CO3 và AgNO3.
- X không phản ứng với cả 3 dung dịch: NaOH, Ba(NO3)2, HNO3.
Vậy dung dịch X là dung dịch nào sau đây?
A. Dung dịch FeCl2.
B. Dung dịch BaCl2.
C. Dung dịch Mg(NO3)2.
D. Dung dịch CuSO4.
Câu 5: Dung dịch nào sau đây dẫn điện được:
A. Dung dịch ancol.
B. Dung dịch muối ăn.
C. Dung dịch benzen trong ancol.
D. Dung dịch đường.
Câu 6: Nung nóng hỗn hợp 14,0 lít NH3 và 16,0 lít O2, trong điều kiện thích hợp sẽ điều chế được bao nhiêu lít khí NO với H = 75% (các thể tích khí đo ở cùng điều kiện t0 và p)?
A. 9,6 lít
B. 12,8 lít
C. 16 lít
D. 10,5 lít
Câu 7: Cho sơ đồ điều chế HNO3 trong phòng thí nghiệm:
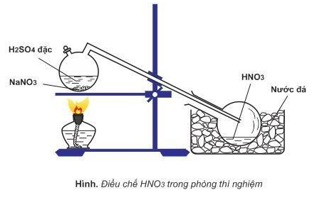
Phát biểu nào sau đây là sai khi nói về quá trình điều chế HNO3?
A. Đốt nóng bình cầu bằng đèn cồn để phản ứng xảy ra nhanh hơn.
B. HNO3 sinh ra dưới dạng hơi nên cần làm lạnh để ngưng tụ.
C. HNO3 có nhiệt độ sôi thấp (830C) nên dễ bị bay hơi khi đun nóng.
D. HNO3 là axit yếu hơn H2SO4 nên bị đẩy ra khỏi muối.
Câu 8: Cho 300 ml dung dịch AlCl3 1M tác dụng với 500 ml dung dịch NaOH 2M thì khối lượng kết tủa thu được là:
A. 15,6g. B. 25,2g.
C. 7,8g. D. 23,4g.
Câu 9: Kim loại tác dụng với HNO3 không tạo ra được chất nào sau đây?
A. NH4NO3 B. NO2.
C. N2. D. N2O5
Câu 10: Nhiệt phân hoàn toàn 18,8 gam muối nitrat của kim loại M, thu được 8,0 gam oxit kim loại tương ứng. M là kim loại:
A. Cu B. Zn
C. Mg D. Fe
Câu 11: Cho phản ứng NaOH + HCl → NaCl + H2O. Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A. KOH + HNO3 → KNO3 + H2O.
B. 2KOH + FeCl2 → Fe(OH)2 + 2KCl.
C. NaOH + NaHCO3 → Na2CO3 + H2O.
D. NaOH + NH4Cl → NaCl + NH3 + H2O.
Câu 12: Cho các phát biểu sau:
(1) Photpho trắng là chất rắn trong suốt, màu trắng hoặc màu vàng nhạt, trông giống như sáp, có cấu trúc tinh thể phân tử.
(2) Photpho đỏ là chất bột màu đỏ có cấu trúc polime nên khó nóng chảy và khó bay hơi hơn photpho trắng.
(3) Trong tự nhiên photpho tồn tại chủ yếu dạng tự do.
(4) Ở nhiệt độ thường, photpho trắng phát quang màu lục nhạt trong bóng tối.
(5) Ở nhiệt độ thường photpho kém hoạt động hóa học hơn nitơ do độ âm điện nhỏ hơn.
(6) Phần lớn photpho dùng sản xuất axit photphoric, một phần sản xuất diêm, bom, đạn cháy.
Số phát biểu đúng là:
A. 6
B. 5
C. 4
D. 3
Câu 13: Điều khẳng định nào sau đây đúng khi nói về tính chất hóa học của NH3. NH3 có:
A. Tính oxi hoá
B. Tính khử và tính bazơ yếu
C. Tính khử
D. Tính bazơ yếu
Câu 14: Dung dịch thu được khi trộn lẫn 200 ml dung dịch NaCl 0,2M và 300 ml dung dịch Na2SO4 0,2M có nồng độ mol cation Na+ là bao nhiêu?
A. 1M.
B. 0,32M.
C. 0,23M.
D. 0,1M.
Câu 15: Phát biểu nào sau đây đúng?
A. H3PO4 là axit có tính khử mạnh.
B. H3PO4 là một axit có tính oxi hoá mạnh vì photpho có số oxi hoá cao nhất +5.
C. H3PO4 là một axit trung bình, trong dung dịch phân li theo 3 nấc.
D. H3PO4 là một axit rất mạnh.
Câu 16: Trong thành phần phân tử hợp chất hữu cơ nhất thiết phải có nguyên tố:
A. cacbon
B. hiđro
C. oxi
D. nitơ.
Câu 17: Oxi hóa hoàn toàn 1,5 gam hợp chất hữu cơ X, thu được 0,224 lít N2 và 0,896 lít CO2 (các khí đều đo ở đktc) và 0,9 gam H2O. Khối lượng nguyên tố oxi trong 1,5 gam X là
A. 0,32 gam
B. 0,16 gam
C. 0,64 gam
D. 0,78 gam
Câu 18: Khi đốt 1 lít khí X cần 6 lít O2 thu dược 4 lít CO2 và 5 lít hơi H2O (có thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất). Công thức phân tử của X là
A. C4H10
B. C4H8O2
C. C4H10O2
D. C3H8O.
Câu 19: Kết luận nào sau đây là đúng?
A. Các nguyên tử trong phân tử hợp chất hữu cơ liên kết với nhau không theo một thứ tự nhất định.
B. Các chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm -CH2-, do đó tính chất hóa học khác nhau là những chất đồng đẳng.
C. Các chất có cùng công thức phân tử nhưng khác nhau về công thức cấu tạo được gọi là các chất đồng đẳng của nhau.
D. Các chất khác nhau có cùng công thức phân tử được gọi là các chất đồng phân của nhau.
Câu 20: Phân bón có hàm lượng nitơ cao nhất là:
A. NH4NO3
B. (NH4)2SO4
C. NH4Cl
D. (NH2)2CO
Câu 21: Tính oxi hóa của cacbon thể hiện ở phản ứng
A. C + O2 CO2.
B. C + 2CuO 2Cu + CO2.
C. 3C + 4Al Al4C3.
D. C + H2O CO + H2.
Câu 22: Một loại phân supephotphat kép có chứa 69,62% muối canxi đihiđrophotphat, còn lại gồm các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là:
A. 48,52% B. 39,76%
C. 42,25% D. 45,75%
Câu 23: Khi nhiệt phân, nhóm các muối nitrat cho sản phẩm kim loại, khí NO2, O2 là
A. Cu(NO3)2, Pb(NO3)2.
B. Ca(NO3)2, Hg(NO3)2, AgNO3.
C. Zn(NO3)2, AgNO3, LiNO3.
D. Hg(NO3)2, AgNO3.
Câu 24: Trong bình kín chứa 0,5 mol CO và m gam Fe3O4. Đun nóng bình cho tới khi phản ứng xảy ra hoàn toàn thì khí trong bình có tỉ khối so với khí CO ban đầu là 1,457. Giá trị của m là:
A. 17,4. B. 11,6.
C. 22,8. D. 23,2.
Câu 25: Số liên kết σ và số liên kết π trong CH2 = CH – CH2 – CH = CH2 lần lượt là:
A. 8 và 2.
B. 10 và 2.
Câu 26: Dãy các chất đều phản ứng với NH3 trong điều kiện thích hợp là:
A. HCl, O2, Cl2, FeO.
B. H2SO4, Ba(OH)2, FeO, NaOH.
C. HCl, HNO3, AlCl3, CuO.
D. KOH, HNO3, CuO, CuCl2.
Câu 27: Phản ứng hóa học nào sau đây có phương trình ion thu gọn là H+ + \(O{H^ - }\) → H2O?
A. HCl + NaOH → H2O + NaCl
B. NaOH + NaHCO3 → H2O + Na2CO3
C. H2SO4 + BaCl2 → 2HCl + BaSO4↓
D. H2SO4 + Ba(OH)2 → 2H2O + BaSO4↓
Câu 28: Chất nào sau đây không tạo kết tủa khi cho vào dung dịch AgNO3
A. KBr
B. K3PO4
C. HCl
D. H3PO4
Câu 29: pH của dung dịch Ba(OH)2 0,05M là:
A. 13
B. 12
C. 1
D. 11
Câu 30: Chất nào sau đây là hiđroxit lưỡng tính?
A. Mg(OH)2.
B. Fe(OH)3.
C. KOH.
D. Al(OH)3.
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 5
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 5)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag =108; Ba = 137)
Câu 1: Phát biểu nào sau đây là đúng?
A. Phân lân cung cấp nitơ hóa hợp cho cây dưới dạng ion nitrat (NO3-) và ion amoni (NH4+).
B. Phân hỗn hợp chứa nitơ, photpho, kali được gọi chung là phân NPK.
C. Phân urê có công thức là (NH4)2CO3.
D. Amophot là hỗn hợp các muối (NH4)2HPO4 và KNO3.
Câu 2: Dãy gồm các ion cùng tồn tại trong một dung dịch là
A. Fe3+, \(O{H^ - }\), Cl–, Ba2+.
B. Na+, Ag+, \(NO_3^ - \), \(C{l^ - }\)
C. Ca2+, Cl–, Na+, \(CO_3^{2 - }\).
D. K+, Ba2+, OH–, Cl–.
Câu 3: Phản ứng giữa HNO3 với FeO sản phẩm khử tạo ra NO. Tổng hệ số cân bằng (các số là số nguyên tối giản) trong phản ứng này là:
A. 20
B. 12
C. 16
D. 22
Câu 4: Phương trình ion thu gọn của phản ứng cho biết:
A. bản chất của phản ứng trong dung dịch chất điện li
B. nồng độ các ion trong dung dịch
C. những ion nào tồn tại trong dung dịch
D. không cho biết được điều gì
Câu 5: Sản phẩm của phản ứng nhiệt phân hoàn toàn AgNO3 là:
A. Ag, NO2, O2
B. Ag2O, NO2, O2
C. Ag, NO, O2
D. Ag2O, NO, O2
Câu 6: Đốt cháy hoàn toàn 3 gam hợp chất hữu cơ X thu được 4,4 gam CO2 và 1,8 gam H2O. Biết tỉ khối của X so với He (MHe = 4) là 7,5. Công thức phân tử của X là:
A. CH2O2.
B. C2H6.
C. C2H4O.
D. CH2O
Câu 7: Khi cho Mg dư tác dụng với dung dịch HNO3 thu được hỗn hợp khí X gồm N2O và N2. Khi phản ứng kết thúc, cho thêm NaOH vào thì giải phóng khí Y. Khí Y là:
A. NH3.
B. H2.
C. NO.
D. NO2.
Câu 8: Dung dịch A chứa 0,1 mol Ca2+, 0,1 mol Cu2+, 0,2 mol \(NO_3^ - \) và x mol Cl- Giá trị của x là
A. 0,4
B. 0,3
C. 0,2
D. 0,5
Câu 9: Kim loại không tác dụng được với dung dịch HNO3 đặc, nguội:
A. Cu, Ag
B. Al, Cu.
C. Fe, Al
D. Zn, Fe
Câu 10: Cho 2,24 lít CO2 (đktc) hấp thụ vào 200 ml dung dịch NaOH 1M thu được dung dịch A. Chất tan trong dung dịch A là:
A. NaHCO3
B. NaHCO3 và Na2CO3
C. Na2CO3
D. Na2CO3 và NaOH dư
Câu 11: Tổng thể tích N2 và H2 (đktc) cần dùng để điều chế 51 gam NH3 (H = 25%) là:
A. 537,6 lít
B. 512,23 lít
C. 120 lít
D . 134,4 lít
Câu 12: Hoà tan hoàn toàn 4,48 gam kim loại M bằng dung dịch HNO3 đặc nóng thu được 5,376 lít khí NO2 (đktc). Kim loại M là:
A. Fe.
B. Al.
C. Cu.
D. Mg.
Câu 13: Hòa tan 6,3 g hỗn hợp Mg và Al trong dung dịch HNO31M đặc nguội dư, thoát ra 6,72 lít khí NO2 (đktc). Khối lượng Al trong hỗn hợp ban đầu là:
A. 5,4g.
B. 2,4g
C. 2,7g.
D. 3,2g.
Câu 14: Để nhận biết khí NH3 ta dùng:
A. Giấy quỳ tím chuyển sang màu xanh.
B. Giấy quỳ tím ẩm chuyển sang màu xanh.
C. Giấy quỳ tím ẩm chuyển sang màu đỏ.
D. Giấy quỳ tím chuyển sang màu đỏ.
Câu 15: Khí CO không khử được oxit kim loại nào sau đây ở nhiệt độ cao?
A. Fe3O4.
B. CuO.
C. MgO.
D. PbO.
Câu 16: Để phân biệt 2 chất rắn Na2CO3 và Na2SiO3 có thể dùng thuốc thử là
A. dung dịch NaOH.
B. dung dịch HCl
C. dung dịch NaCl
D. nước
Câu 17: Trong y học, dược phẩm Nabica là chất được dùng để trung hòa bớt lượng axit (dư) HCl trong dạ dày. Công thức của Nabica là:
A. NaHCO3.
B. (NH4)2CO3
C. Na2CO3
D.NH4HCO3
Câu 18: Chọn cấu hình electron lớp ngoài cùng của nguyên tố nhóm VA:
A. ns2np5
B. ns2np3
C. ns2np2
D. ns2np4
Câu 19: Ở điều kiện thường photpho hoạt động hóa học khá hơn nitơ là do
A. Photpho ở trạng thái rắn còn nitơ ở trạng thái khí.
B. Độ âm điện của P nhỏ hơn nitơ.
C. Photpho chỉ có liên kết đơn, còn nitơ có liên kết ba.
D. P có đô âm điện lớn hơn nitơ.
Câu 20: Cho Fe(III) oxit tác dụng với axit nitric thì sản phẩm thu được là:
A. Fe(NO3)2, NO và H2O
B. Fe(NO3)2, NO2 và H2O
C. Fe(NO3)2, N2
D. Fe(NO3)3 và H2O
Câu 21: Cho P tác dụng với Ca, sản phẩm thu được là:
A. Ca3P2.
B. Ca2P3.
C. Ca3(PO4)2.
D. CaP2.
Câu 22: Trong bình kín chứa 0,5 mol CO và m gam Fe3O4. Đun nóng bình cho tới khi phản ứng xảy ra hoàn toàn thì khí trong bình có tỉ khối so với khí CO ban đầu là 1,457. Giá trị của m là:
A. 17,4.
B. 11,6.
C. 22,8.
D. 23,2.
Câu 23: Một dung dịch chứa Mg2+ (0,02 mol), K+ (0,03 mol), Cl- (0,04 mol) và ion Z (y mol). Ion Z và giá trị của y là:
A. \(NO_3^ - \) (0,03).
B. \(CO_3^{2 - }\) (0,015).
C. \(SO_4^{2 - }\) (0,01).
D. \(NH_4^ + \) (0,01).
Câu 24: Cho các phát biểu sau:
(1) Độ dinh dưỡng của phân đạm, phân lân và phân kali tính theo phần trăm khối lượng tương ứng của N2O5; P2O5 và K2O.
(2) Người ta không bón phân urê kèm với vôi.
(3) Phân lân chứa nhiều photpho nhất là supephotphat kép.
(4) Bón nhiều phân đạm amoni sẽ làm đất chua.
(5) Quặng photphorit có thành phần chính là Ca3(PO4)2.
Trong các phát biểu trên, số phất biểu đúng là
A. 5.
B. 2.
C. 3.
D. 4.
Câu 25: Đốt cháy hoàn toàn m gam hợp chất hữu cơ X (C, H, O). Cần vừa đủ 6,72 lít O2 (đktc), thu được 4,48 lít CO2 (đktc) và 5,4 gam H2O. Thành phần phần trăm khối lượng oxi trong X là
A. 34,78%
B. 69,56%
C. 76,19 %
D. 67,71%
Câu 26: Liên kết hóa học trong phân tử chất hữu cơ chủ yếu là liên kết
A. ion
B. cộng hóa trị
C. kim loại
D. hiđro.
Câu 27: Trong công nghiệp, N2 được tạo ra bằng cách nào sau đây?
A. Nhiệt phân muối NH4NO3 đến khối lượng không đổi.
B. Chưng cất phân đoạn không khí lỏng.
C. Phân hủy NH3.
D. Đun nóng Mg với dung dịch HNO3 loãng.
Câu 28: Tìm phản ứng viết sai:
A. NH4NO3 NH3 + HNO3
B. (NH4)2CO3 2NH3 + CO2 + H2O
C. NH4Cl NH3 + HCl
D. NH4HCO3 NH3 + CO2 + H2O
Câu 29: Thêm 0,15 mol KOH vào dung dịch chứa 0,1 mol H3PO4. Sau phản ứng trong dung dịch chứa:
A. KH2PO4 và K3PO4.
B. K2HPO4 và K3PO4.
C. KH2PO4 và K2HPO4.
D. K3PO4 và KOH dư.
Câu 30: Cho các chất KNO3, Fe(NO3)3, Zn(NO3)2, Fe(NO3)2. Số chất khi bị nhiệt phân thu được hỗn hợp khí NO2, O2 là:
A. 4.
B. 3
C. 2
D. 1
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 6
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 6)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag =108; Ba = 137)
I. TRẮC NGHIỆM (6 ĐIỂM)
Câu 1: Cho từng chất: Fe, Cu, P, Al(OH)3, FeSO4, FeO lần lượt phản ứng với HNO3 đặc, nóng. Số phản ứng thuộc loại phản ứng oxi hoá - khử là:
A. 3. B. 6.
C. 5. D. 4.
Câu 2: Trong thực tế, người ta thường dùng chất nào sau đây để làm xốp bánh?
A. (NH4)2SO4.
B. K2SO4.
C. NaCl.
D. NH4HCO3.
Câu 3: Cho thí nghiệm như hình vẽ:
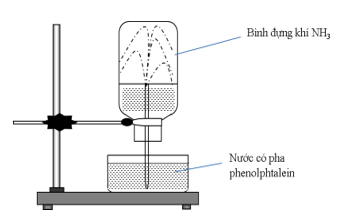
Hiện tượng xảy ra trong thí nghiệm là
A. nước phun vào bình và chuyển thành màu xanh.
B. nước phun vào bình và chuyển thành màu tím.
C. nước phun vào bình và chuyển thành màu hồng.
D. nước phun vào bình và không có màu.
Câu 4: Dung dịch Y chứa 0,01 mol K+; 0,02 mol Na+; 0,02 mol Cl- và x mol \(SO_4^{2 - }\). Cô cạn dung dịch Y thì thu được bao nhiêu gam muối khan (giả sử chỉ có nước bay hơi)?
A. 2,52.
B. 2,40.
C. 2,25.
D. 2,04.
Câu 5: Trộn 150 dung dịch KOH 1M tác dụng với 50ml dung dịch H3PO4 2M. Sau khi phản ứng hoàn toàn thu được dung dịch T. Muối có trong dung dịch T là
A. KH2PO4 và K2HPO4.
B. KH2PO4 và K3PO4.
C. K2HPO4 và K3PO4.
D. KH2PO4.
Câu 6: Cho dung dịch KOH dư vào 50 ml dung dịch (NH4)2SO4 1M. Đun nóng nhẹ, thể tích khí NH3 thoát ra (đktc) là
A. 1,12 lít.
B. 2,24 lít.
C. 4,48 lít.
D. 0,112 lít.
Câu 7: Chất nào là chất điện li mạnh?
A. CH3COOH.
B. H2S.
C. Cu(OH)2.
D. KCl.
Câu 8: Cặp chất nào sau đây không xảy ra phản ứng trong dung dịch?
A. NH4Cl và AgNO3.
B. MgCl2 và KNO3.
C. CH3COONa và HCl.
D. Fe2(SO4)3 và NaOH.
Câu 9: Độ dinh dưỡng của phân lân được đánh giá theo tỉ lệ phần trăm về khối lượng của:
A. P2O5.
B. nguyên tố P.
C. K2O.
D. N2O5.
Câu 10: Trường hợp nào sau đây, khi nhiệt phân tạo ra sản phẩm là oxit kim loại, khí nitơ đioxit và oxi?
A. KNO3, Pb(NO3)2.
B. Fe(NO3)3, AgNO3.
C. Zn(NO3)2, Mg(NO3)2.
D. Pb(NO3)2, Ca(NO3)2.
Câu 11: Silic thể hiện tính oxi hóa trong phản ứng nào sau đây?
A. Si + 2F2 → SiF4.
B. Si + O2 SiO2.
C. 2Mg + Si Mg2Si.
D. Si + 2NaOH + H2O → Na2SiO3 + 2H2.
Câu 12: Hòa tan 6,3 gam hỗn hợp Mg và Al trong dung dịch HNO31M đặc nguội dư, thoát ra 6,72 lít khí NO2 (đktc). Khối lượng Al trong hỗn hợp ban đầu là:
A. 5,4g
B. 2,4g.
C. 2,7g.
D. 3,2g.
Câu 13: Khí CO không khử được oxit kim loại nào sau đây ở nhiệt độ cao?
A. Fe3O4.
B. CuO.
C. MgO.
D. PbO.
Câu 14: Vai trò của cacbon trong phản ứng Ca3(PO4)2 + 5C + 3SiO2 3CaSiO3 + 2P + 5CO là:
A. Chất khử
C. Axit
B. Chất oxi hoá
D. Bazơ
Câu 15: SiO2 tan được trong dung dịch axit nào sau đây?
A. HCl
B. HNO3
C. H2SO4
D. HF
Câu 16: Ở điều kiện thường photpho hoạt động hóa học khá hơn nitơ là do
A. Photpho ở trạng thái rắn còn nitơ ở trạng thái khí.
B. Độ âm điện của P nhỏ hơn nitơ.
C. Photpho chỉ có liên kết đơn, còn nitơ có liên kết ba .
D. P có đô âm điện lớn hơn nitơ.
Câu 17: Có thể phân biệt 3 dd : NaCl, Na3PO4, NaNO3 chỉ bằng 1 thuốc thử là
A. dung dịch Ba(OH)2
B. dung dịch AgNO3
C. Cu kim loại
D. dung dịch BaCl2.
Câu 18: Hiện tượng các chất có cấu tạo và tính chất hóa học tương tự nhau, chúng chỉ hơn kém nhau một hay nhiều nhóm metylen (–CH2–) được gọi là hiện tượng
A. đồng phân.
B. đồng vị.
C. đồng đẳng.
D. đồng khối.
Câu 19: Đốt cháy hoàn toàn 3,0 gam một hợp chất hữu cơ X, người ta thu được 4,40 gam CO2 và 1,80 gam H2O. Công thức đơn giản nhất của hợp chất hữu cơ X là:
A. C2H4O. B. C2H5O.
C. CH2O. D. CH2O2.
Câu 20: Cho một số phát biểu về đặc điểm chung của các phân tử hợp chất hữu cơ sau
1. Hợp chất hữu cơ nhất thiết phải chứa C.
2. Có thể chứa nguyên tố khác như Cl, N, P, O,...
3. Liên kết hóa học chủ yếu là liên kết cộng hóa trị.
4. Liên kết hóa học chủ yếu là liên kết ion.
5. Dễ bay hơi, khó cháy.
6. Phản ứng hóa học xảy ra nhanh.
Các câu đúng là
A. 1, 3, 5.
B. 4, 5, 6.
C. 2, 4, 6.
D. 1, 2, 3.
II. TỰ LUẬN (4 điểm)
Câu 1 (2,0 điểm): Hoàn thành chuỗi phản ứng sau (ghi rõ điều kiện, nếu có):
NO NO2 HNO3 Mg(NO3)2 MgO
Câu 2 (1,0 điểm): Hòa tan 15 gam hỗn hợp gồm Al và Cu bằng một lượng vừa đủ dung dịch HNO3 đặc nóng, thu được 20,16 lít khí NO2 (ở đktc, là sản phẩm khử duy nhất) và dung dịch X. Xác định thành phần phần trăm khối lượng của Al và Cu trong hỗn hợp.
Câu 3 (1 điểm): Đốt cháy hoàn toàn 5,6 gam hợp chất hữu cơ A thu được 13,2 gam CO2 và 3,6 gam H2O. Tỉ khối của A so với H2 là 28. Xác định công thức phân tử của chất hữu cơ A.
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 7
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 7)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag =108; Ba = 137)
I. TRẮC NGHIỆM (6 điểm)
Câu 1: Hòa tan hoàn toàn 1,2 gam kim loại X vào dung dịch HNO3 dư thu được 0,224 lít khí N2 ở đktc (sản phẩm khử duy nhất). Kim loại X là
A. Al B. Mg
C. Zn D. Cu
Câu 2: Hai chất nào sau đây là đồng đẳng của nhau?
A. C2H5OH, CH3OCH3.
B. CH3CH2CH2OH, C2H5OH.
C. CH3OCH3, CH3CHO.
D. C4H10, C6H6.
Câu 3: Trong phòng thí nghiệm có thể điều chế N2 bằng cách
A. phân hủy khí NH3.
B. nhiệt phân NaNO2.
C. thủy phân Mg3N2.
D. Đun hỗn hợp NaNO2 và NH4Cl.
Câu 4: Công thức đơn giản nhất là công thức:
A. biểu diễn số lượng nguyên tử của các nguyên tố trong phân tử.
B. biểu thị tỉ lệ tối giản các nguyên tử của các nguyên tố trong phân tử.
C. biểu thị tỉ lệ tối đa các nguyên tử của các nguyên tố trong phân tử.
D. biểu thị tỉ lệ số nguyên tử của các nguyên tố trong phân tử.
Câu 5: Cho 44 gam NaOH vào dung dịch chứa 39,2 gam H3PO4. Sau khi phản ứng xảy ra hoàn toàn. Hỏi những muối nào thu được và khối lượng muối khan thu được là bao nhiêu?
A. Na2HPO4 và 14,2g; Na3PO4 và 49,2g
B. Na3PO4 và 50,0g
C. NaH2PO4 và 49,2g; Na2HPO4 và 14,2g
D. Na2HPO4 và 15,0g
Câu 6: Theo thuyết cấu tạo hoá học, trong phân tử các chất hữu cơ, các nguyên tử liên kết hoá học với nhau theo cách nào sau đây:
A. đúng hoá trị.
B. đúng số oxi hoá.
C. một thứ tự nhất định.
D. đúng hoá trị và theo một thứ tự nhất định
Câu 7: Khí N2 tương đối trơ ở nhiệt độ thường là do
A. Trong phân tử N2 chứa liên kết 3 rất bền.
B. Nguyên tử nitơ có độ âm điện lớn nhất trong nhóm nitơ.
C. Nitơ có bán kính nguyên tử nhỏ, phân tử không phân cực.
D. Trong phân tử N2, mỗi nguyên tử còn một cặp electron chưa tham gia liên kết.
Câu 8: Cho 2,24 lít CO2 (đktc) vào 200 ml dung dịch Ca(OH)2 1M , khối lượng kết tủa thu được là:
A. 10g B. 15g
C. 20g D. 25g
Câu 9: Phương trình hóa học nào viết sai so với phản ứng xảy ra?
A. CaCl2 + CO2 + H2O → CaCO3 + 2HCl
B. FeS + 2HCl → FeCl2 + H2S
C. BaCl2 + H2SO4 → BaSO4 + 2HCl
D. CH3COONa + HCl → CH3COOH + NaCl
Câu 10: Công thức cấu tạo nào sau đây là sai?
A. CH2 = CH2
B. CH ≡ CH
C. CH3 = CH2 – CH3
D. CH3 – CH(CH3) – CH3
Câu 11: Các chất nào trong dãy sau đều là chất hữu cơ?
A. C2H2, C12H22O11, C2H4, NaCN.
B. CH3COOH, C2H5OH, C6H12O6, CO.
C. CH3COOH, CH3COONa, (NH4)2CO3, C6H6.
D. HCOOH, CH4, C6H12O6, CH3COONa.
Câu 12: Tính oxi hóa của C thể hiện ở phản ứng( điều kiện phản ứng coi như có đủ)?
A. C + 2CuO → 2Cu + CO
B. C + H2O → CO+ H2
C. 3C + 4Al → Al4C3
D. C+O2 → CO2
Câu 13: Liên kết hóa học chủ yếu trong hợp chất hữu cơ là
A. liên kết đơn.
B. liên kết cho nhận.
C. liên kết cộng hóa trị.
D. liên kết ion.
Câu 14: Để khắc chữ lên thủy tinh người ta dựa vào phản ứng:
A. SiO2 + 4HF →SiF4 + 2H2O
B. SiO2 + Na2CO3 →Na2SiO3 + CO2
C. SiO2 + 2NaOH →Na2SiO3 + CO2
D. SiO2 + Mg → 2MgO + Si
Câu 15: Dung dịch amoniac trong nước có chứa các ion nào sau đây (bỏ qua sự phân li của nước):
A. \(NH_4^ + \), NH3, \({H^ + }\).
B. \(NH_4^ + \), \(O{H^ - }\).
C. \(NH_4^ + \), NH3.
D.\(NH_4^ + \), NH3, \(O{H^ - }\).
Câu 16: Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2 thu được hỗn hợp khí X (tỉ khối của X so với khí hiđro bằng 18,8). Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là:
A. 11,28g. B. 20,50g.
C. 8,60g. D. 9,40g.
Câu 17: Đánh giá độ dinh dưỡng của phân lân bằng hàm lượng %:
A. H3PO4. B. P.
C. \(PO_4^{3 - }\). D. P2O5.
Câu 18: Số liên kết xích-ma (Ϭ) trong phân tử C4H10 là:
A. 10. B. 13.
C. 12. D. 14.
Câu 19: Kim cương và than chì là các dạng
A. đồng phân của cacbon.
B. thù hình của cacbon.
C. đồng vị của cacbon.
D. đồng hình của cacbon.
Câu 20: Cho phản ứng NaOH + HCl → NaCl + H2O. Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A. 2KOH + FeCl2 → Fe(OH)2 + 2KCl.
B. NaOH + NaHCO3 → Na2CO3 + H2O.
C. KOH + HNO3 → KNO3 + H2O.
D. NaOH + NH4Cl → NaCl + NH3 + H2O.
II. TỰ LUẬN (4 điểm)
Câu 1 (2 điểm): Khi hòa tan hoàn toàn 18,3 gam hỗn hợp Al và Al2O3 trong dung dịch HNO3 10%, thấy thoát ra 6,72 lít khí không màu hóa nâu trong không khí (ở đktc, sản phẩm khử duy nhất) .
a) (1 điểm) Tính thành phần phần trăm về khối lượng trong hỗn hợp trên.
b) (1 điểm) Tính khối lượng dung dịch axit HNO3 cần dùng.
Câu 2 (2 điểm): Một chất hữu cơ X có thành phần khối lượng các nguyên tố là: 54,5% C; 9,1% H; 36,4% O.
a) Tìm công thức đơn giản nhất của X?
b) Biết X có khối lượng phân tử là 88 đvC. Hãy xác định công thức phân tử của X?
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 8
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 8)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag=108; Ba = 137)
I. TRẮC NGHIỆM
Câu 1: Đặc điểm chung của các phân tử hợp chất hữu cơ là
1. thành phần nguyên tố chủ yếu là C và H.
2. có thể chứa nguyên tố khác như Cl, N, P, O.
3. liên kết hóa học chủ yếu là liên kết cộng hoá trị.
4. liên kết hoá học chủ yếu là liên kết ion.
5. dễ bay hơi, khó cháy.
6. phản ứng hoá học xảy ra nhanh.
Nhóm các ý không đúng là:
A. 4, 5, 6. B. 1, 2, 3.
C. 1, 3, 5. D. 1,4,5.
Câu 2: Cho dung dịch amoniac dư vào dung dịch muối FeCl2. Hiện tượng là:
A. Có kết tủa màu trắng xanh không tan.
B. Có kết tủa keo trắng sau đó tan trong NH3 dư.
C. Có kết tủa keo trắng không tan.
D. Có kết tủa màu nâu đỏ không tan.
Câu 3: Để phân biệt 4 lọ mất nhẫn, mỗi lọ chứa một trong các dung dịch sau: (NH4)2SO4, NH4Cl, Na2SO4, NaCl, người ta chỉ cần dùng một thuốc thử duy nhất là
A. BaCl2.
B. HCl.
C. NaOH.
D. Ba(OH)2.
Câu 4: Hiệu ứng nhà kính là hiện tượng Trái Đất đang ấm dần lên, do các bức xạ có bước sóng dài trong vùng hồng ngoại bị giữ lại, mà không bức xạ ra ngoài vũ trụ. Chất khí gây ra hiệu ứng nhà kính là:
A. N2. B. H2.
C. CO2. D. O2.
Câu 5: Glucozơ có nhiều trong quả nho, công thức phân tử là C6H12O6. Công thức đơn giản nhất của glucozơ là
A. CH2O.
B. C2H4O2.
C. C4H8O4.
D. C6H12O6.
Câu 6: Kim loại không phản ứng với axit HNO3 đặc nguội là
A. Ca. B. Al.
C. Ag. D. Cu.
Câu 7: Thuốc muối nabica được dùng trong công nghiệp thực phẩm và dùng làm thuốc chữa đau dạ dày. Công thức hóa học của nabica là
A. CaCO3.
B. Na2CO3.
C. NH4HCO3.
D. NaHCO3.
Câu 8: Dung dịch chất nào sau đây (cùng nồng độ) dẫn điện tốt nhất?
A. K2SO4. B. Al2(SO4)3.
C. NaOH. D. KNO3.
Câu 9: Công thức của phân urê là:
A. (NH2)2CO.
B. (NH2)2CO3.
C. NH4NO3.
D. (NH4)2CO3.
Câu 10: Tính khử của cacbon thể hiện ở phản ứng nào trong các phản ứng sau?
A. 2C + Ca → CaC2.
B. 3C + 4Al → Al4C3.
C. C + 2H2 → CH4.
D. 3C + 2KClO3 → 2KCl+ 3CO2.
Câu 11: Trong các chất sau, chất nào là chất điện li mạnh?
A. HF. B. NaCl.
C. H2O. D. Fe(OH)2.
Câu 12: Nhúng giấy quỳ tím vào dung dịch có pH =12, thì
A. quỳ tím không đổi màu.
B. quỳ tím hoá xanh.
C. quỳ tím hoá đỏ.
D. quỳ tím bị mất màu.
Câu 13: Khí CO2 không thể dùng để dập tắt đám cháy chất nào sau đây?
A. Metan. B. Cacbon.
C. Magie. D. Photpho.
Câu 14: Cặp dung dịch nào sau đây khi trộn với nhau thì có phản ứng trao đổi ion xảy ra?
A. KCl và NaNO3.
B. Na2CO3 và KNO3.
C. Fe2(SO4)3 và HNO3.
D. K2SO4 và Ba(NO3)2.
Câu 15: Cho sơ đồ phản ứng: M + HNO3 → M(NO3)n + X + H2O. X là sản phẩm khử của N. X không thể là chất nào sau đây?
A. NO2. B. NH4NO3.
C. N2O5. D. N2.
Câu 16: Khi nhiệt phân hoàn toàn các muối AgNO3, NaNO3, Zn(NO3)2 thì chất rắn thu được sẽ là:
A. Ag2O, NaNO2, ZnO.
B. Ag, NaNO2, ZnO.
C. A2O, Na2O, ZnO.
D. Ag, NaNO2, Zn.
Câu 17: Người ta điều chế HNO3 bằng phản ứng sau: NH3 → NO → NO2 → HNO3. Khối lượng axit HNO3 thu được từ 0,85 tấn NH3 là (hiệu suất chung của cả quá trình là 90%)
A. 2,835 tấn.
B. 3,150 tấn.
C. 3,500 tấn.
D.1,7955 tấn.
Câu 18: Hoà tan vừa hết 3,6 gam một kim loại M bằng dung dịch HNO3 loãng, dư thu được 6,72 lít khí NO2 (đktc). M là kim loại nào sau đây?
A. Al. B. Cu.
C. Fe. D. Mg.
Câu 19: Dẫn V lít khí (đktc) CO2 vào 100 ml dung dịch Ca(OH)2 1M thu được 6 gam kết tủa và dung dịch A. Lọc bỏ kết tủa và lấy dung dịch A đun nóng thì thu đươc kêt tủa nữa. Giá trị của V là:
A. 3,136.
B. 1,344.
C. 1,344 và 3,136.
D. 3,36 và 1,12.
Câu 20: Phân tích hợp chất hữu cơ X, người ta thu được 54,54% C; 9,10% H và 36,36% O. Công thức đơn giản nhất của X là:
A. C4H10O. B. CH2O.
C. C2H4O. D. C4H8O2.
II. TỰ LUẬN
Câu 1 (2 điểm): Khi hòa tan hoàn toàn 18,3 gam hỗn hợp Al và Al2O3 trong dung dịch HNO3 10%, thấy thoát ra 6,72 lít khí không màu hóa nâu trong không khí (ở đktc, sản phẩm khử duy nhất).
a) Tính thành phần phần trăm về khối lượng trong hỗn hợp trên.
b) Tính khối lượng dung dịch axit HNO3 cần dùng.
Câu 2 (2 điểm): Đốt cháy hoàn toàn 7,4 gam hợp chất hữu cơ X (C, H, O). Thu được 6,72 lít CO2 (đktc) và 5,4 gam H2O. Khi hóa hơi 1,85 gam X, thu được thể tích bằng với thể tích của 0,7 gam N2 cùng nhiệt độ, áp suất. Xác định công thức phân tử của X.
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 9
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 9)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag =108; Ba = 137)
Câu 1: Cho 40 ml dd HCl 0,75M vào 160 ml dung dịch KOH 0,2M thu được 200 ml dung dịch có pH bằng:
A. 10. B. 12.
C. 11. D. 13.
Câu 2: Cho 44 gam NaOH vào dung dịch chứa 39,2 gam H3PO4. Sau khi phản ứng xảy ra hoàn toàn, đem cô cạn dung dịch thu được. Muối được tạo thành và khối lượng tương ứng là:
A. Na3PO4: 50 gam.
B. Na2HPO4: 14,2 gam và Na3PO4: 49,2 gam.
C. Na2HPO4: 15 gam.
D. Na2HPO4: 49,2 gam và Na3PO4: 14,2 gam.
Câu 3: Chất nào sau đây là hiđroxit lưỡng tính?
A. Mg(OH)2. B. Fe(OH)3.
C. KOH. D. Al(OH)3.
Câu 4: Chất nào sau đây là muối axit?
A. CH3COONa. B. Na2HPO4.
C. Na2CO3. D. NH4Cl.
Câu 5: Cho V1 ml dung dịch NaOH có pH = 12. Pha loãng dung dịch này bằng V2 ml nước thu được dung dịch NaOH có pH = 10. Tỉ lệ \(\frac{{{V_1}}}{{{V_2}}}\) là:
A. \(\frac{{100}}{1}\). B. \(\frac{{99}}{1}\).
C. \(\frac{1}{{100}}\). D. \(\frac{1}{{99}}\).
Câu 6: Giá trị pH của dung dịch thu được khi trộn lẫn 200 ml dung dịch NaOH 0,1M với 200 ml dung dịch HNO3 0,3M là (bỏ qua sự điện li của nước)
A. 13. B. 2.
C. 12. D. 1.
Câu 7: Khử 16 gam hỗn hợp gồm Al2O3, Fe2O3, Fe3O4 bằng CO ở nhiệt độ cao, sau phản ứng thu được 11,2 gam chất rắn. Thể tích khí CO (ở đktc) đã tham gia phản ứng là
A. 2,24 lít. B. 3,36 lít.
C. 6,72 lít. D. 8,96 lít.
Câu 8: Cho các phát biểu sau:
(a) Các muối amoni tan trong nước tạo dung dịch chất điện li yếu.
(b) Khí amoniac nhẹ hơn không khí và ít tan trong nước.
(c) Muối amoni tác dụng với dung dịch kiềm, đun nóng thu được khí không mùi.
(d) Khí amoniac làm quì tím ẩm hóa xanh.
Số phát biểu không đúng là
A. 3. B. 2.
C. 4. D. 1.
Câu 9: Nhỏ dung dịch bạc nitrat vào dung dịch natri photphat đựng trong ống nghiệm thì xuất hiện kết tủa màu
A. trắng. B. vàng.
C. đen. D. nâu.
Câu 10: Cho 2,16 gam Mg tác dụng hết với dung dịch HNO3 loãng, dư. Sau khi phản ứng xảy ra hoàn toàn thu được 0,896 lít khí NO (ở đktc) và dung dịch X. Khối lượng muối khan thu được khi cô cạn dung dịch X là
A. 13,32g. B. 13,92g.
C. 6,52g. D. 8,88g.
Câu 11: Cho sơ đồ phản ứng sau: Ca3(PO4)2 X Y Ag3PO4. Cặp chất X, Y lần lượt là:
A. P2O5, Na3PO4.
B. P, H3PO4.
C. H3PO4, Na3PO4.
D. P, P2O5.
Câu 12: Để đề phòng bị nhiễm độc khí CO nên sử dụng mặt nạ phòng độc có chứa
A. đồng (II) oxit.
B. clo.
C. than chì.
D. than hoạt tính.
Câu 13: Thành phần chính của phân supephotphat kép là:
A. CaHPO4.
B. Ca(H2PO4)2 và CaSO4.
C. Ca(H2PO4)2.
D. CaHPO4 và CaSO4.
Câu 14: Cho các phát biểu sau:
(a) Giá trị pH tăng thì tính bazơ của dung dịch tăng và tính axit của dung dịch giảm.
(b) Trong công nghiệp, khí nitơ được sản xuất bằng phương pháp chưng cất phân đoạn không khí lỏng.
(c) Photpho trắng hoạt động hóa học mạnh hơn photpho đỏ.
(d) Phân NPK là phân hỗn hợp.
(e) Khí CO2 gây nên hiệu ứng nhà kính, làm cho trái đất nóng lên.
(g) Than gỗ được dùng để chế tạo thuốc nổ đen, thuốc pháo.
Số phát biểu đúng là:
A. 3. B. 4.
C. 6. D. 5.
Câu 15: Nước đá khô (CO2 rắn) dùng để tạo môi trường lạnh và khô trong việc bảo quản hoa quả tươi vì:
A. nước đá khô có khả năng hút ẩm.
B. nước đá khô có khả năng thăng hoa.
C. nước đá khô có khả năng khử trùng.
D. nước đá khô dễ hoá lỏng.
Câu 16: Cho những cặp chất sau: (1) C và CO, (2) CO2 và dung dịch Ba(OH)2, (3) CO và CaO, (4) CO2 và Al. Các cặp chất không có phản ứng xảy ra là:
A. (1) và (3) B. (2) và (3)
C. (3) và (4) D. (1) và (2)
Câu 17: Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M. Nhỏ từ từ từng giọt cho đến hết 350 ml dung dịch HCl 1M vào 200 ml dung dịch X, tạo thành V lít khí (đktc). Giá trị của V là:
A. 4,48. B. 3,36
C. 2,24. D. 1,12.
Câu 18: Nung 2,23 gam hỗn hợp X gồm các kim loại Fe, Al, Zn, Mg trong oxi, sau một thời gian thu được 2,71 gam hỗn hợp Y. Hòa tan hoàn toàn Y vào dung dịch HNO3 dư thu được 0,672 lít khí NO (đktc) là sản phẩm khử duy nhất. Số mol HNO3 tham gia phản ứng là:
A. 0,18. B. 0,14.
C. 0,16. D. 0,12.
Câu 19: Đốt cháy hoàn toàn 7,4 gam hợp chất hữu cơ X (C, H, O) thu được 6,72 lít CO2 (đktc) và 5,4 gam H2O. Khi hóa hơi 1,85 gam X, thu được thể tích bằng với thể tích của 0,7 gam N2 cùng nhiệt độ, áp suất. Xác định công thức phân tử của X.
A. C5H10O B. C3H6O2
C. C2H2O3 D. C3H6O.
Câu 20: Hợp chất X có công thức đơn giản nhất là CH2O. Tỉ khối hơi của X so với hiđro bằng 30. Công thức phân tử của X là:
A. CH2O B. C2H4O2
C. C3H6O2 D. C4H8O2.
Câu 21: Chất nào sau đây không phân li ra ion khi hòa tan vào nước?
A. Saccarozơ.
B. Axit sunfuric.
C. Natri clorua.
D. Natri hiđroxit.
Câu 22: Cho các chất sau: HCl, NaOH, Na2SO4, NaCl, CH3COOH, KOH, NaBr, H2S, Fe(OH)2. Số chất điện li mạnh là
A. 6. B. 4.
C. 5. D. 7.
Câu 23: Phân tích chất hữu cơ X chứa C, H, O ta có:
mC : mH : mO = 2,24 : 0,357 : 2. Công thức đơn giản nhất của X là:
A. C6H12O4 B. CH3O
C. C3H6O2 D. C3H6O
Câu 24: Liên kết hóa học trong phân tử chất hữu cơ chủ yếu là liên kết
A. cộng hóa trị B. ion
C. kim loại D. hiđro.
Câu 25: Cho từng chất sau: FeO, Fe, Fe3O4, Fe2O3, Fe(NO3)2, Fe(OH)2 lần lượt tác dụng với dung dịch HNO3 đặc, nóng, dư. Số phản ứng oxi hóa-khử xảy ra là:
A. 2. B. 4.
C. 5. D. 3.
Câu 26: Đặc điểm chung của hợp chất hữu cơ là
A. tan trong nước, không tan trong dung môi hữu cơ.
B. nhiêt độ nóng chảy, nhiệt độ sôi cao.
C. liên kết trong phân tử chủ yếu là liên kết ion.
D. thường kém bền với nhiệt và dễ cháy.
Câu 27: Để tách riêng NH3 ra khỏi hỗn hợp gồm N2, H2, NH3 trong công nghiệp người ta đã:
A. cho hỗn hợp qua nước vôi trong dư.
B. cho hỗn hợp qua bột CuO nung nóng.
C. nén và làm lạnh hỗn hợp để hòa lỏng NH3.
D. cho hỗn hợp qua dung dịch H2SO4 đặc.
Câu 28: Muối được làm bột nở trong thực phẩm là
A. (NH4)2CO3. B. Na2CO3.
C. NH4HSO3. D. NH4Cl.
Câu 29: Điều chế NH3 từ hỗn hợp hồm N2 và H2 (tỉ lệ 1∶ 3). Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9. Hiệu suất phản ứng là:
A. 25%. B. 40%.
C. 10%. D. 20%.
Câu 30: “Thủy tinh lỏng” là:
A. silic đioxit nóng chảy.
B. dung dịch đặc của Na2SiO3 và K2SiO3.
C. dung dịch bão hòa của axit silixic.
D. thạch anh nóng chảy.
--- Hết ---
Giám thị không giải thích thêm
Bộ 10 Đề thi Hóa học lớp 11 Học kì 1 năm 2022 tải nhiều nhất - Đề 10
Phòng Giáo dục và Đào tạo ...
Đề thi Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hoá học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 10)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: .............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; K = 39; Cl = 35,5; Ca = 40; P= 31; S = 32; Fe = 56; Cu = 64; Zn = 65; Ag=108; Ba = 137)
Câu 1: Thực hiện các thí nghiệm sau:
(a) Nung NH4NO2 rắn.
(b) Đun nóng NaCl tinh thể với dung dịch H2SO4 (đặc).
(c) Nhỏ HCl vào dung dịch NaHCO3.
(d) Sục khí CO2 vào dung dịch Ca(OH)2 (dư).
(e) Sục khí SO2 vào dung dịch KMnO4.
(g) Cho dung dịch KHSO4 vào dung dịch NaHCO3.
(h) Cho CuS vào dung dịch HCl (loãng).
(i) Cho Na2SO3 vào dd H2SO4 (dư), đun nóng.
Số thí nghiệm sinh ra chất khí là
A. 4. B. 6.
C. 5. D. 2.
Câu 2: Cho 200 ml dung dịch H3PO4 1M tác dụng với 250 ml dung dịch NaOH 2M. Khối lượng muối thu được sau phản ứng là
A. 12,00 gam NaH2PO4 và 14,20 gam Na2HPO4.
B. 16,40 gam Na3PO4.
C. 14,20 gam Na2HPO4 và 16,40 gam Na3PO4.
D. 14,20 gam Na2HPO4.
Câu 3: Cho 4,86 gam kim loại X tác dụng hoàn toàn với HNO3, thu được 4,032 lít NO (ở đktc) là sản phẩm khử duy nhất. Kim loại X là
A. Mg. B. Zn.
C. Al. D. Fe.
Câu 4: Khí amoniac làm giấy quỳ tím ẩm
A. chuyển thành màu xanh.
B. không đổi màu.
C. mất màu.
D. chuyển thành màu đỏ.
Câu 5: Dãy muối nitrat khi nhiệt phân tạo thành oxit kim loại, khí NO2 và O2 là
A. NaNO3, Mg(NO3)2, Cu(NO3)2, AgNO3.
B. Mg(NO3)2, Fe(NO3)3, Pb(NO3)2, AgNO3.
C. Al(NO3)3, Mg(NO3)2, Pb(NO3)2, Cu(NO3)2.
D. KNO3, Mg(NO3)2, Pb(NO3)2, Cu(NO3)2.
Câu 6: Công thức hoá học của supephotphat kép là
A. Ca3(PO4)2.
B. CaHPO4.
C. Ca(H2PO4)2 và CaSO4.
D. Ca(H2PO4)2.
Câu 7: Phản ứng được sử dụng trong việc khắc chữ lên thủy tinh là
A. SiO2 + 2NaOH → Na2SiO3 + CO2.
B. SiO2 + Na2CO3→ Na2SiO3 + CO2.
C. SiO2 + Mg → 2MgO + Si.
D. SiO2 + 4HF → SiF4 + 2H2O.
Câu 8: Dãy các kim loại được điều chế khi dùng CO để khử oxit kim loại tương ứng ở nhiệt độ cao là
A. Fe, Zn, Cu.
B. Fe, Al, Cu.
C. Cu, Ca, Fe.
D. Mg, Zn, Fe.
Câu 9: Đốt cháy hoàn toàn m gam hợp chất hữu cơ X cần vừa đủ 5,04 lít O2 (đktc). Hấp thụ sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được 15 gam kết tủa. Dung dịch còn lại có khối lượng giảm so với khối lượng của dung dịch Ca(OH)2 là 4,8 gam. Tỉ khối hơi của X so với H2 nhỏ hơn 40. Công thức phân tử của X là:
A. C3H4O2. B. C3H8O.
C. C4H8O. D. C3H8O2.
Câu 10: Nung một hợp chất hữu cơ X với lượng dư chất oxi hóa CuO, người ta thu được khí CO2, hơi H2O và khí N2. Kết luận nào sau đây chính xác?
A. X chắc chắn chứa C, H, N và có thể có hoặc không có oxi.
B. X là hợp chất của 3 nguyên tố C, H, N.
C. Chất X chắc chắn có chứa C, H, có thể có N.
D. X là hợp chất của 4 nguyên tố C, H, N, O.
Câu 11: Chọn phát biểu đúng?
A. Giá trị pH tăng thì độ axit giảm.
B. Dung dịch có pH >7 làm quỳ tím hoá đỏ.
C. Dung dịch có pH < 7 làm quỳ tím hoá xanh.
D. Giá trị pH tăng thì độ axit tăng.
Câu 12: Cho phương trình ion: FeS + \({H^ + }\)+ \(SO_4^{2 - }\) → \(F{e^{3 + }}\)+ SO2 + H2O.
Tổng hệ số nguyên tối giản củaphương trình ion này là
A. 30. B. 50.
C. 36. D. 42.
Câu 13: Dãy gồm các chất tác dụng được với dung dịch Ba(HCO3)2 là:
A. HNO3, Ca(OH)2, KHSO4, Mg(NO3)2.
B. NaCl, Na2SO4, Ca(OH)2.
C. HNO3, Ca(OH)2, KHSO4, Na2SO4.
D. HNO3, NaCl, Na2SO4.
Câu 14: Trộn V lít dung dịch H2SO4 0,01M vào 2V lít dung dịch NaOH 0,025M. Giá trị pH của dung dịch thu được bằng:
A. 12. B. 10.
C. 11. D. 8.
Câu 15: Nếu xem toàn bộ quá trình điều chế HNO3 có hiệu suất 80% thì từ 1mol NH3 sẽ thu được một lượng HNO3 là
A. 63,24g. B. 78,75g.
C. 50,40g. D. 55,40g.
Câu 16: Hiện tượng các chất hữu cơ khác nhau nhưng có cùng công thức phân tử gọi là
A. Đồng đẳng.
B. Đồng vị.
C. Đồng khối.
D. Đồng phân.
Câu 17: Dung dịch chất nào sau đây có thể phản ứng được với CaCO3?
A. NaCl.
B. NaNO3.
C. H2SO4.
D. KOH.
Câu 18: Nhiệt phân hoàn toàn 16,8 gam NaHCO3 thu được m gam Na2CO3. Giá trị của m là:
A. 12,4. B. 13,2.
C. 10,6. D. 21,2.
Câu 19: Cho vài giọt dung dịch phenolphtalein vào dung dịch NH3 thì dung dịch chuyển thành:
A. màu hồng B. màu vàng
C. màu xanh D. màu cam
Câu 20: Etilen là một hiđrocacbon có công thức: CH2 = CH2. Số liên kết π (pi) trong một phân tử etilen là:
A. 1. B. 2.
C. 4. D. 3.
Câu 21: Một loại đạm có hàm lượng nguyên tố dinh dưỡng cao, khi bón không làm thay đổi pH của đất đó là urê. Công thức của urê là:
A. KNO3.
B. NH4Cl.
C. NH4NO3.
D. (NH2)2CO.
Câu 22: Hấp thụ hết V lít khí CO2 đo ở đktc bằng dung dịch Ca(OH)2 dư, kết thúc thí nghiệm thu được 5 gam kết tủa. Giá trị của V là
A. 2,24. B. 1,12.
C. 3,36. D. 4,48.
Câu 23: Hòa tan hoàn toàn m gam Fe bằng dung dịch HNO3, dư thu được 1,68 lít khí NO (là sản phẩm khử duy nhất ở đktc). Giá trị của m là:
A. 11,2. B. 4,2.
C. 8,4. D. 5,6.
Câu 24: Sử dụng than củi hoặc than tổ ong để đốt sưởi ấm về mùa đông giá rét, nếu đóng chặt cửa phòng sẽ rất nguy hiểm vì trong quá trình cháy sẽ sinh ra một khí rất độc, có thể gây nôn nao, nếu mạnh hơn có thể gây tử vong do ngạt. Vậy khí đó là gì?
A. CO. B. CO2.
C. NO2. D. H2.
Câu 25: Oxi hóa hoàn toàn 6,15 gam hợp chất hữu cơ X bằng oxi nguyên chất thu được 2,25 gam H2O; 6,72 lít CO2 và 0,56 lít N2 (đkc). Phần trăm khối lượng O trong X xấp xỉ là
A. 26,0%. B. 48,9%
C. 49,9%. D. 59,4%.
Câu 26: Dung dịch Y chứa Ba2+ 0,05 mol; Mg2+ 0,15 mol; \(C{l^ - }\) 0,2 mol; \(HCO_3^ - \) y mol. Đun nóng đến cạn dung dịch Y thu được muối khan có khối lượng là:
A. 24,9 gam.
B. 22,7 gam.
C. 18,7 gam.
D. 23,55 gam.
Câu 27: Kim loại Cu tan trong dung dịch axit HNO3 nhận thấy thoát ra khí X có màu nâu đỏ, là sản phẩm khử duy nhất. Vậy X là:
A. NO. B. NO2.
C. N2. D. N2O.
Câu 28: Phân tích 0,58 gam một hợp chất hữu cơ X (chứa C, H, O) tìm được %C = 62,06; % H = 10,34. Vậy khối lượng oxi trong hợp chất X là
A. 0,08 gam.
B. 0,16 gam.
C. 0,09 gam.
D. 0,14 gam.
Câu 29: Chất khí X gây ra hiệu ứng nhà kính và tham gia vào quá trình quang hợp của cây xanh tạo tinh bột. Chất khí X là
A. O2. B. CO2.
C. N2. D. H2.
Câu 30: Oxi hóa hoàn toàn 7,5 gam hợp chất hữu cơ X bằng oxi nguyên chất thu được 4,5 gam H2O; 4,48 lít CO2 và 1,12 lít N2 (đkc). Phần trăm khối lượng O trong X xấp xỉ là
A. 49,94%. B. 42,66%.
C. 48,96% D. 59,46%.
--- Hết ---
Giám thị không giải thích thêm