Tài liệu Đề thi Giữa kì 2 Hóa học lớp 11 có đáp án năm 2022 (6 đề) tổng hợp từ đề thi môn Hóa học 11 của các trường THPT trên cả nước đã được biên soạn chi tiết giúp học sinh ôn luyện để đạt điểm cao trong bài thi Giữa học kì 2 Hóa học lớp 11. Mời các bạn cùng đón xem:
Đề thi Giữa kì 2 Hóa học lớp 11 có đáp án năm 2022 (6 đề) - Đề 1
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 2
Năm học 2022 - 2023
Bài thi môn: Hóa học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 1)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: ............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; K = 39; Cl = 35,5; Ca = 40; Br = 80; Ag = 108; Ba = 137)
I. TRẮC NGHIỆM (7,5 điểm)
Câu 1: Phản ứng đặc trưng của ankan là phản ứng
A. cộng. B. thế.
C. tách. D. cháy.
Câu 2: Số nguyên tử cacbon trong phân tử pentan là
A. 5. B. 3.
C. 4. D. 6.
Câu 3: C3H8 có tên gọi là
A. propan. B. etan.
C. propin. D. propen.
Câu 4: Ở điều kiện thường, chất nào sau đây tồn tại trạng thái lỏng?
A. CH4. B. C2H6.
C. C8H18. D. C3H8.
Câu 5: Ankan nào sau đây có đồng phân mạch cacbon?
A. Butan. B. Propan.
C. Metan. D. Etan.
Câu 6: Chất nào sau đây không phải là ankan?
A. C3H8. B. C2H2.
C. C2H6. D. CH4.
Câu 7: Anken có công thức tổng quát là
A. CnH2n (n ≥ 1). B. CnH2n (n ≥ 2).
C. CnH2n – 2 (n ≥ 2). D. CnH2n + 2 (n ≥1).
Câu 8: Hiđrocacbon X không làm mất màu dung dịch brom ở nhiệt độ thường. X là chất nào sau đây?
A. benzen B. Etilen
C. propen D. stiren.
Câu 9: Dãy gồm các anken được sắp xếp theo nhiệt độ sôi tăng dần là
A. C2H4, C4H8, C3H6, C5H10.
B. C2H4, C3H6, C4H8, C5H10.
C. C5H10, C4H8, C3H6,C2H4.
D. C2H4, C3H6, C5H10, C4H8.
Câu 10: 1 mol buta-1,3-đien phản ứng tối đa với bao nhiêu mol Br2?
A. 1 mol. B. 3 mol.
C. 2 mol. D. 4 mol.
Câu 11: Hiện nay trong công nghiệp, buta-1,3-đien được điều chế bằng cách
A. tách nước của etanol.
B. đề hiđro hóa butan hoặc butilen.
C. tách HX từ dẫn xuất halogen.
D. hiđro hóa vinylaxetilen.
Câu 12: Đốt cháy hoàn toàn 0,1 mol hiđrocacbon X thu được 0,3 mol CO2. X tác dụng với dung dịch AgNO3/NH3 tạo kết tủa. Công thức cấu tạo của X là
A. CH≡C-CH3. B. CH2=CH-CH3.
C. CH≡CH. D. CH2=CH-C≡CH.
Câu 13: Để làm sạch etilen có lẫn axetilen có thể cho hỗn hợp đi qua dung dịch nào sau đây?
A. Br2.
B. KMnO4.
C. AgNO3/NH3 dư.
D. HBr.
Câu 14: But-2-en có công thức cấu tạo là
A. CH3-CH2-CH2-CH3.
B. CH3-CH=CH-CH3.
C. CH2=CH-CH2-CH3.
D. CH2=CH-CH3.
Câu 15: Số đồng phân cấu tạo mạch hở của C4H8 là
A. 3. B. 4.
C. 2. D. 5.
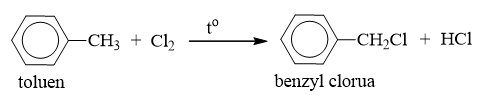
Câu 16: Toluen tác dụng với dung dịch KMnO4 khi đun nóng, thu được sản phẩm hữu cơ là
A. C6H5OK. B. C6H5CH2OH.
C. C6H5CHO. D. C6H5COOK.
Câu 17: Phân tử buta-1,3-đien có
A. hai liên kết đôi cách nhau hai liên kết đơn.
B. hai liên kết đôi cách nhau một liên kết đơn.
C. hai liên kết đôi cạnh nhau.
D. hai liên kết đơn cách nhau một liên kết đôi.
Câu 18: Số nguyên tử hiđro trong phân tử but-1-in là
A. 4. B. 6.
C. 8. D. 10.
Câu 19: Chất nào sau đây có khả năng tác dụng với dung dịch AgNO3/NH3 tạo kết tủa vàng nhạt?
A. Etan. B. Etilen.
C. Metan. D. Axetilen.
Câu 20: Ankan X có tỉ khối hơi so với H2 bằng 29. Công thức phân tử của X là
A. CH4. B. C2H6.
C. C3H8. D. C4H10.
Câu 21: 2,8 gam anken X làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Công thức phân tử của X là
A. C5H10. B. C2H4.
C. C3H6. D. C4H8.
Câu 22: Chất X có công thức cấu tạo CH3-CH(CH3)-CH2-CH3. Tên gọi của X là
A. 2-metylbutan.
B. 3-metylbutan.
C. 2-metylpentan.
D. isobutan.
Câu 23: Khi thực hiện phản ứng đun nóng CH3COONa với vôi tôi xút thu được
A. CH4. B. C2H6.
C. C2H2. D. CO2.
Câu 24: Monoclo hóa propan thu được sản phẩm chính là
A. 2-clopropan.
B. 1-clopropan.
C. 1,2-điclopropan.
D. 2,2- điclopropan.
Câu 25: Hiđrocacbon nào sau đây khi phản ứng với dung dịch brom thu được 1,2-đibrombutan?
A. But-1-en. B. Butan.
C. Buta-1,3-đien. D. But-2-en.
II. TỰ LUẬN (2, 5 ĐIỂM)
Câu 1 (1 điểm): Viết phương trình hóa học của phản ứng xảy ra trong các trường hợp sau:
a) Điều chế C2H4 từ C2H5OH.
b) Trùng hợp C2H4.
c) Dẫn khí C2H2 qua dung dịch AgNO3/NH3.
d) CH4 tác dụng với Cl2/ánh sáng (tỉ lệ 1:1).
Câu 2 (1,5 điểm): Cho 8,6 gam hỗn hợp khí X gồm CH4, C2H4 và C2H2 tác dụng với dung dịch brom (dư) thì khối lượng brom phản ứng là 48 gam. Mặt khác, 13,44 lít X (đktc) tác dụng với lượng dư dung dịch AgNO3 trong NH3 thu được 36 gam kết tủa. Giả sử các phản ứng xảy ra hoàn toàn. Tính phần trăm thể tích của CH4 trong X.
--- Hết ---
Giám thị không giải thích thêm
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
I. TRẮC NGHIỆM
|
1. B |
2. A |
3. A |
4. C |
5. A |
6. B |
7. B |
8. A |
9. B |
10. C |
|
11. B |
12. A |
13. C |
14. B |
15. A |
16. D |
17. B |
18. B |
19. D |
20. D |
|
21. D |
22. A |
23. A |
24. A |
25. A |
|
|
|
|
|
Câu 1
Đáp án B
Phản ứng đặc trưng của ankan là phản ứng thế.
Câu 2
Đáp án A
Công thức phân tử của pentan là C5H12 ⟹ Trong phân tử có 5 nguyên tử cacbon.
Câu 3
Đáp án A
C3H8 có tên gọi là propan.
Câu 4
Đáp án C
Các ankan có số C từ 1 - 4 thì ở thể khí, các ankan tiếp theo ở thể lỏng, từ C18H38 trở đi là các chất rắn.
Câu 5
Đáp án A
Các ankan có số nguyên tử C từ 4 trở lên sẽ có đồng phân mạch cacbon.
Câu 6
Đáp án B
Các ankan có công thức chung dạng CnH2n + 2 nên CH4, C2H6, C3H8 là các ankan.
Câu 7
Đáp án B
Anken có công thức tổng quát là CnH2n với n ≥ 2.
Câu 8
Đáp án A
- Benzen không làm mất màu dung dịch nước brom ở nhiệt độ thường, kể cả khi đun nóng.
- Etilen, propen, stiren làm mất màu dung dịch brom ở nhiệt độ thường vì có liên kết đôi tham gia cộng hợp với brom.
Phương trình hóa học minh họa:
CH2 = CH2 + Br2 → CH2Br – CH2Br
Câu 9
Đáp án B
Nhiệt độ sôi của anken tăng dần theo chiều tăng của phân tử khối.
⟹ Nhiệt độ sôi tăng dần từ C2H4, C3H6, C4H8, C5H10.
Câu 10
Đáp án C
Công thức cấu tạo của buta – 1,3 – đien là: CH2 = CH – CH = CH2.
⟹ Phân tử có 2 liên kết đôi.
⟹ 1 mol buta – 1,3 – đien sẽ phản ứng tối đa với 2 mol Br2.
Câu 11
Đáp án B
Buta-1,3-đien được điều chế bằng cách đề hiđro hóa butan hoặc butilen.
CH3 – CH2 – CH2 – CH3 CH2 = CH – CH = CH2 + 2H2
Câu 12
Đáp án A
Số nguyên tử C trong X là: \(\frac{{{n_{C{O_2}}}}}{{{n_X}}}\)= 3
Mà X tác dụng với dung dịch AgNO3/NH3 tạo kết tủa ⟹ Công thức cấu tạo của X có dạng: CH ≡ C – CH3.
Câu 13
Đáp án C
Để làm sạch etilen có lẫn axetilen có thể cho hỗn hợp đi qua dung dịch AgNO3/NH3 dư vì chỉ có axetilen bị giữ lại, còn etilen không phản ứng thoát ra ngoài.
Phương trình hóa học:
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag + 2NH4NO3
Câu 14
Đáp án B
But-2-en có công thức cấu tạo là CH3-CH=CH-CH3.
Câu 15
Đáp án A
Số đồng phân mạch hở của C4H8 là:
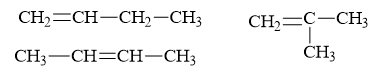
Câu 16
Đáp án D
Phương trình hóa học:
C6H5CH3 + 2KMnO4 C6H5COOK + MnO2 + KOH + H2O
Câu 17
Đáp án B
Công thức cấu tạo của buta – 1,3 – đien là: CH2 = CH – CH = CH2.
⟹ Hai liên kết đôi cách nhau 1 liên kết đơn.
Câu 18
Đáp án B
Công thức cấu tạo của but-1-in là CH ≡ C – CH2 – CH3
⟹ Công thức phân tử là: C4H6.
⟹ Có 6 nguyên tử H trong phân tử.
Câu 19
Đáp án D
Các ank-1-in có khả năng tác dụng với dung dịch AgNO3/NH3.
⟹ Axetilen có khả năng tác dụng với dung dịch AgNO3/NH3 sinh ra kết tủa màu vàng nhạt.
Phương trình hóa học:
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3
Câu 20
Đáp án D
Ankan có X có công thức phân tử là CnH2n + 2 (n ≥ 1).
Mà MX = 2.29 = 58
⟹ 14n + 2 = 58
⟹ n = 4.
Câu 21
Đáp án D
Gọi công thức của anken là CnH2n (n ≥ 2).
Ta có: \({n_{B{r_2}}} = \frac{8}{{160}} = 0,05\,mol\)⟹ nX = 0,05 mol
⟹ 14n = \(\frac{{2,8}}{{0,05}}\)
⟹ n = 4
⟹ Công thức phân tử là C4H8.
Câu 22
Đáp án A
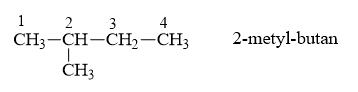
Câu 23
Đáp án A
CH3COONa + NaOH CH4 + Na2CO3
Câu 24
Đáp án A
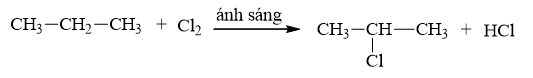
⟹ Sản phẩm chính là 2-clopropan.
Câu 25
Đáp án A
But-1-en phản ứng với dung dịch brom thu được 1,2-đibrombutan.
CH2 = CH – CH2 – CH3 + Br2 → CH2Br – CHBr – CH2 – CH3
II. TỰ LUẬN
Câu 1:
a) C2H5OH CH2 = CH2 + H2O
b)
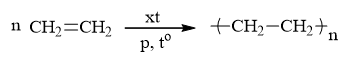
c) CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3
d) CH4 + Cl2 CH3Cl + HCl
Câu 2:
Gọi số mol của CH4, C2H4 và C2H2 trong 8,6 gam hỗn hợp lần lượt là x, y, z mol.
Theo bài ta có:
\(\left\{ \begin{array}{l}16x + 28y + 26z = 8,6\\y + 2z = \frac{{48}}{{160}}\\k.(x + y + z) = \frac{{13,44}}{{22,4}}\\kz = \frac{{36}}{{240}}\end{array} \right.\)
\( \Rightarrow \left\{ \begin{array}{l}16x + 28y + 2z = 8,6\\y + 2z = 0,3\\\frac{{x + y + z}}{z} = \frac{{0,6}}{{0,15}}\end{array} \right.\)
\( \Rightarrow \left\{ \begin{array}{l}x = 0,2\\y = 0,1\\z = 0,1\end{array} \right.(mol)\)
Phần trăm thể tích của CH4 là:
%CH4 = \(\frac{x}{{x + y + z}}.100\% = \frac{{0,2}}{{0,2 + 0,1 + 0,1}}.100\% = 50\% \)
Đề thi Giữa kì 2 Hóa học lớp 11 có đáp án năm 2022 (6 đề) - Đề 2
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 2
Năm học 2022 - 2023
Bài thi môn: Hóa học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 2)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: ............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; K = 39; Cl = 35,5; Ca = 40; Br = 80; Ag = 108; Ba = 137)
Câu 1: Công thức cấu tạo thu gọn của buta-1,3-đien là
A. CH2=CH-CH=CH2.
B. CH3-CH=CH-CH3.
C. CH2=C=CH-CH3.
D. CH≡C-CH=CH2.
Câu 2: Phần trăm khối lượng cacbon trong phân tử ankan X bằng 82,76%. Công thức phân tử của X là
A. C2H6. B. C4H10.
C. CH4. D. C5H12.
Câu 3: Hiđrocacbon nào sau đây thuộc dãy đồng đẳng anken?
A. C2H4. B. C2H2.
C. C2H6. D. C3H8.
Câu 4: Cho các chất sau: metan, propen, but-2-in và axetilen. Kết luận nào sau đây là đúng?
A. Cả 4 chất đều có khả năng làm mất màu dung dịch nước brom
B. Có 2 chất tạo kết tủa với dung dịch bạc nitrat trong amoniac
C. Có 3 chất có khả năng làm mất màu dung dịch nước brom
D. Cả 4 chất đều làm mất màu dung dịch thuốc tím
Câu 5: Biết rằng 0,1 lít khí etilen (đktc) làm mất màu tối đa 50 ml dung dịch nước brom. Nếu dùng 0,1 lít khí axetilen (đktc) thì có thể làm mất màu tối đa bao nhiêu ml dung dịch nước brom trên?
A. 50 ml. B. 200 ml.
C. 25 ml. D. 100 ml
Câu 6: Ankylbenzen X có phần trăm khối lượng cacbon bằng 90,566%. Số đồng phân cấu tạp của X là
A. 2 B. 3
C. 4 D. 5
Câu 7: Khi đốt cháy hoàn toàn một ankan bất kì thì tạo ra
A. số mol CO2 lớn hơn số mol H2O.
B. không xác định được.
C. số mol CO2 bằng số mol H2O
D. số mol H2O lớn hơn số mol CO2.
Câu 8: Đốt cháy hoàn toàn hỗn hợp 3 ankin A, B, C thu được 3,36 lít CO2 (đktc) và 1,8 gam H2O. Vậy số mol hỗn hợp ankin bị đốt cháy là
A. 0,05 mol B. 0,1 mol
C. 0,15 mol D. 0,25mol
Câu 9: Hiđrocacbon X có tỉ khối đối với không khí xấp xỉ 3,173. Ở nhiệt độ thường, X không làm mất màu nước brom. Khi đun nóng, X làm mất màu dung dịch KMnO4. X là
A. benzen
B. etylbenzen
C. toluen
D. stiren.
Câu 10: Anken nào sau đây có đồng phân hình học
A. pent-1-en
B. 2-metylbut-2-en
C. pent-2-en
D. 3-metylbut-1-en
Câu 11: Đốt cháy hoàn toàn 0,15 mol hỗn hợp 2 ankan thu được 9,45 gam H2O. Cho sản phẩm cháy vào dung dịch Ca(OH)2 dư thì khối lượng kết tủa thu được là
A. 42,5 gam
B. 15,0 gam
C. 37,5 gam
D. 52,5 gam
Câu 12: Dãy đồng đẳng của ankan có công thức chung là
A. CnH2n-2 (n ≥ 2)
B. CnH2n (n ≥ 2)
C. CnH2n-6 (n ≥ 6)
D. CnH2n+2 (n ≥ 1)
Câu 13: Đốt cháy hoàn toàn m gam hỗn hợp X gồm CH4, C3H6, C4H6, C3H4 thu được 17,6 gam CO2 và 10,8 gam H2O. m có giá trị là
A. 4 gam B. 2 gam
C. 8 gam D. 6 gam
Câu 14: Stiren không có khả năng phản ứng với
A. Brom khan có Fe xúc tác
B. dung dịch KMnO4
C. dung dịch brom
D. dung dịch AgNO3/NH3
Câu 15: Liên kết đôi do những liên kết nào hình thành?
A. Hai liên kết π
B. Liên kết σ và π
C. Hai liên kết σ
D. Liên kết σ
Câu 16: Dẫn 4,48 lít (đktc) hỗn hợp khí X gồm propin và but-2-in cho qua bình dựng dung dịch AgNO3/NH3 thấy có 14,7 gam kết tủa màu vàng. Thành phần % thể tích của mỗi khí trong X là
A. C3H4 80% và C4H6 20%.
B. C3H4 50% và C4H6 50%.
C. C3H4 33% và C4H6 67%.
D. C3H4 25% và C4H6 75%.
Câu 17: Chất nào sau đây có khả năng tác dụng với dung dịch AgNO3/NH3 tạo kết tủa vàng nhạt?
A. Etan. B. Etilen.
C. Metan. D. Axetilen.
Câu 18: X có tỉ khối hơi so với H2 bằng 29. Công thức phân tử của X là
A. CH4. B. C2H6.
C. C3H8. D. C4H10.
Câu 19: Khi thực hiện phản ứng đun nóng CH3COONa với vôi tôi xút thu được
A. CH4. B. C2H6.
C. C2H2. D. CO2.
Câu 20: 2,8 gam anken X làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Công thức phân tử của X là
A. C5H10. B. C2H4.
C. C3H6. D. C4H8.
Câu 21: Dãy gồm các anken được sắp xếp theo nhiệt độ sôi tăng dần là
A. C2H4, C4H8, C3H6, C5H10.
B. C2H4, C3H6, C4H8, C5H10.
C. C5H10, C4H8, C3H6,C2H4.
D. C2H4, C3H6, C5H10, C4H8.
Câu 22: 1 mol buta-1,3-đien phản ứng tối đa với bao nhiêu mol Br2?
A. 1 mol. B. 3 mol.
C. 2 mol. D. 4 mol.
Câu 23: Hiện nay trong công nghiệp, buta-1,3-đien được điều chế bằng cách
A. tách nước của etanol.
B. đề hiđro hóa butan hoặc butilen.
C. tách HX từ dẫn xuất halogen.
D. hiđro hóa vinylaxetilen.
Câu 24: Đốt cháy hoàn toàn 0,1 mol hiđrocacbon X thu được 0,3 mol CO2. X tác dụng với dung dịch AgNO3/NH3 tạo kết tủa. Công thức cấu tạo của X là:
A. CH≡C-CH3.
B. CH2=CH-CH3.
C. CH≡CH.
D. CH2=CH-C≡CH.
Câu 25: Ankan X có phần trăm khối lượng cacbon bằng 80%. Công thức phân tử của ankan X là:
A. CH4. B. C2H6.
C. C3H8. D. C4H10.
Câu 26: Phát biểu nào sau đây không đúng?
A. Các anken không tan trong nước nhưng tan tốt trong dầu mỡ.
B. Etien được điều chế bằng cách đun C2H5OH với H2SO4 đặc ở 170oC.
C. Trong công nghiệp, anken được được điều chế từ phản ứng tách H2 của ankan.
D. Nhiệt độ nóng chảy của các anken giảm dần khi số nguyên tử cacbon tăng dần.
Câu 27: Sản phẩm chính trong phản ứng giữa but-1-en với hiđro bromua là
A. CH3-CH2-CHBr-CH2Br.
B. CH2Br-CH2-CH2-CH2Br.
C. CH3-CH2-CHBr-CH3.
D. CH3-CH=CH-CH2Br.
Câu 28: Trùng hợp hiđrocacbon X thu được polibutađien (cao su buna). X là
A. but-1-en.
B. but-2-en.
C. buta-1,3-đien.
D. but-2-in.
Câu 29: Cho CaC2 vào H2O thu được khí
A. CH4. B. C2H2.
C. C2H4. D. CO2.
Câu 30: Cho 0,15 mol C2H2 phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được m gam kết tủa. Giá trị của m là
A. 24,0. B. 21,6.
C. 10,8. D. 36.
--- Hết ---
Giám thị không giải thích thêm
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
|
1. A |
2. B |
3. A |
4. C |
5. D |
6. C |
7. D |
8. A |
9. C |
10. C |
|
11. C |
12. D |
13. D |
14. D |
15. B |
16. B |
17. D |
18. D |
19. A |
20. D |
|
21. B |
22. C |
23. B |
24. A |
25. B |
26. D |
27. C |
28. C |
29. B |
30. D |
Câu 1
Đáp án A
Công thức cấu tạo thu gọn của buta-1,3-đien là CH2 = CH – CH = CH2.
Câu 2
Đáp án B
Gọi công thức ankan là CnH2n + 2 với n ≥ 1.
Theo bài ta có:
\(\frac{{12n}}{{14n + 2}}.100 = 82,76\)
⇒ n = 4
⇒ Công thức phân tử của ankan là C4H10.
Câu 3
Đáp án A
Dãy đồng đẳng của anken có công thức chung là CnH2n với n ≥ 2.
Câu 4
Đáp án C
Công thức cấu tạo của các chất:
Metan: CH4
Propen: CH2 = CH – CH3
But – 2 – in: CH3 – C ≡ C – CH3
Axetilen: CH ≡ CH
A sai vì chỉ có 3 chất đều có khả năng làm mất màu dung dịch nước brom là propen, but-2-in và axetilen.
B sai vì chỉ có 1 chất tạo kết tủa với dung dịch bạc nitrat trong amoniac là axetilen.
C đúng.
D sai vì có 3 chất đều làm mất màu dung dịch thuốc tím là propen, but-2-in và axetilen.
Câu 5
Đáp án D
Ta có: 1 phân tử etilen sẽ phản ứng với 1 phân tử brom.
Nhưng 1 phân tử axetilen sẽ phản ứng được với 2 phân tử brom.
Khi đó: 0,1 lít khí etilen (đktc) làm mất màu tối đa 50 ml dung dịch nước brom.
Vậy 0,1 lít khí axetilen (đktc) thì có thể làm mất màu tối đa 50.2 = 100 ml dung dịch nước brom.
Câu 6
Đáp án C
Gọi công thức của ankylbenzen là \({C_n}{H_{2n - 6}}\) với n ≥ 6.
Theo bài ta có: \(\frac{{12.n}}{{14n - 6}}.100 = 90,566\)⟹ n = 8
⟹ Công thức phân tử của X là C8H10
Các đồng phân của X là:
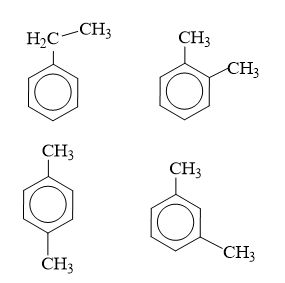
⟹ Có 4 đồng phân.
Câu 7
Đáp án D
Phương trình đốt cháy ankan:
CnH2n + 2 + (\(\frac{{3n + 1}}{2}\)) O2 n CO2 + (n + 1) H2O
⇒ Khi đốt cháy hoàn toàn một ankan bất kì thì tạo ra số mol H2O lớn hơn số mol CO2.
Câu 8
Đáp án A
Ta có: \({n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15\,mol\); \({n_{{H_2}O}} = \frac{{1,8}}{{18}} = 0,1\,mol\)
⇒ \({n_{hh\,\,ankin}} = {n_{C{O_2}}} - {n_{{H_2}O}}\)= 0,15 – 0,1 = 0,05 mol
Câu 9
Đáp án C
Ở nhiệt độ thường X không làm mất màu nước brom. Khi đun nóng, X làm mất màu dung dịch KMnO4 ⇒ X là ankylbenzen.
⇒ Công thức của X có dạng CnH2n – 6 với n ≥ 6.
Mà MX = 29. 3,173 = 92
⇒ 14n – 6 = 92
⇒ n = 7
⇒ X là toluen.
Câu 10
Đáp án C
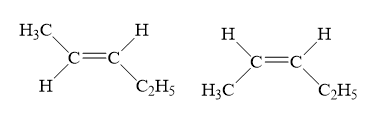
Anken có đồng phân hình học khi có dạng:
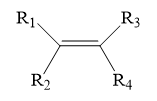 với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)
với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)
⇒ pent-2-en có đồng phân hình học.
Câu 11
Đáp án C
Ta có: \({n_{{H_2}O}} = \frac{{9,45}}{{18}} = 0,525\,mol\)
⇒ \({n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}\)
⇒ \({n_{C{O_2}}} = {n_{{H_2}O}} - {n_{Ankan}}\)= 0,525 – 0,15 = 0,375 mol
⇒ \({n_{CaC{O_3} \downarrow }} = {n_{C{O_2}}} = 0,375\,mol\)
⇒ \({m_ \downarrow }\)= 0,375 .100 = 37,5 gam
Câu 12
Đáp án D
Dãy đồng đẳng của ankan có công thức chung là: CnH2n+2 (n ≥ 1).
Câu 13
Đáp án D
Ta có: \({n_{C{O_2}}} = \frac{{17,6}}{{44}} = 0,4\,mol\); \({n_{{H_2}O}} = \frac{{10,8}}{{18}} = 0,6\,mol\)
⇒ nC = 0,4 mol; nH = 0,6.2 = 1,2 mol
⇒ mX = mC + mH = 0,4.12 + 1,2.1 = 6 gam
Câu 14
Đáp án D
Công thức cấu tạo của stiren: C6H5 – CH = CH2.
⇒ Stiren không có khả năng phản ứng với dung dịch AgNO3/NH3 vì không có liên kết ba ở đầu mạch.
Câu 15
Đáp án B
Liên kết đôi là do một liên kết σ và một liên kết π tạo thành.
Câu 16
Đáp án B
Phương trình phản ứng:
CH ≡ C – CH3 + AgNO3 + NH3 ⟶ Ag – C ≡ C – CH3↓ + NH4NO3
Ta có: \({n_{hh\,\,X}} = \frac{{4,48}}{{22,4}} = 0,02\,mol\)
\({n_{propin}} = {n_ \downarrow } = \frac{{14,7}}{{147}} = 0,1\,mol\)
⇒ nbut-2-in = 0,2 – 0,1 = 0,1 mol
⇒ %C3H4 = %C4H6 = 50%
Câu 17
Đáp án D
Axetilen có khả năng tác dụng với dung dịch AgNO3/NH3 tạo kết tủa vàng nhạt.
Phương trình hóa học:
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3
Câu 18
Đáp án D
Ta có: MX = 29.2 = 58
⇒ X có công thức phân tử là C4H10.
Câu 19
Đáp án A
CH3COONa (r) + NaOH CH4 + Na2CO3
⟹ X là khí CH4.
Câu 20
Đáp án D
Gọi công thức của anken có dạng CnH2n với n ≥ 2.
\({n_{anken}} = {n_{B{r_2}}} = \frac{8}{{160}} = 0,05\,mol\)
⇒ 14n = \(\frac{{2,8}}{{0,05}} = 56\)
⇒ n = 4
⇒ Công thức phân tử của anken là C4H8.
Câu 21
Đáp án B
Nhiệt độ sôi của các anken tăng dần khi số C tăng dần.
⇒ Dãy gồm các anken được sắp xếp theo nhiệt độ sôi tăng dần là C2H4, C3H6, C4H8, C5H10.
Câu 22
Đáp án C
Công thức cấu tạo của buta-1,3-đien là: CH2 = CH – CH = CH2.
⇒ có 2 liên kết π.
⇒ 1 mol buta-1,3-đien phản ứng tối đa với 2 mol Br2.
Câu 23
Đáp án B
Hiện nay trong công nghiệp, buta-1,3-đien được điều chế bằng cách đề hiđro hóa butan hoặc butilen.
CH3 – CH2 – CH2 – CH3 CH2 = CH – CH = CH2 + 2H2
Câu 24
Đáp án A
Số nguyên tử C trong X là \(\frac{{{n_{C{O_2}}}}}{{{n_X}}} = \frac{{0,3}}{{0,1}} = 3\)
Mà X tác dụng với dung dịch AgNO3/NH3 tạo kết tủa ⇒ X có dạng ank-1-in.
⇒ Công thức cấu tạo của X là CH ≡ C – CH3.
Câu 25
Đáp án B
Gọi công thức của ankan có dạng là CnH2n + 2 với n ≥ 1.
⇒ \(\frac{{12n}}{{14n + 2}}.100 = 80\)
⇒ n = 2
⇒ Công thức của ankan X là C2H6.
Câu 26
Đáp án D
D sai vì nhiệt độ nóng chảy của các anken tăng dần khi số nguyên tử cacbon tăng dần.
Câu 27
Đáp án C
Phương trình hóa học:
CH2 = CH – CH2 – CH3 + HBr ⟶ CH3 – CHBr – CH2 – CH3
Câu 28
Đáp án C
Trùng hợp buta-1,3-đien thu được polibutađien (cao su buna).
Phương trình hóa học:
n CH2 = CH – CH = CH2 (– CH2 – CH = CH – CH2 –)n
Câu 29
Đáp án B
Phương trình hóa học:
CaC2 + 2H2O → C2H2 + Ca(OH)2
Câu 30
Đáp án D
Phương trình hóa học:
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3
⇒ \({n_ \downarrow } = {n_{{C_2}{H_2}}} = 0,15\,mol\)
⇒ \({m_ \downarrow }\)= 0,15.240 = 36 gam
Đề thi Giữa kì 2 Hóa học lớp 11 có đáp án năm 2022 (6 đề) - Đề 3
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 2
Năm học 2022 - 2023
Bài thi môn: Hóa học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 3)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: ............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; K = 39; Cl = 35,5; Ca = 40; Br = 80; Ag = 108; Ba = 137)
Câu 1: Chất nào sau đây là ankan?
A. C6H6. B. C2H6.
C. C4H6. D. C3H6.
Câu 2: Chất nào sau đây có đồng phân mạch cacbon?
A. CH4. B. C2H6.
C. C3H8. D. C4H10.
Câu 3: Ankan có khả năng tham gia phản ứng
A. thế với halogen.
B. cộng với hiđro.
C. trùng hợp.
D. thủy phân.
Câu 4: Anken có công thức tổng quát là
A. CnH2n + 2 (n ≥ 2).
B. CnH2n (n ≥ 2).
C. CnH2n – 2 (n ≥ 3).
D. CnH2n – 6 (n ≥ 6).
Câu 5: Số đồng phân ankin có công thức phân tử C4H6 là
A. 4. B. 2.
C. 3. D. 5.
Câu 6: Ankan X có tỉ khối hơi so với H2 bằng 15. Công thức phân tử của X là
A. CH4. B. C2H6.
C. C3H8. D. C4H10.
Câu 7: Trong các chất dưới đây, chất nào có nhiệt độ sôi thấp nhất?
A. Etan. B. Propan.
C. Butan. D. Pentan.
Câu 8: Cho propan tác dụng với brom (chiếu sáng, tỉ lệ mol 1:1), sản phẩm chính thu được là
A. 1-brompropan.
B. 2-brompropan.
C. 2,2-đibrompropan.
D. 2,3-đibrompropan.
Câu 9: Sản phẩm chủ yếu trong hỗn hợp thu được khi cho toluen phản ứng với brom theo tỷ lệ mol 1 : 1 (có một bột sắt) là
A. Benzybromua.
B. o-bromtoluen và p-bromtoluen.
C. p-bromtoluen và m-bromtoluen.
D. o-bromtoluen và m-bromtoluen.
Câu 10: Trong phòng thí nghiệm, metan được điều chế bằng phương pháp nào sau đây?
A. Nung natri axetat với vôi tôi xút.
B. Chưng cất từ dầu mỏ.
C. Tổng hợp trực tiếp từ cacbon và hiđro.
D. Cracking butan.
Câu 11: Trong công nghiệp, etien được điều chế bằng cách:
A. tách nước từ ancol etylic.
B. tách hiđro từ etan.
C. đun nóng natri axetat khan với hỗn hợp vôi tôi xút.
D. cho canxi cacbua tác dụng với nước.
Câu 12: Phản ứng nào dưới đây không đúng qui tắc Mac-côp-nhi-côp?
A. CH3CH=CH2 + HCl → CH3CHClCH3.
B. CH3CH2CH=CH2 + H2O → CH3CH2CH(OH)CH3.
C. (CH3)2C=CH2 + HBr → (CH3)2CH-CH2Br.
D. (CH3)2C=CH-CH3 + HCl → (CH3)2CClCH2CH3.
Câu 13: Đốt cháy hoàn toàn một hiđrocacbon X thu được 8,8 gam CO2 và 3,6 gam H2O. X có công thức phân tử là
A. CH4. B. C2H6.
C. C2H4. D. C2H2.
Câu 14: Ankylbenzen X có phần trăm khối lượng cacbon bằng 90,566%. Số đồng phân cấu tạo của X là
A. 2 B. 3
C. 4 D. 5
Câu 15: Cho axetilen tác dụng với H2O/HgSO4 (80oC) tạo thành sản phẩm có tên là
A. ancol etylic.
B. axeton.
C. anđehit axetic.
D. axit axetic.
Câu 16: Biết 4 gam ankin X làm mất màu dung dịch chứa tối đa 32 gam brom. Công thức phân tử của X là
A. C5H8. B. C2H2.
C. C3H4. D. C4H6.
Câu 17: Để phân biệt toluen, benzen, stiren chỉ cần dùng dung dịch
A. NaOH B. HCl
C. Br2 D. KMnO4
Câu 18: Etilen có tên gọi khác là
A. eten. B. axetilen.
C. etan. D. propen.
Câu 19: Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch KMnO4?
A. CH4. B. C2H4.
C. C3H8. D. C4H10.
Câu 20: Phát biểu nào sau đây về tính chất vật lí của anken là sai?
A. Không tan trong nước và nhẹ hơn nước.
B. Nhiệt độ sôi tăng theo chiều tăng của phân tử khối.
C. Tan nhiều trong nước và trong dầu mỡ.
D. Từ C2H4 đến C4H8 là chất khí ở điều kiện thường.
Câu 21: Isopren có công thức cấu tạo là
A. CH2=CH–CH=CH2.
B. CH2=C=CH2.
C. CH2=C=CH – CH3.
D. CH2=C(CH3)-CH=CH2.
Câu 22: Trime hóa axetilen thu được sản phẩm là
A. C2H6. B. C2H4.
C. C6H6. D. C4H4.
Câu 23: Cho các chất sau: metan, axetilen, etilen, pent-1-in và but-2-in. Số chất tác dụng được với dung dịch AgNO3/NH3 tạo kết tủa là
A. 4. B. 3.
C. 1. D. 2.
Câu 24: Đốt cháy hoàn toàn ankin X thu được 3,36 lít CO2 (đktc) và 1,8 gam H2O. Số mol ankin phản ứng là
A. 0,15. B. 0,25.
C. 0,08. D. 0,05.
Câu 25: Khi cho 2-metylbutan phản ứng với Cl2 (chiếu sáng, tỉ lệ mol 1:1) thu được sản phẩm chính là
A. 1-clo-2-metylbutan.
B. 2-clo-2-metylbutan.
C. 2-clo-3-metylbutan.
D. 1-clo-3-metylbutan.
Câu 26: Trong phòng thí nghiệm, cho canxi cacbua tác dụng với nước thu được chất khí nào sau đây?
A. Metan B. Etilen
C. Axetilen D. Buta-1,3-đien
Câu 27: Phần trăm khối lượng cacbon trong phân tử ankan X bằng 82,76%. Công thức phân tử của X là:
A. C2H6. B. C4H10.
C. CH4. D. C5H12.
Câu 28: Hỗn hợp khí X gồm H2 và C3H6 có tỷ khối so với H2 là 9. Hỗn hợp X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với H2 là 11,25. Hiệu suất của phản ứng hiđro hóa là
A. 90% B. 80%
C. 50% D. 60%
Câu 29: Anken nào sau đây có đồng phân hình học?
A. pent-1-en B. 2-metylbut-2-en
C. pent-2-en D. 3-metylbut-1-en
Câu 30: Hiđrocacbon X là đồng đẳng của benzen có công thức phân tử dạng (C3H4)n. X có công thức phân tử nào dưới đây:
A. C12H16 B. C9H12
C. C15H20 D. C6H8.
--- Hết ---
Giám thị không giải thích thêm
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
|
1. B |
2. D |
3. A |
4. B |
5. B |
6. B |
7. A |
8. B |
9. B |
10. A |
|
11. B |
12. C |
13. C |
14. C |
15. C |
16. C |
17. D |
18. A |
19. B |
20. C |
|
21. D |
22. C |
23. D |
24. D |
25. B |
26. C |
27. B |
28. C |
29. B |
30. B |
Câu 1
Đáp án B
Ankan có công thức chung là \({C_n}{H_{2n + \,2}}\)với n ≥ 1.
⟹ C2H6 là ankan.
Câu 2
Đáp án D
Các ankan có từ 4 nguyên tử C trở lên sẽ có đồng phân mạch cacbon.
Câu 3
Đáp án A
Ankan có khả năng tham gia phản ứng thế với halogen.
Ví dụ:
CH4 + Cl2 CH3Cl + HCl
Câu 4
Đáp án B
Anken có công thức tổng quát là CnH2n (n ≥ 2).
Câu 5
Đáp án B
Các đồng phân ankin có công thức phân tử C4H6 là:
CH≡C-CH2-CH3 và CH3-C≡C-CH3.
Vậy có tất cả 2 đồng phân ankin có công thức phân tử C4H6.
Câu 6
Đáp án B
Ankan có X có công thức phân tử là CnH2n + 2 (n ≥ 1).
Mà MX = 2.15 = 30
⟹ 14n + 2 = 30
⟹ n = 2.
⟹ Công thức của X là C2H6.
Câu 7
Đáp án A
Nhiệt độ sôi của ankan thì tăng dần theo chiều tăng của số nguyên tử cacbon vì khối lượng phân tử tăng dần.
⟹ Trong 4 đáp án thì etan có nhiệt độ sôi thấp nhất.
Câu 8
Đáp án B
Phương trình hóa học:
CH3 – CH2 – CH3 + Br2 CH3 – CHBr – CH3 + HBr
Câu 9
Đáp án B
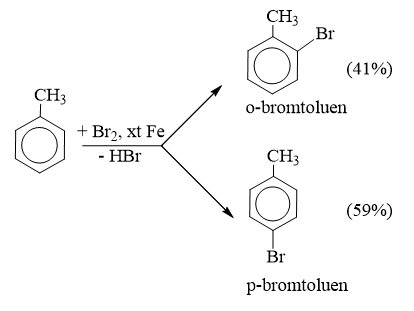
Câu 10
Đáp án A
Trong phòng thí nghiệm, metan được điều chế bằng phương pháp nung natri axetat với vôi tôi xút.
Phương trình hóa học:
CH3COONa + NaOH CH4 + Na2CO3
Câu 11
Đáp án B
Trong công nghiệp, etien được điều chế bằng cách tách hiđro từ etan.
C2H6 C2H4 + H2
Câu 12
Đáp án C
Quy tắc Mac-cop-nhi-cop: Trong phản ứng cộng HX vào liên kết bội, nguyên tử H ưu tiên cộng vào nguyên tử cacbon bậc thấp hơn, còn nguyên tử hay nhóm nguyên tử X ưu tiên cộng vào nguyên tử cacbon bậc cao hơn.
⟹ Phản ứng C cộng không theo quy tắc Maccopnhicop.
Câu 13
Đáp án C
\({n_{{H_2}O}} = \frac{{3,6}}{{18}} = 0,2\,mol\); \({n_{C{O_2}}} = \frac{{8,8}}{{44}} = 0,2\,mol\)
⟹ Tỉ lệ C : H = 0,2 : 0,4 = 1 : 2
⟹ Công thức đơn giản nhất của X là CH2.
⟹ Công thức phân tử là C2H4
Câu 14
Đáp án C
Gọi công thức của ankylbenzen là \({C_n}{H_{2n - 6}}\) với n ≥ 6.
Theo bài ta có: \(\frac{{12.n}}{{14n - 6}}.100 = 90,566\)⟹ n = 8
⟹ Công thức phân tử của X là C8H10.
Các đồng phân của X là:
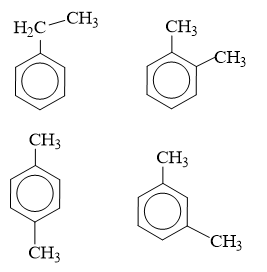
⟹ Có 4 đồng phân.
Câu 15
Đáp án C
CH ≡ CH + H2O CH3CHO
Câu 16
Đáp án C
Gọi công thức phân tử của ankin là \({C_n}{H_{2n - 2}}\)với n ≥ 2.
\({n_{B{r_2}}} = \frac{{32}}{{160}} = 0,2\,mol\) ⟹ \({n_{ankin}} = \frac{{{n_{B{r_2}}}}}{2} = 0,1\,mol\)
⟹ 14n – 2 = \(\frac{4}{{0,1}} = 40\)
⟹ n = 3
⟹ Công thức của ankin là C3H4.
Câu 17
Đáp án D
Để phân biệt toluen, benzen, stiren chỉ cần dùng dung dịch KMnO4.
Hiện tượng:
- Làm mất màu dung dịch KMnO4 ngay nhiệt độ thường là stiren.
- Làm mất màu dung dịch KMnO4 khi đun nóng là toluen.
- Không làm mất màu dung dịch KMnO4 kể cả khi đun nóng là benzen.
Câu 18
Đáp án A
Etilen (CH2 = CH2) có tên gọi khác là eten.
Câu 19
Đáp án B
Ở điều kiện thường, chất có liên kết π kém bền sẽ làm mất màu dung dịch KMnO4.
⟹ C2H4 làm mất màu dung dịch KMnO4.
Câu 20
Đáp án C
C sai vì anken không tan trong nước.
Câu 21
Đáp án D
Isopren có công thức cấu tạo là:
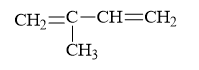
Câu 22
Đáp án C
3C2H2 C6H6
Câu 23
Đáp án D
Các ank-1-in có phản ứng với dung dịch AgNO3/NH3 tạo kết tủa.
⟹ Axetilen, pent-1-in có phản ứng với dung dịch AgNO3/NH3 tạo kết tủa.
Câu 24
Đáp án D
\({n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15\,mol\); \({n_{{H_2}O}} = \frac{{1,8}}{{18}} = 0,1\)mol
⟹ \({n_{ankin}} = 0,15 - 0,1 = 0,05\,mol\)
Câu 25
Đáp án B
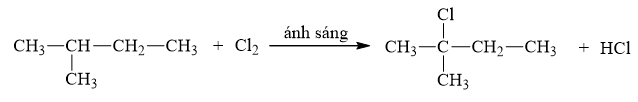
⟹ Sản phẩm chính là 2-clo-2-metylbutan.
Câu 26
Đáp án C
Trong phòng thí nghiệm, cho canxi cacbua tác dụng với nước thu được chất khí axetilen
Phương trình hóa học:
CaC2 + 2H2O → Ca(OH)2 + C2H2 ↑
Câu 27
Đáp án B
Gọi công thức của ankan X là \({C_n}{H_{2n + 2}}\)với n ≥ 1.
Theo bài: \(\frac{{12n}}{{14n + 2}}.100 = 82,76\) ⟹ n = 4.
⟹ Công thức của ankan X là C4H10.
Câu 28
Đáp án C
\(\frac{{{n_{{H_2}}}}}{{{n_{{C_3}{H_6}}}}} = \frac{{42 - 9.2}}{{9.2 - 2}} = \frac{3}{2}\)⟹ Hiệu suất tính theo C3H6.
Ta có: mX = mY ⟹ \(\frac{{{n_X}}}{{{n_Y}}} = \frac{{{{\overline M }_Y}}}{{{{\overline M }_X}}} = \frac{{11,25.2}}{{9.2}} = \frac{5}{4}\)
Giả sử: nX = 5 mol; nY = 4 mol ⟹ Ở hỗn hợp X: \({n_{{H_2}}} = 3\,mol\); \({n_{{C_3}{H_6}}} = 2\,mol\)
⟹ \({n_{{C_3}{H_6}\,pu}} = {n_{{H_2}\,pu}} = {n_X} - {n_Y}\)= 5 – 4 = 1 mol
⟹ H = \(\frac{{{n_{{C_3}{H_6}\,pu}}}}{{{n_{{C_3}{H_6}}}}}.100\% = \frac{1}{2}.100\% = 50\% \)
Câu 29
Đáp án B
Anken có đồng phân hình học khi có dạng:
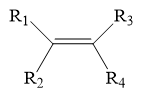 với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)
với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)
⟹ pent-2-en có đồng phân hình học.
Câu 30
Đáp án B
Gọi công thức của X có dạng \({C_m}{H_{2m - 6}}\) với m ≥ 6.
⟹ 14m – 6 = 40n và m = 3n
⟹ n = 3
⟹ Công thức phân tử của X là C9H12
Đề thi Giữa kì 2 Hóa học lớp 11 có đáp án năm 2022 (6 đề) - Đề 4
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 2
Năm học 2022 - 2023
Bài thi môn: Hóa học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 4)
(Thí sinh không được sử dụng tài liệu)
Họ, tên thí sinh: ..................................................................... Lớp: ............................
(Cho H = 1; C = 12; N = 14; O = 16; Na = 23; K = 39; Cl = 35,5; Ca = 40; Br = 80; Ag = 108; Ba = 137)
Câu 1: Ở điều kiện thường, chất nào sau đây tồn tại trạng thái lỏng?
A. CH4. B. C2H6.
C. C8H18. D. C3H8.
Câu 2: Ankan nào sau đây có đồng phân mạch cacbon?
A. Butan. B. Propan.
C. Metan. D. Etan.
Câu 3: Chất nào sau đây không phải là ankan?
A. C3H8. B. C2H2.
C. C2H6. D. CH4.
Câu 4: Anken có công thức tổng quát là
A. CnH2n (n ≥ 1). B. CnH2n (n ≥ 2).
C. CnH2n – 2 (n ≥ 2). D. CnH2n + 2 (n ≥ 1).
Câu 5: Quy tắc Mac-côp-nhi-côp được áp dụng trong phản ứng nào sau đây?
A. Cộng Br2 vào anken đối xứng.
B. Cộng HX vào anken đối xứng.
C. Trùng hợp anken.
D. Cộng HX vào anken bất đối xứng.
Câu 6: But-2-en có công thức cấu tạo là
A. CH3-CH2-CH2-CH3.
B. CH3-CH=CH-CH3.
C. CH2=CH-CH2-CH3.
D. CH2=CH-CH3.
Câu 7: Số đồng phân cấu tạo mạch hở của C4H8 là
A. 3. B. 4.
C. 2. D. 5.
Câu 8: Số nguyên tử hiđro trong phân tử vinyl axetilen là
A. 4. B. 6.
C. 8. D. 10.
Câu 9: Chất nào sau đây có khả năng tác dụng với dung dịch AgNO3/NH3 tạo kết tủa vàng nhạt?
A. Etan. B. Etilen.
C. Metan. D. Axetilen.
Câu 10: X có tỉ khối hơi so với H2 bằng 29. Công thức phân tử của X là
A. CH4. B. C2H6.
C. C3H8. D. C4H10.
Câu 11: Khi thực hiện phản ứng đun nóng CH3COONa với vôi tôi xút thu được
A. CH4. B. C2H6.
C. C2H2. D. CO2.
Câu 12: 2,8 gam anken X làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Công thức phân tử của X là
A. C5H10. B. C2H4.
C. C3H6. D. C4H8.
Câu 13: Dãy gồm các anken được sắp xếp theo nhiệt độ sôi tăng dần là:
A. C2H4, C4H8, C3H6, C5H10.
B. C2H4, C3H6, C4H8, C5H10.
C. C5H10, C4H8, C3H6, C2H4.
D. C2H4, C3H6, C5H10, C4H8.
Câu 14: 1 mol buta-1,3-đien phản ứng tối đa với bao nhiêu mol Br2?
A. 1 mol. B. 3 mol.
C. 2 mol. D. 4 mol.
Câu 15: Đốt cháy 6,72 lít (đktc) hỗn hợp gồm hai hiđrocacbon X và Y (MY > MX) thu được 11,2 lít CO2 (đktc) vào 10,8 gam H2O. Công thức của X là
A.C2H6 B. C2H4
C. CH4 D. C2H2
Câu 16: Đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol CO2 bằng số mol H2O. Thành phần phần trăm về số mol của X và Y trong hỗn hợp M lần lượt là
A. 75% và 25% B. 20% và 80%
C. 35% và 65% D. 50% và 50%
Câu 17: Hỗn hợp khí X gồm 0,1 mol C2H2 ; 0,2 mol C2H4 và 0,3 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 11. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,1 B. 0,2
C. 0,4 D. 0,3
Câu 18: Ba hiđrocacbon X,Y, Z là đồng đẳng kế tiếp, khối lượng phân tử của Z bằng 2 lần khối lượng phân tử của X. Các chất X, Y , Z thuộc dãy đồng đẳng:
A. ankan B. Ankađien
C. anken D. ankin
Câu 19: Dãy đồng đẳng benzen có công thức chung là
A.CnH2n+2 B. CnH2n-2
C. CnH2n-4 D. CnH2n-6
Câu 20: Công thức phân tử của toluen là
A.C6H6 B. C7H8
C. C8H8 D. C8H10
Câu 21: Benzen tác dụng với Cl2 có ánh sáng, thu được hexaclorua. Công thức của hexaclorua là
A.C6H6Cl2 B. C6H6Cl6
C. C6H5Cl D. C6H6Cl4
Câu 22: Chất nào sau đây làm mất màu dung dịch KMnO4 khi đun nóng?
A. benzen B. Toluen
C. 3 propan D. metan
Câu 23: Đốt cháy hoàn toàn 5,3 gam ankybenzen X thu được 8,96 lít CO2 (đktc). Công thức phân tử của X là
A. C6H6 B. C7H8
C. C8H8 D. C8H10
Câu 24: Chất nào sau đây có đồng phân hình học?
A. CH3CH2CH2CH3
B. CH3CH2CH=CH2.
C. CH3CH=CHCH3
D.CH3C≡CH3
Câu 25: Cho 3,36 lít (đktc) hỗn hợp gồm etan và etilen đi chậm qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,10 B. 0,10 và 0,05
C. 0,12 và 0,03 D.0,03 và 0,12
Câu 26: Đốt cháy hoàn toàn V lít (đktc) hỗn hợp X gồm CH4, C2H4 thu được 0,15 mol CO2 và 0,2 mol H2O. Giá trị của V là
A. 2,24 B. 3,36
C. 4,48 D. 1,68
Câu 27: Hỗn hợp khí X gồm H2 và C3H6 có tỷ khối so với H2 là 9. Hỗn hợp X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với H2 là 11,25. Hiệu suất của phản ứng hiđro hóa là
A. 90% B. 80%
C. 50% D. 60%
Câu 28: Công thức phân tử của etylbenzen là
A.C6H6 B. C7H8
C. C8H8 D. C8H10
Câu 29: Hiđrocacbon X có chứa vòng benzen, X không thể là
A.C8H10 B. C6H4
C. C8H8 D. C7H8
Câu 30: Toluen tác dụng với Cl2, ánh sáng (tỉ lệ mol 1 : 1 ), thu được sản phẩm hữu cơ là
A. o-clotoluen B. p-clotoluen.
C. phenyl clorua D. Benzyl clorua
--- Hết ---
Giám thị không giải thích thêm
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
|
1. C |
2. A |
3. B |
4. B |
5. D |
6. B |
7. A |
8. A |
9. D |
10. D |
|
11. A |
12. D |
13. B |
14. C |
15. C |
16. D |
17. B |
18. C |
19. D |
20. B |
|
21. B |
22. B |
23. D |
24. C |
25. B |
26. A |
27. C |
28. D |
29. B |
30. D |
Câu 1
Đáp án C
Ở nhiệt độ thường, các ankan có số C từ 18 trở lên sẽ ở thể lỏng.
Câu 2
Đáp án A
Các ankan từ C1 đến C3 không có đồng phân. Từ C4 trở đi có đồng phân mạch cacbon.
Câu 3
Đáp án B
Các ankan có công thức tổng quát là CnH2n + 2 với n ≥ 1.
⇒ C2H2 không phải là ankan.
Câu 4
Đáp án B
Công thức tổng quát của anken là CnH2n với n ≥ 2.
Câu 5
Đáp án D
Quy tắc Mac-côp-nhi-côp được áp dụng trong phản ứng cộng HX vào anken bất đối xứng.
Câu 6
Đáp án B
But-2-en có công thức cấu tạo là CH3-CH=CH-CH3.
Câu 7:
Đáp án A
Ta có: \(k = \frac{{4.2 - 8 + 2}}{2} = 1\)
⇒ Đồng phân anken
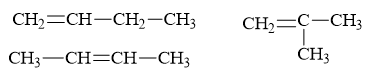
Câu 8:
Đáp án A
Công thức cấu tạo của vinyl axetilen là CH ≡ C – CH = CH2.
⇒ Có 4 nguyên tử H.
Câu 9
Đáp án D
Chất có khả năng tác dụng với dung dịch AgNO3/NH3 tạo kết tủa vàng nhạt.
⇒ Chất này có dạng là ank-1-in.
⇒ Axetilen thỏa mãn.
Phương trình hóa học:
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3
Câu 10
Đáp án D
Ta có: MX = 29.2 = 58 đvC
⇒ X là C4H10.
Câu 11
Đáp án A
Phương trình hóa học:
CH3COONa (r) + NaOH CH4 + Na2CO3
⟹ X là khí CH4.
Câu 12
Đáp án D
Gọi công thức của anken có dạng CnH2n với n ≥ 2.
\({n_{anken}} = {n_{B{r_2}}} = \frac{8}{{160}} = 0,05\,mol\)
⇒ 14n = \(\frac{{2,8}}{{0,05}} = 56\)
⇒ n = 4
⇒ Công thức phân tử của anken là C4H8.
Câu 13
Đáp án B
Nhiệt độ sôi của các anken tăng dần khi số C tăng dần.
⇒ Dãy gồm các anken được sắp xếp theo nhiệt độ sôi tăng dần là C2H4, C3H6, C4H8, C5H10.
Câu 14
Đáp án C
Công thức cấu tạo của buta-1,3-đien là: CH2 = CH – CH = CH2.
⇒ có 2 liên kết π.
⇒ 1 mol buta-1,3-đien phản ứng tối đa với 2 mol Br2.
Câu 15
Đáp án C
Ta có: \({n_{hh}} = \frac{{6,72}}{{22,4}} = 0,3\,mol\)
\({n_{C{O_2}}} = \frac{{11,2}}{{22,4}} = 0,5\,mol\); \({n_{{H_2}O}} = \frac{{10,8}}{{18}} = 0,6\,mol\)
Số \(\overline C \)của hỗn hợp khí là: \(\overline C = \frac{{{n_{C{O_2}}}}}{{{n_{hh}}}} = \frac{{0,5}}{{0,3}} = 1,67 < 2\)
⇒ Khí X là CH4.
Câu 16
Đáp án D
Gọi công thức tổng quát của ankan và ankin lần lượt là CnH2n +2 (với n ≥ 1) và CmH2m – 2 (với n ≥ 2).
Khi đốt ankan: \({n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}\)(1)
Khi đốt cháy ankin: \({n_{ankin}} = {n_{C{O_2}}} - {n_{{H_2}O}}\)(2)
(1) – (2) ⇒ nankan – nankin = \(\sum {{n_{{H_2}O}}} - \sum {{n_{C{O_2}}}} \)
Khi đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol CO2 bằng số mol H2O.
⇒ nankin = nankan
⇒ %nankin = %nankan = 50%
Câu 17
Đáp án B
Áp dụng bảo toàn khối lượng:
mY = mX = 0,1.26. + 0,2.28 + 0,3.2 = 8,8 (gam)
Mà MY = 11.2 = 22 ⇒ nY = \(\frac{{8,8}}{{22}}\) = 0,4 mol
Số mol H2 tham gia phản ứng là:
nX – nY = (0,1 + 0,2 + 0,3) – 0,4 = 0,2 mol
Ta có:\({n_{{H_2}}}\)phản ứng + \({n_{B{r_2}}}\)= \(2{n_{{C_2}{H_2}}} + {n_{{C_2}{H_4}}}\)
⇒ \({n_{B{r_2}}}\)= 2.0,1 + 0,2 - 0,2 = 0,2 mol
Câu 18
Đáp án C
Phân tử Z hơn phân tử X 2 nhóm CH2 ⇒ MZ = MX + 28
Theo bài: MZ = 2MX ⇒ MX + 28 = 2MX
⇒ MX = 28
⇒ X là C2H4 (anken)
⇒ X, Y, X thuộc dãy đồng đẳng anken.
Câu 19
Đáp án D
Dãy đồng đẳng benzen có công thức chung là CnH2n – 6 (n ≥ 6).
Câu 20
Đáp án B
Công thức của toluen là C6H5-CH3.
⇒ Công thức phân tử của toluen là C7H8.
Câu 21
Đáp án B
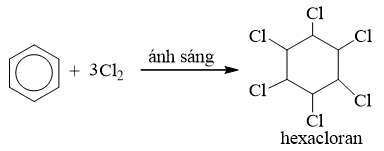
Câu 22
Đáp án B
Toluen làm mất màu dung dịch KMnO4 khi đun nóng.
Phương trình hóa học:
C6H5CH3 + 2KMnO4 C6H5COOK + 2MnO2 + KOH + H2O
Câu 23
Đáp án D
Gọi công thức của ankylbenzen là \({C_n}{H_{2n - 6}}\) với n ≥ 6.
Ta có: \({n_{C{O_2}}} = \frac{{8,96}}{{22,4}} = 0,4\,mol\) ⇒ \({n_X} = \frac{{0,4}}{n}\,\,(mol)\)
⇒ 14n – 6 = \(\frac{{5,3}}{{\frac{{0,4}}{n}}} = \frac{{53n}}{4}\)
⇒ n = 8
⇒ Công thức phân tử của X là C8H10.
Câu 24
Đáp án C
Anken có đồng phân hình học khi có dạng:
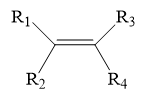 với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)
với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)
⇒ CH3CH=CHCH3 có đồng phân hình học.
Câu 25
Đáp án B
Ta có: \({n_{hh}} = \frac{{3,36}}{{22,4}} = 0,15\,mol\)
Khối lượng bình brom tăng chính là khối lượng của etilen vì chỉ có etilen phản ứng với brom.
⇒ \({m_{{C_2}{H_4}}}\)= 2,8 gam ⇒ \({m_{{C_2}{H_4}}} = \frac{{2,8}}{{28}} = 0,1\,mol\)
⇒ \({n_{{C_2}{H_6}}}\)= 0,15 - 0,1 = 0,05 mol
Câu 26
Đáp án A
Ta có: \({n_{C{H_4}}} = {n_{{H_2}O}} - {n_{C{O_2}}}\)= 0,2 - 0,15 = 0,05 mol
Bảo toàn nguyên tố C: \[{n_{C{H_4}}}\; + {\rm{ }}2{n_{{C_2}{H_4}}}{\rm{ = }}{n_{C{O_2}}}\]
⇒ \({n_{{C_2}{H_4}}}\)= 0,05 mol
⇒ V = 22,4.(0,05 + 0,05) = 2,24 lít
Câu 27
Đáp án C
Ta có: \(\frac{{{n_{{H_2}}}}}{{{n_{{C_3}{H_6}}}}} = \frac{{42 - 9.2}}{{9.2 - 2}} = \frac{3}{2}\)⟹ Hiệu suất tính theo C3H6.
Mà mX = mY ⟹ \(\frac{{{n_X}}}{{{n_Y}}} = \frac{{{{\overline M }_Y}}}{{{{\overline M }_X}}} = \frac{{2.11,25}}{{2.9}} = \frac{5}{4}\)
Giả sử, nX = 5, nY = 4 ⟹ Trong hỗn hợp X chứa \({n_{{H_2}}} = 3\,mol\); \({n_{{C_3}{H_6}}} = 2\,mol\)
⟹ \({n_{{C_3}{H_6}\,pu}}\) = nX – nY = 5 – 4 = 1 mol
⟹ H = \[\frac{1}{2}.100\% = 50\% \]
Câu 28
Đáp án D
Công thức của etylbenzen là C6H5-CH2CH3.
⇒ Công thức phân tử của etylbenzen là C8H10.
Câu 29
Đáp án B
Hiđrocacbon X có chứa vòng benzen, X không thể là C6H4 vì riêng vòng benzen đã chứa 3π + 1 vòng nên nếu có 6C thì số H phải là 6.
Câu 30
Đáp án D