Tailieumoi.vn giới thiệu Giải bài tập Hóa Học lớp 11 Bài 5: Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li chính xác, chi tiết nhất giúp học sinh dễ dàng làm bài tập Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li lớp 11.
Giải bài tập Hóa Học lớp 11 Bài 5: Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li
Câu hỏi và bài tập (trang 22 sgk Hóa học lớp 11)
Bài 1 trang 22 sgk Hóa học 11: Viết phương trình điện li của các chất sau : K2S, Na2HPO4, NaH2PO4, Pb(OH)2, HBrO, HF, HClO4.
Lời giải
Phương trình điện li :
a) K2S → 2K++ S2-
b) Na2HPO4 → 2Na++ HPO42-
HPO42- H++PO43-
c) NaH2PO4 → Na++ H2PO4-
H2PO4- H++ HPO42-
HPO42- H++ PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơ
H2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H++ BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.
Bài 2 trang 22 sgk Hóa học 11: Một dung dịch có [H+] = 0,010M. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm ? Hãy cho biết màu của quỳ tím trong dung dịch này.
[H+]= 1,0.10-2M
[OH-] = 1,0.10-14/[H+] = 1,0.10-14/1,0.10-2 = 1,0 . 10-12 M
pH = -log [H+] = -log(1,0.10-2) = 2
Vậy dung dịch này là axit, quỳ tím trong dung dịch này có màu đỏ.
Bài 3 trang 22 sgk Hóa học 11: Một dung dịch có pH = 9,0. Tính nồng độ mol của các ion H+ và OH- trong dung dịch. Hãy cho biết màu của phenolphtalein trong dung dịch này.
Bài 4 trang 22 sgk Hóa học 11: Viết các phương trình phân tử và ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau :
a) Na2CO3 + Ca(NO3)2
b) FeSO4 + NaOH (loãng)
c) NaHCO3 + HCl
d) NaHCO3+ NaOH
e) K2CO3+ NaCl
g) Pb(OH)2 (r) + HNO3
h) Pb(OH)2 (r) + NaOH
i) CuSO4 + Na2S
Phương trình ion rút gọn :
a) Na2CO3 + Ca(NO3)2 2NaNO3 + CaCO3
Ca2+ + CO32- → CaCO3 ↓
b) FeSO4 + 2NaOH Fe(OH)2 + Na2SO4
Fe2+ + 2OH- → Fe(OH)2↓
c) NaHCO3 + HCl NaCl + CO2 + H2O
HCO3- + H+ → CO2 ↑ + H2O
d) NaHCO3 + NaOH Na2CO3 + H2O
HCO3- + OH- → H2O + CO32-
e) K2CO3 + NaCl không phản ứng
g) Pb(OH)2 + 2HNO3 Pb(NO3)2 + 2H2O
Pb(OH)2(r) + 2H+ → Pb2+ + 2H2O
h) Pb(OH)2 + 2NaOH Na2PbO2 + 2H2O
Pb(OH)2(r) + 2OH- → PbO22- + 2H2O
i) CuSO4 + Na2S CuS + Na2SO4
Cu2+ + S2- → CuS↓.
Bài 5 trang 22 sgk Hóa học 11: Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
A. các chất phản ứng phải là những chất dễ tan.
B. các chất phản ứng phải là những chất điện li mạnh.
C. một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng
D. phản ứng không phải là thuận nghịch.
Bài 6 trang 23 sgk Hóa học 11: Kết tủa CdS (hình 1,7a) được tạo thành trong dung dịch bằng cặp chất nào dưới đây ?

A. CdCl2 + NaOH
B. Cd(NO3)2 + H2S
C. Cd(NO3)2 + HCl
D. CdCl2 + Na2SO4
Cd(NO3)2 + H2S → CdS + 2HNO3
Đáp án B
Bài 7 trang 23 sgk Hóa học 11: Viết phương trình hoá học (dưới dạng phân tử và ion rút gọn) của phản ứng trao đổi ion trong dung dịch tạo thành từng kết tủa sau : Cr(OH)3 ; Al(OH)3 ; Ni(OH)2 (hình 1.7 b, c, d).
Lời giải
Cr(NO3)3 + 3NaOH (vừa đủ) → Cr(OH)3↓ + 3NaNO3 ;
=> Cr3+ + 3OH- → Cr(OH)3↓
AlCl3 + 3KOH (vừa đủ) → Al(OH)3↓ + 3KCl ;
=> Al3+ + 3OH- → Al(OH)3↓
Ni(NO3)2 + 2NaOH → Ni(OH)2↓+ 2NaNO3
=> Ni2+ + 2OH- → Ni(OH)2↓
Lý thuyết luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li.
1. Thuyết axit - bazơ của A-rê-ni-út.
- Axit là chất khi tan trong nước phân li ra ion H+.
- Bazơ là những chất khi tan trong nước phân li ra ion OH-
- Hiđroxit lưỡng tính khi tan trong nước vừa có thể phân li như axit vừa phân li như bazơ.
- Hầu hết các muối khi tan trong nước, điện li hoàn toàn ra cation kim loại (hoặc cation NH4+) và anion gốc axit.
+ Nếu gốc axit còn chứa hiđro có tính axit, thì gốc đó điện li yếu ra cation H+ và anion gốc axit.
2. Tích số ion của nước
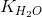 = [H+].[OH-] = l,0.10-14(ở 25°C).
= [H+].[OH-] = l,0.10-14(ở 25°C).
- Nó là hằng số trong nước cũng như trong dung dịch loãng của các chất khác nhau.
3. Giá trị [H+] và pH đặc trưng cho các môi trường
- Môi trường trung tính: [H+] = 10-7 M hay pH = 7,0
- Môi trường axit: [H+] > 10-7 M hay pH < 7,0
- Môi trường kiềm: [H+] < 10-7 M hay pH > 7,0
4. Điểu kiện xảy ra phản ứng trao đổi ion trong dung dịch
- Tạo thành chất kết tủa.
- Tạo thành chất điện li yếu.
- Tạo thành chất khí.
5. Phương trình ion rút gọn cho biết bản chất của phản ứng trong dung dịch các chất điện li.
Trong phương trình ion rút gọn của phản ứng, người ta lược bỏ những ion không tham gia phản ứng. Còn những chất kết tủa, điện li yếu, chất khí được giữ nguyên dưới dạng phân tử.