Lời giải bài tập Khoa học tự nhiên lớp 7 Bài 7: Hóa trị và công thức hóa học sách Chân trời sáng tạo hay, ngắn gọn sẽ giúp học sinh dễ dàng trả lời câu hỏi KHTN 7 Bài 7 từ đó học tốt môn Khoa học tự nhiên 7.
Giải bài tập KHTN lớp 7 Bài 7: Hóa trị và công thức hóa học
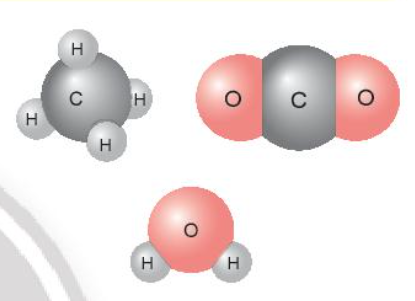
Trả lời:
- Các nguyên tử liên kết với nhau theo nguyên tắc hóa trị: trong phân tử hợp chất 2 nguyên tố, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia
- Để lập được công thức hóa học của các chất:
+ Xác định công thức hóa học dựa vào phần trăm nguyên tố và khối lượng phân tử
+ Xác định công thức hóa học dựa vào quy tắc hóa trị
1. Hóa trị
Phương pháp giải:
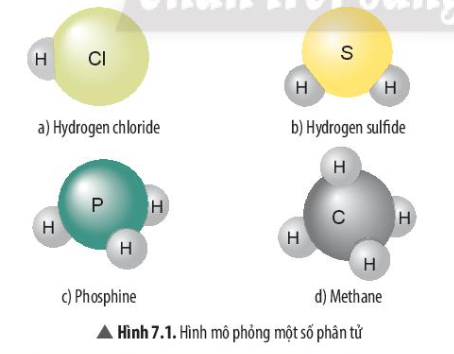
Quan sát Hình 7.1, đếm số nguyên tử H liên kết với các nguyên tử Cl, S, P, C trong phân tử
Trả lời:
- Phân tử hydrogen chloride: 1 nguyên tử Cl liên kết với 1 nguyên tử H
- Phân tử hydrogen sulfur: 1 nguyên tử S liên kết với 2 nguyên tử H
- Phân tử phosphine: 1 nguyên tử P liên kết với 3 nguyên tử H
- Phân tử methane: 1 nguyên tử C liên kết với 4 nguyên tử H
Phương pháp giải:
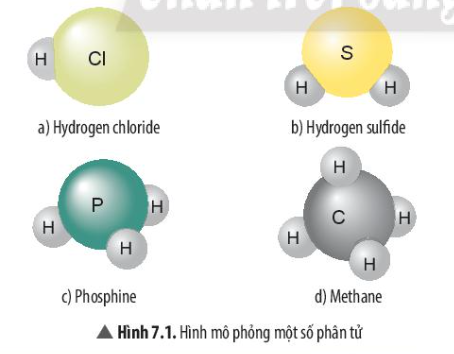
Người ta quy ước nguyên tố H luôn có hóa trị I. Nguyên tử của nguyên tố khác liên kết được với bao nhiêu nguyên tử H thì nguyên tố đó có hóa trị bằng bấy nhiêu
Trả lời:
- Nguyên tử Cl liên kết với 1 nguyên tử H => Cl hóa trị I
- Nguyên tử S liên kết với 2 nguyên tử H => S hóa trị II
- Nguyên tử P liên kết với 3 nguyên tử H => P hóa trị III
Phương pháp giải:
Tham khảo ví dụ 1 trang 46: Nguyên tử C có hóa trị IV, có thể liên kết với 4 nguyên tử H hoặc liên kết với 2 nguyên tử O
Trả lời:
- Nguyên tử X có hóa trị IV
=> 1 nguyên tử X có khả năng liên kết với 2 nguyên tử O hoặc 4 nguyên tử H

Phương pháp giải:
Trong phân tử silicon dioxide có 1 nguyên tử Si, 2 nguyên tử O
Trả lời:
- 1 nguyên tử O góp chung 2 electron
=> 2 nguyên tử O góp chung 4 electron
- 1 nguyên tử S liên kết với 2 nguyên tử O
=> Si góp chung 4 electron
=> Nguyên tố Silicon có hóa trị IV
- Ứng dụng của silicon dioxide
+ Sản xuất kính cửa sổ, lọ thủy tinh
+ Lọc nước, xử lí nước tinh khiết
+ Sản xuất xi măng
+ Sản xuất đồ gốm
+ Góp phần sản xuất xà phòng và chất nhuộm màu
2. Quy tắc hóa trị
Phương pháp giải:
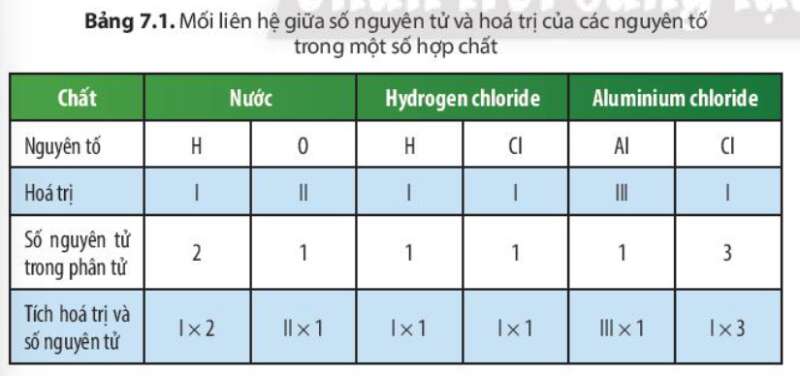
- So sánh tích hóa trị và số nguyên tử của 2 nguyên tố
Trả lời:
- Xét phân tử nước: I x 2 = II x 1
=> Tích hóa trị và số nguyên tử H = Tích hóa trị và số nguyên tử O
- Xét phân tử hydrogen chloride: I x 1 = I x 1
=> Tích hóa trị và số nguyên tử H = Tích hóa trị và số nguyên tử Cl
- Xét phân tử aluminium chloride: III x 1 = I x 3
=> Tích hóa trị và số nguyên tử Al = Tích hóa trị và số nguyên tử Cl
Phương pháp giải:
Quy tắc hóa trị: Trong phân tử hợp chất hai nguyên tố, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia
Trả lời:
- Xét nguyên tố Ca và Cl: 1 nguyên tử Ca có hóa trị II liên kết với a nguyên tử Cl có hóa trị I
=> Áp dụng quy tắc hóa trị: II x 1 = I x a
=> a = 2
=> 1 nguyên tử Ca liên kết với 2 nguyên tử Cl
- Xét nguyên tố Ca và O: 1 nguyên tử Ca có hóa trị II liên kết với b nguyên tử O có hóa trị II
=> Áp dụng quy tắc hóa trị: II x 1 = II x b
=> b = 1
=> 1 nguyên tử Ca liên kết với 1 nguyên tử O
3. Công thức hóa học
Câu hỏi thảo luận 4 trang 47 KHTN lớp 7: Dựa vào Ví dụ 2, em hãy hoàn thành bảng sau:
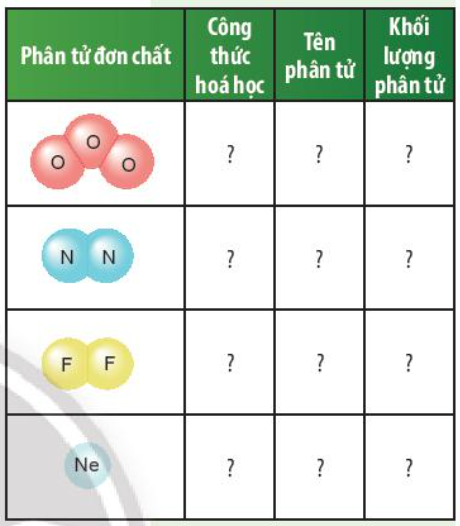
Phương pháp giải:
Ví dụ 2: Phân tử khí hydrogen được tạo thành từ 2 nguyên tử hydrogen liên kết với nhau
=> Công thức hóa học của phân tử khí hydrogen là H2
=> Công thức hóa học của đơn chất được biểu diễn bằng kí hiệu nguyên tố hóa học kèm với chỉ số ghi ở bên dưới. Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử
Trả lời:
Phương pháp giải:
- Đối với đơn chất kim loại, hạt hợp thành là nguyên tử nên kí hiệu hóa học của nguyên tố kim loại được coi là công thức hóa học của đơn chất kim loại
- Với 1 số đơn chất phi kim ở thể rắn, quy ước công thức hóa học là kí hiệu nguyên tố
Trả lời:
- Đơn chất kim loại
+ Sodium: Na
+ Copper: Cu
+ Iron: Fe
+ Potassium: K
- Đơn chất phi kim:
+ Carbon: C
+ Sulfur: S
+ Phosphorus: P
+ Silicon: Si
Câu hỏi thảo luận 6 trang 48 KHTN lớp 7: Em hãy hoàn thành bảng sau
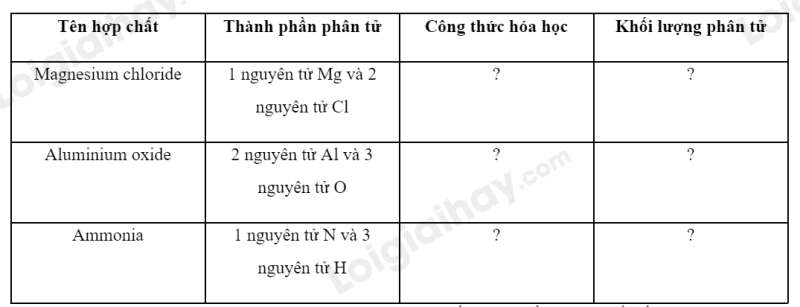
Phương pháp giải:
- Công thức hóa học của hợp chất gồm kí hiệu hóa học của những nguyên tố tạo ra hợp chất kèm theo chỉ số ở dưới chân bên phải kí hiệu hóa học. Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố
- Khối lượng phân tử = Tổng khối lượng các nguyên tử
Trả lời:
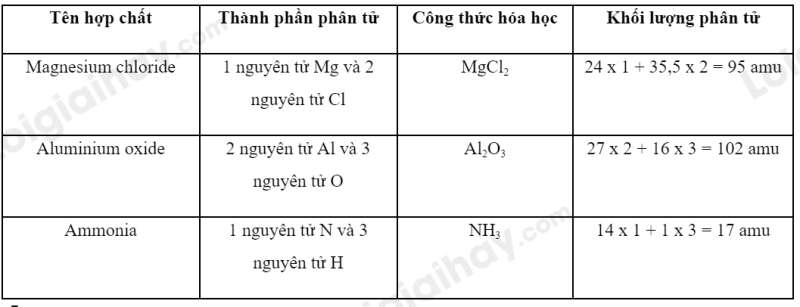
Phương pháp giải:
- Công thức hóa học của hợp chất gồm kí hiệu hóa học của những nguyên tố tạo ra hợp chất kèm theo chỉ số ở dưới chân bên phải kí hiệu hóa học. Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố
- Khối lượng phân tử = Tổng khối lượng các nguyên tử
Trả lời:
- Phân tử iron(III) oxide có công thức hóa học là: Fe2O3. Gồm có
+ 2 nguyên tử của nguyên tố Fe, 3 nguyên tử của nguyên tố O
+ Khối lượng phân tử = 56 x 2 + 16 x 3 = 160 amu
Phương pháp giải:
- Công thức hóa học của hợp chất gồm kí hiệu hóa học của những nguyên tố tạo ra hợp chất kèm theo chỉ số ở dưới chân bên phải kí hiệu hóa học. Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố
- Khối lượng phân tử = Tổng khối lượng các nguyên tử
Trả lời:
- Công thức hóa học của 1 chất cho biết:
+ Nguyên tố tạo nên chất đó
+ Số nguyên tử của nguyên tố tạo nên chất
+ Khối lượng phân tử của chất
4. Tính phần trăm nguyên tố trong hợp chất
Phương pháp giải:
Với hợp chất: AxBy ta có:
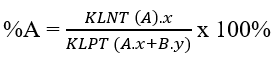
Tổng tất cả các phần trăm nguyên tố trong một phân tử luôn bằng 100%
Trả lời:
- Xét phân tử Al2O3:
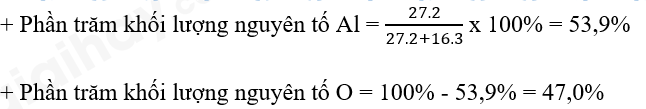
- Xét phân tử MgCl2:
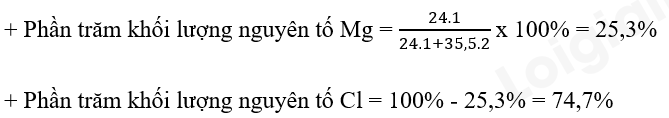
- Xét phân tử Na2S:

- Xét phân tử (NH4)2CO3:

Phương pháp giải:
- Hydrogen: Kí hiệu hóa học là H, có hóa trị I
- Nhóm phosphate: Kí hiệu hóa học là PO4, hóa trị III
- Áp dụng quy tắc hóa trị
- Các tính phần trăm khối lượng nguyên tố: Với hợp chất: AxBy ta có: 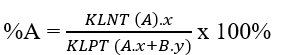
Trả lời:
- Hydrogen: Kí hiệu hóa học là H, có hóa trị I
- Nhóm phosphate: Kí hiệu hóa học là PO4, hóa trị III
- Gọi công thức hóa học phosphoric acid là Hx(PO4)y
- Theo quy tắc hóa trị: I.x = III.y
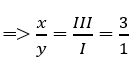
Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 3 và y =1
=> Công thức hóa học của hợp chất: H3PO4

=> Nguyên tố O có phần trăm khối lượng lớn nhất
5. Xác định công thức hóa học
Phương pháp giải:
Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát): AlxCy
Bước 2: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất
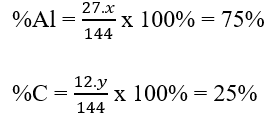
Bước 3: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hóa học cần tìm
Trả lời:

Phương pháp giải:
Bước 1: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất
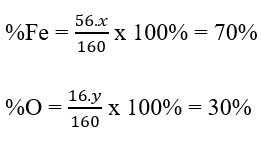
Bước 2: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hóa học cần tìm
Trả lời:

Tìm hiểu qua sách, báo và internet, em hãy cho biết một số ứng dụng của hợp chất (Z)
Phương pháp giải:
Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát): KxNyOz
Bước 2: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất
Bước 3: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hóa học cần tìm
Trả lời:
- Gọi công thức của hợp chất Z là: KxNyOz
- Khối lượng phân tử của hợp chất Z = 101 amu

=> Công thức hóa học của (Z) là: KNO3
- Ứng dụng của hợp chất KNO3:
+ Là một loại phân bón cung cấp các chất dinh dưỡng cho cây
+ Chế tạo thuốc nổ
+ Chất phụ gia để bảo quan thịt chống ôi thiu
+ Sử dụng trong kem đánh răng
Bài tập (trang 51)
Phương pháp giải:
Bước 1: Đặt công thức hóa học tổng quát là AxOy
Bước 2: Áp dụng quy tắc hóa trị => Tìm ra giá trị của x và y
Trả lời:
- Xét hợp chất của oxygen và potassium:
+ Gọi công thức phân tử: KxOy (K có hóa trị I, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => I.x = II.y
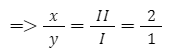
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =1
=> Công thức hóa học của hợp chất: K2O
- Xét hợp chất của oxygen và magnesium:
+ Gọi công thức phân tử: MgxOy (Mg có hóa trị II, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => II.x = II.y
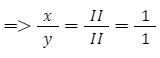
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =1
=> Công thức hóa học của hợp chất: MgO
- Xét hợp chất của oxygen và aluminium:
+ Gọi công thức phân tử: AlxOy (Al có hóa trị III, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => III.x = II.y
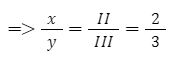
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =3
=> Công thức hóa học của hợp chất: Al2O3
- Xét hợp chất của oxygen và phosphorus:
+ Gọi công thức phân tử: PxOy (P có hóa trị V, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => V.x = II.y
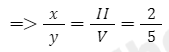
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =5
=> Công thức hóa học của hợp chất: P2O5
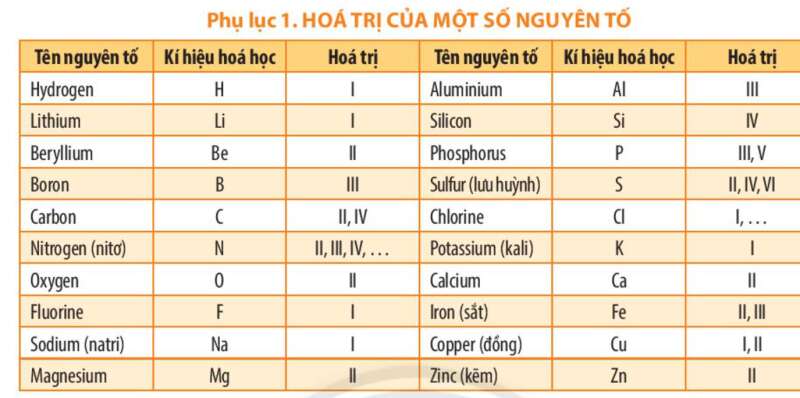
Bài 2 trang 51 KHTN lớp 7: Dựa vào bảng hóa trị ở Phụ lục trang 187, em hãy hoàn thành bảng sau:
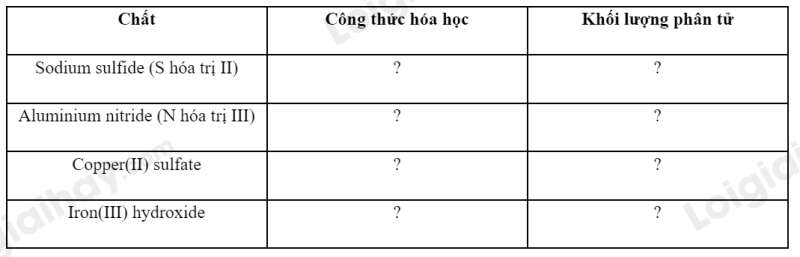
Phương pháp giải:
- Công thức hóa học: Áp dụng quy tắc hóa trị
- Khối lượng phân tử = tổng khối lượng các nguyên tử tạo nên phân tử đó
Trả lời:
- Xét phân tử sodium sulfide: NaxSy (Na hóa trị I, S hóa trị II)
+ Áp dụng quy tắc hóa trị => I.x = II.y
![]()
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =1
=> Công thức hóa học của hợp chất: Na2S
=> Khối lượng phân tử = 23 x 2 + 32.1 = 78 amu
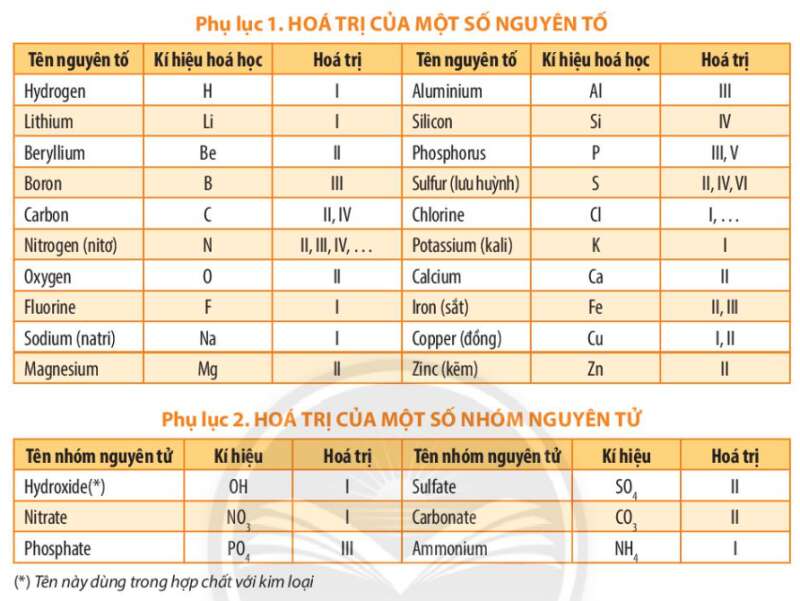
- Xét phân tử Aluminium nitride: AlxNy (Al hóa trị III, N hóa trị III)
+ Áp dụng quy tắc hóa trị => III.x = III.y
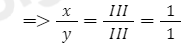
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =1
=> Công thức hóa học của hợp chất: AlN
=> Khối lượng phân tử = 27 x 1 + 14 x 1 = 41 amu
- Xét phân tử Copper (II) sulfate: CuxSy (Cu hóa trị II, S hóa trị II)
+ Áp dụng quy tắc hóa trị => II.x = II.y
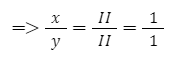
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =1
=> Công thức hóa học của hợp chất: CuS
=> Khối lượng phân tử = 64 x 1 + 32 x 1 = 96 amu
- Xét phân tử Iron(III) hydroxide: Fex(OH)y (Fe hóa trị III, OH hóa trị I)
+ Áp dụng quy tắc hóa trị => III.x = I.y
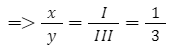
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =3
=> Công thức hóa học của hợp chất: Fe(OH)3
=> Khối lượng phân tử = 56x1 + (16x1 + 1x1) x 1 = 107 amu
- Hoàn thành bảng:
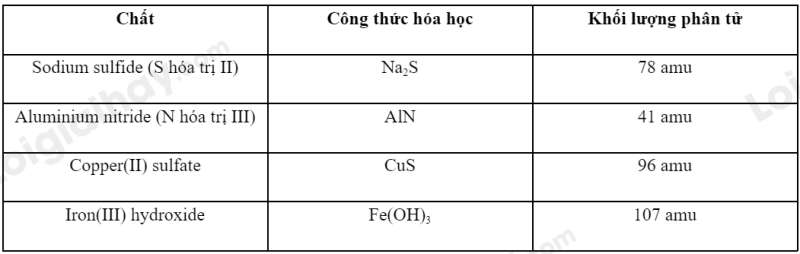

Phương pháp giải:
Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát): CaxCyOz
Bước 2: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất
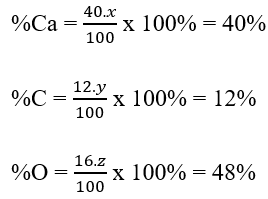
Bước 3: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hóa học cần tìm
Trả lời:

Lý thuyết KHTN 7 Bài 7: Hóa trị và công thức hóa học
I. Hóa trị
1. Định nghĩa
- Hóa trị của một nguyên tố trong hợp chất là con số biểu thị khả năng liên kết của nguyên tử nguyên tố đó với nguyên tử khác trong phân tử.
- Hóa trị được biểu thị bằng các chữ số La Mã (I; II …)
2. Cách xác định
- Để xác định hóa trị của nguyên tố trong hợp chất cộng hóa trị, người ta dựa vào hóa trị của nguyên tố đã biết làm đơn vị, chẳng hạn hóa trị của H là I; hóa trị của O là II.
Ví dụ 1: Trong phân tử phosphine (PH3) một nguyên tử P có khả năng liên kết với 3 nguyên tử H, mỗi nguyên tử H có hóa trị I ⇒ P có hóa trị III
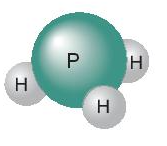
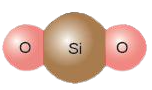
Ví dụ 2: Trong phân tử silicon dioxide (SiO2), 1 nguyên tử Si có khả năng liên kết với 2 nguyên tử O, mỗi nguyên tử O hóa trị II ⇒ Si có hóa trị IV.
II. Quy tắc hóa trị
- Quy tắc hóa trị: Trong phân tử hợp chất hai nguyên tố, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia.
- Ví dụ: Trong phân tử aluminium chlorine (AlCl3), hóa trị và số nguyên tử tham gia liên kết của Al và Cl như sau:
|
Nguyên tố |
Al |
Cl |
|
Hóa trị |
III |
I |
|
Số nguyên tử |
1 |
3 |
|
Tích hóa trị và số nguyên tử |
III × 1 = I × 3 |
|
III. Công thức hóa học
Phân tử của chất được tạo thành từ nguyên tử của một hay nhiều nguyên tố và được biểu diễn bằng công thức hóa học.
1. Viết công thức hóa học của đơn chất
- Công thức hóa học của đơn chất được kí hiệu bằng kí hiệu nguyên tố hóa học kèm với chỉ số (chỉ số nguyên tử của mỗi nguyên tố trong một phân tử) ghi ở bên dưới.
- Một số đơn chất phi kim thể khí (ở điều kiện thường) có công thức hóa học chung là Ax.
Ví dụ: Phân tử khí oxygen được tạo thành từ hai nguyên tử oxygen liên kết với nhau, công thức phân tử của khí oxygen là O2.
- Đối với đơn chất kim loại, hạt hợp thành là nguyên tử nên kí hiệu hóa học của nguyên tố kim loại được coi là công thức hóa học của đơn chất kim loại.
Ví dụ: Kim loại iron có công thức hóa học là Fe.
- Một số đơn chất phi kim ở thể rắn, quy ước công thức hóa học là kí hiệu nguyên tố.
Ví dụ: Công thức hóa học của đơn chất phosphorus là P.
Chú ý:
- Nếu chỉ số trong công thức hóa học bằng 1 thì quy ước không ghi.
- Trong hợp chất gồm oxygen và nguyên tố khác, nguyên tố oxygen thường ghi ở cuối công thức hóa học.
2. Viết công thức hóa học của hợp chất
- Công thức hóa học của hợp chất gồm kí hiệu hóa học của những nguyên tố tạo thành kèm chỉ số ở bên dưới mỗi kí hiệu.
- Công thức chung của phân tử có dạng: AxBy
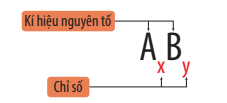
Ví dụ: Phân tử carbon dioxide gồm 1 nguyên tử carbon và 2 nguyên tử oxygen, công thức hóa học của phân tử carbon dioxide là CO2.
- Công thức hóa học cho biết thành phần nguyên tố và số lượng nguyên tử của mỗi nguyên tố có trong phân tử đó. Từ đó, có thể tính được khối lượng phân tử.
Chú ý: Cách viết công thức hóa học hợp chất
- Hợp chất tạo bởi oxygen và nguyên tố khác, công thức hóa học có dạng AxOy.
- Nếu A là kim loại và B là phi kim, công thức hóa học có dạng AxBy.
- Hợp chất tạo bởi hydrogen và nguyên tố A:
+ Nếu A thuộc các nhóm IA đến VA, công thức hóa học có dạng AHx.
+ Nếu A thuộc các nhóm VIA đến VIIA, công thức hóa học có dạng HxA.
IV. Tính phần trăm nguyên tố trong hợp chất
- Phần trăm (%) nguyên tố trong hợp chất được tính bằng tỉ số giữa khối lượng của nguyên tố đó trong một phân tử hợp chất và khối lượng phân tử (KLPT) của hợp chất.
- Khối lượng của nguyên tố trong một phân tử hợp chất được tính bằng tích của khối lượng nguyên tử (KLNT) và số nguyên tử của nguyên tố đó.
- Tổng quát:
+ Với hợp chất AxBy, ta có:
+ Tổng tất cả các phần trăm nguyên tố trong một phân tử luôn bằng 100%.
- Ví dụ: Đối với hợp chất MgCl2
%Mg = = = 25,26%
%O = 100% - 25,26% = 74,74%
V. Xác định công thức hóa học
1. Xác định công thức hóa học khi biết phần trăm nguyên tố và khối lượng phân tử
- Các bước xác định:
Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát);
Bước 2: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất;
Bước 3: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hóa học cần tìm.
- Ví dụ: Thạch nhũ trong hang động có thành phần chính là hợp chất (T). Phân tử (T) có cấu tạo từ nguyên tố calcium, carbon và oxygen với các tỉ lệ phần trăm tương ứng là 40%, 12% và 48%. Khối lượng phân tử (T) là 100 amu. Hãy xác định công thức hóa học của (T).
Hướng dẫn giải:
Đặt công thức hóa học của hợp chất (T) là: CaxCyOz
%Ca = = 40%
⇒ x = 1
%C = = 12%
⇒ y = 1
%O = = 48%
⇒ z = 3
Vậy công thức hóa học của hợp chất là CaCO3
2. Xác định công thức hóa học dựa vào quy tắc hóa trị
- Các bước xác định:
+ Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát)
+ Bước 2: Lập biểu thức tính dựa vào quy tắc hóa trị, chuyển thành tỉ lệ các chỉ số nguyên tử.
+ Bước 3: Xác định số nguyên tử (những số nguyên đơn giản nhất, có tỉ lệ tối giản) và viết công thức hóa học cần tìm.
- Ví dụ: Hợp chất tạo bởi oxygen và phosphorus có dạng:
Theo quy tắc hóa trị ta có: x × V = y × II
Chuyển thành tỉ lệ:
Chọn x = 2; y = 5
Vậy công thức hóa học của hợp chất là P2O5
Chú ý:
- Quy tắc hóa trị thường đúng với đa số hợp chất vô cơ. Tuy nhiên, quy tắc này không đúng với đa số hợp chất hữu cơ (C2H4; C6H6 …) và một số hợp chất vô cơ (H2O2; Na2O2 …)
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Chân trời sáng tạo hay, chi tiết khác:
Bài 6: Giới thiệu về liên kết hóa học
Bài 9: Đồ thị quãng đường - thời gian