Với Giải hóa học lớp 10 trang 64 Chân trời sáng tạo chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 64 Chân trời sáng tạo
Câu hỏi 13 trang 64 Hóa học 10: Mô tả sự hình thành liên kết п
Phương pháp giải:
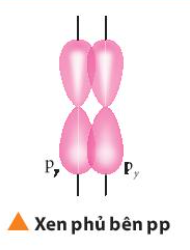
Liên kết п là sự xen phủ bên
Lời giải:
Liên kết п hay còn là sự xen phủ bên: Sự xen phủ thực hiện ở hai bên trục nối giữa hai hạt nhân nguyên tử
Ví dụ:
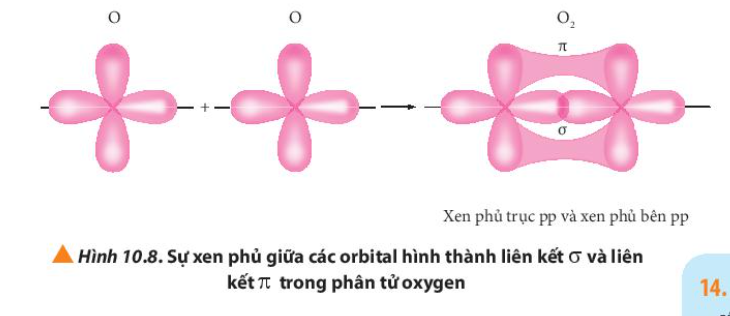
Câu hỏi 14 trang 64 Hóa học 10: Quan sát Hình 10.8, hãy so sánh sự hình thành liên kết σ và liên kết п
 Phương pháp giải:
Phương pháp giải:
So sánh độ xen phủ giữa liên kết п và liên kết σ
Lời giải:
|
|
Liên kết σ |
Liên kết п |
|
Giống nhau |
- Sự xen phủ các orbital của nguyên tử |
|
|
Khác nhau |
- Xen phủ trục - Độ xen phủ lớn hơn - Vùng xen phủ nằm trên đường nối tâm 2 nguyên tử |
- Xen phủ bên - Độ xen phủ nhỏ hơn - Vùng xen phủ nằm hai bên đường nối tâm hai nguyên tử |
Câu hỏi 15 trang 64 Hóa học 10: Theo em, thế nào là liên kết bội? Phân tử nào dưới đây có chứa liên kết bội: Cl2, HCl, O2 và N2?
Phương pháp giải:
- Liên kết bội được hình thành bởi liên kết có 2 – 3 cặp electron góp chung
Lời giải:
- Liên kết bội là liên kết được hình thành giữa hai nguyên tố bằng hai hoặc ba cặp electron góp chung. Liên kết này được biểu thị bằng hai gạch nối hoặc ba gạch nối.
- Xét các phân tử:
+ Cl2: Cl – Cl => Liên kết đơn
+ HCl: H – Cl => Liên kết đơn
+ O2 : O = O => Liên kết bội
+ N2: N N => Liên kết bội
Câu hỏi 16 trang 64 Hóa học 10: Sự xen phủ có sự tham gia của orbital nào luôn là xen phủ trục?
Phương pháp giải:
Xen phủ trục là vùng xen phủ nằm trên đường nối tâm hai nguyên tử
Lời giải:
Sự xen phủ có sự tham gia của orbital s luôn là xen phủ trục vì dù theo phương, chiều nào thì vùng xen phủ cũng nằm trên đường nối tâm
Câu hỏi 17 trang 64 Hóa học 10: Số liên kết σ và liên kết п trong mỗi liên kết đơn, liên kết đôi và liên kết ba lần lượt bằng bao nhiêu?
Lời giải:
- Liên kết đơn: 1 liên kết σ
- Liên kết đôi: 1 liên kết σ, 1 liên kết п
- Liên kết ba: 1 liên kết σ, 2 liên kết п
Luyện tập trang 64 Hóa học 10: Vẽ sơ đồ xen phủ orbital giữa 2 nguyên tử carbon hình thành liên kết đôi trong phân tử ethylene (C2H4).
Phương pháp giải:
- Phân tử C2H4 gồm 1 liên kết đôi giữa 2 nguyên tử C => 1 liên kết σ, 1 liên kết п
- Liên kết giữa C và H là liên kết đơn => Liên kết σ
Lời giải: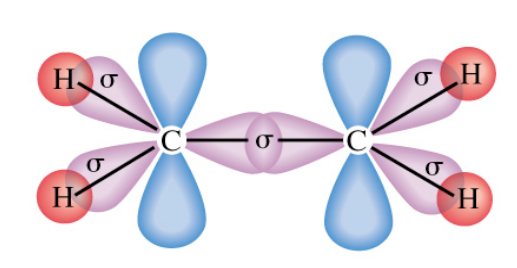
Câu hỏi 18 trang 64 Hóa học 10: Căn cứ giá trị năng lượng liên kết H-H và N N đã cho, liên kết trong phân tử nào dễ bị phá vỡ hơn?
Phương pháp giải:
Lời giải:
- Để phá vỡ 1 mol phân tử H2 cần cung cấp năng lượng là 432 kJ/mol
- Để phá vỡ 1 mol phân tử N2 cần cung cấp năng lượng là 945 kJ/mol
=> Liên kết trong phân tử H2 dễ bị phá vỡ hơn
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác: