Với Giải hóa học lớp 10 trang 25 Chân trời sáng tạo chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 25 Chân trời sáng tạo
Bài 1 trang 25 Hóa học 10: Một nguyên tử X gồm 16 proton, 16 electron và 16 neutron. Nguyên tử X có kí hiệu là
A.
B.
C.
D.
Phương pháp giải:
- Số P = Số Z
- Số khối A = N + P
Lời giải:
- Nguyên tử X có 16 proton => Nguyên tử S
- Số proton = số hiệu nguyên tử = 16 => Z = 16
- Số khối = số proton + số neutron = 16 + 16 = 32
=> Kí hiệu nguyên tử X:
Đáp án C
Bài 2 trang 25 Hóa học 10: Silicon là nguyên tố được sử dụng để chế tạo vật liệu bán dẫn, có vai trò quan trọng trong sản xuất công nghiệp. Trong tự nhiên, nguyên tố này có 3 đồng vị với số khối lần lượt là 28, 29, 30. Viết kí hiệu nguyên tử cho mỗi đồng vị của silicon. Biết nguyên tố silicon có số hiệu nguyên tử là 14.
Phương pháp giải:
Lời giải:
- Số khối = 28:
- Số khối = 29:
- Số khối = 30:
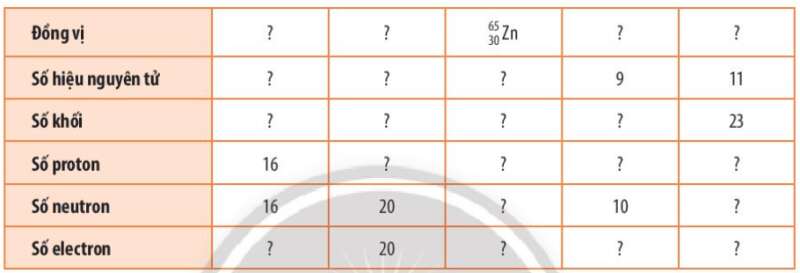
Bài 3 trang 25 Hóa học 10: Hoàn thành những thông tin chưa biết trong bảng sau:
Phương pháp giải:

- Số hiệu nguyên tử = số proton = số electron
- Số khối: A = số proton (P) + số neutron (N)
Lời giải:
|
Đồng vị |
|
|
|
|
|
|
Số hiệu nguyên tử |
16 |
20 |
30 |
9 |
11 |
|
Số khối |
32 |
40 |
65 |
19 |
23 |
|
Số proton |
16 |
20 |
30 |
9 |
11 |
|
Số neutron |
16 |
20 |
35 |
10 |
12 |
|
Số electron |
16 |
20 |
30 |
9 |
11 |
Bài 4 trang 25 Hóa học 10: Trong tự nhiên, magnesium có 3 đồng vị bền là 24Mg, 25Mg và 26Mg. Phương pháp phổ khối lượng xác nhận đồng vị 26Mg chiếm tỉ lệ phần trăm số nguyên tử là 11%. Biết rằng nguyên tử khối trung bình của Mg là 24,32. Tính % số nguyên tử của đồng vị 24Mg, đồng vị 25Mg?
Phương pháp giải:
Bước 1: Gọi phần trăm đồng vị 24Mg là x%
=> Phần trăm đồng vị 25Mg là: 100 – 11 – x
Bước 2: Áp dụng công thức:
Nguyên tử khối trung bình:
Trong đó: A, B, C, D… là số khối của các đồng vị
a, b, c, d… là phần trăm của các đồng vị tương ứng
Lời giải:
Gọi phần trăm đồng vị 24Mg là x%
=> Phần trăm đồng vị 25Mg là: 100 – 11 – x = (89 – x) %
Nguyên tử khối trung bình của Mg = 24,32
Áp dụng công thức:
=>
=> x = 79%
=> Phần trăm đồng vị 24Mg là 79%
=> Phần trăm đồng vị 25Mg là: 10%
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác: