Tailieumoi.vn giới thiệu Giải sách bài tập Hóa học lớp 11 Bài 27: Luyện tập Ankan và xicloankan chi tiết giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 27: Luyện tập Ankan và xicloankan
Bài 27.1 trang 42 SBT Hóa học 11: Nhận xét nào sau đây đúng ?
A. Tất cả ankan và tất cả xicloankan đều không tham gia phản ứng cộng.
B. Tất cả ankan và tất cả xicloankan đều có thể tham gia phản ứng cộng.
C. Tất cả ankan không tham gia phản ứng cộng nhưng một số xicloankan lại có thể tham gia phản ứng cộng.
D. Một số ankan có thể tham gia phản ứng cộng và tất cả xicloankan không thể tham gia phản ứng cộng.
Lời giải:
Tất cả ankan không tham gia phản ứng cộng nhưng một số xicloankan lại có thể tham gia phản ứng cộng.
=> Chọn C.
Bài 27.2 trang 42 SBT Hóa học 11: Các ankan không tham gia loại phản ứng nào cho dưới đây ?
A. Phản ứng thế
B. Phản ứng cộng
C. Phản ứng tách
D. Phản ứng cháy
Lời giải:
Trong phân tử ankan chỉ chứa liên kết đơn, do đó ankan không tham gia phản ứng cộng.
=> Chọn B
Bài 27.3 trang 42 SBT Hóa học 11: Tên gọi phù hợp với hợp chất
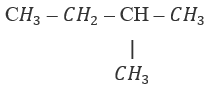 là:
là:
A. Pentan B. 3-metylbutan
C. 2-metylpentan D. 2-metylbutan
Lời giải:
Mạch cacbon được đánh số như sau:
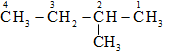
=> Chọn D.
Bài 27.4 trang 42 SBT Hóa học 11: Nhận xét nào sau đây sai?
A. Khi đốt cháy hoàn toàn một ankan trong oxi, số mol H2O tạo ra lớn hơn số mol CO2.
B. Khi đốt cháy hoàn toàn một hiđrocacbon trong oxi, nếu số mol H2O tạo thành lớn hơn số mol CO2 thì hiđrocacbon đó là ankan.
C. Các ankan có thể tham gia phản ứng thế.
D. Nếu một hiđrocacbon có thể tham gia phản ứng thế thì hiđrocacbon là ankan.
Lời giải:
Trong phân tử ankan chỉ chứa liên kết đơn, do đó ankan có phản ứng đặc trưng là phản ứng thế.
=> Chọn D.
Bài 27.5 trang 42 SBT Hóa học 11: Cho clo tác dụng với butan, thu được hai dẫn xuất monoclo .
1. Dùng công thức cấu tạo viết phương trình hoá học, ghi tên các sản phẩm.
2. Tính phần trăm của mỗi sản phẩm đó, biết rằng nguyên tử hiđro liên kết với cacbon bậc hai có khả năng bị thế cao hơn 3 lần so với nguyên tử hiđro liên kết với cacbon bậc một.
Phương pháp giải:
1. Do butan có cấu trúc đối xứng nên sẽ có 2 vị trí thế của clo.
2. Dựa vào dữ kiện "nguyên tử hiđro liên kết với cacbon bậc hai có khả năng bị thế cao hơn 3 lần so với nguyên tử hiđro liên kết với cacbon bậc một" tính % mỗi sản phẩm.
Lời giải:
1.
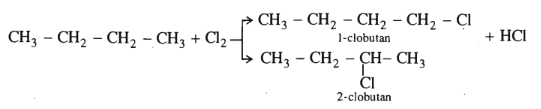
2.Ở butan có 6 nguyên tử H liên kết với C bậc một và 4 nguyên tử H liên kết với C bậc hai. Nếu khả năng thế của C bậc một là 1 thì của C bậc hai là 3, vì thế :
1-clobutan chiếm: . 100% = 33,33%
2-clobutan chiếm: 100% - 33,33% = 66,67%
Bài 27.6 trang 42 SBT Hóa học 11: Hỗn hợp M ở thể lỏng, chứa hai ankan. Để đốt cháy hoàn toàn hỗn hợp M cần dùng vừa hết 63,28 lít không khí (đktc). Hấp thụ hết sản phẩm cháy vào dung dịch Ca(OH)2 lấy dư, thu được 36,00 g chất kết tủa.
1. Tính khối lượng hỗn hợp M biết rằng oxi chiếm 20,00% thể tích không khí.
2. Xác định công thức phân tử và phần trăm khối lượng của từng chất trong hỗn hợp M nếu biết thêm rằng hai ankan khác nhau 2 nguyên tử cacbon.
Phương pháp giải:
Cách 1:
1. +) Tính số mol và
+) Gọi CT trung bình của 2 ankan là:
+) Viết PTHH:
+) Dựa vào PTHH lập hệ phương trình 2 ẩn, giải phương trình khối lượng của hỗn hợp M.
2. +) Dựa vào giá trị tìm được ở trên biện luận các trường hợp để tìm CTPT của 2 ankan.
+) Gọi số mol mỗi ankan là x, y (mol)
+) Lập hệ phương trình 2 ẩn phần trăm khối lượng của từng chất.
Cách 2:
1. Ta có: Khối lượng M = khối lượng C + khối lượng H.
2. +) Tìm khối lượng trung bình của 1 mol ankan.
+) Do hai ankan khác nhau 2 nguyên tử cacbon nên ta có phương trình: 14n + 2 < < 14n + 30
+) Biện luận để tìm n phần trăm khối lượng của từng chất.
Lời giải:
Số mol : = 0,565 (mol)
Số mol = số mol = = 0,36 (mol).
Cách 1:
1.
a mol a mol a mol
Khối lượng hỗn hợp M= (14 + 2)a = (14 . 7,2 + 2) . 5.10-2 =5,14(g).
2. Vì = 7,2 và hai ankan khác nhau hai nguyên tử cacbon nên có hai cặp chất phù hợp :
- (x mol) và (y mol).
(x mol) và (y mol).
Nếu n = 6:
% về khối lượng của trong hỗn hợp M :
% về khối lượng của trong hỗn hợp M : 100% - 33,46% = 66,54%
Nếu n = 7:
Thành phần phần trăm về khối lượng của trong hỗn hợp :
Thành phần phần trăm về khối lượng của trong hỗn hợp : 100% - 87,55% = 12,45%
Cách 2:
1. Trong 0,36 mol CO2, khối lượng cacbon : 0,36 . 12 = 4,32 (g) và khối lượng oxi: 0,36 . 32 = 11,52 (g).
Khối lượng oxi trong nước là : 0,565 . 32, - 11,52 = 6,56 (g).
Khối lương hiđro (trong nước) :
Khối lượng M = khối lượng C + khối lượng H = 4,32 + 0,82 = 5,14 (g)
2. Khi đốt 1 mol ankan, số mol H2O tạo ra nhiều hơn số mol CO2 là 1 mol. Khi đốt hỗn hợp M, số mol H2O nhiều hơn số mol CO2:
Vậy, hỗn hợp M có mol ankan.
Khối lượng trung bình của 1 mol ankan :
14n + 2 < 102,8 < 14n + 30 5,20 < n < 7,20
Đến đây có thể tìm được công thức phân tử và phần trăm khối lượng từng chất như ở cách thứ nhất.
Bài 27.7* trang 42 SBT Hóa học 11: Một bình kín dung tích 11,2 lít có chứa 6,4 g O2 và 1,36 g hỗn hợp khí A gồm 2 ankan. Nhiệt độ trong bình là 0°C và áp suất là atm. Bật tia lửa điện trong bình kín đó thì hỗn hợp A cháy hoàn toàn. Sau phản ứng, nhiệt độ trong bình là 136,5°C và áp suất là atm.
Nếu dẫn các chất trong binh sau phản ứng vào dung dịch Ca(OH)2 lấy dư thì có 9 gam kết tủa tạo thành.
1. Tính và , biết rằng thể tích bình không đổi.
2. Xác định công thức phân tử và phần trăm thể tích từng chất trong hỗn hợp A, biết rằng số mol của ankan có phân tử khối nhỏ nhiều gấp 1,5 lần số mol của ankan có phân tử khối lớn.
Phương pháp giải:
1. +) Giả sử hỗn hợp A có x mol CnH2n+2 và y mol CmH2m+2
+) Viết PTHH khi đốt cháy A.
+) Từ các dữ kiện đề bài lập các phương trình toán học để tính và
2. Biện luận n, m => CTPT của 2 ankan => phần trăm thể tích từng chất.
Lời giải:
1. Giả sử hỗn hợp A có x mol CnH2n+2 và y mol CmH2m+2 :
(14n + 2)x + (14m + 2)y = 1,36 14(nx + my) + 2(x + y) = 1,36 (1)
Khi đốt hỗn hợp A :
x mol x mol nx mol (n + 1)x mol
y mol y mol ny mol (n + 1)y mol
nx + my = 0,09 (2)
Từ (1) và (2), tìm được x + y = 0,05.
Số mol trước phản ứng : = 0,2(mol).
Tổng số mol khi trước phản ứng : 0,2 + 0,05 = 0,25 (mol).
Nếu ở đktc thì V0 = 0,25.22,4 = 5,6 (lít).
Thực tế = 11,2 (lít)
= = = = 0,5(atm).
Số mol hơi nước : (n + 1)x + (m + 1)y = nx + my + x + y = 0,14
Số mol O2 dự phản ứng: = 0,16 (mol)
SỐ mol O2 còn dư : 0,2 - 0,16 = 0,04 (mol).
Tổng số mol khí sau phản ứng : 0,09 + 0,14 + 0,04 = 0,27 (mol).
Nếu ở đktc thì = 0,27.22,4 = 6,048 (lít)
Thực tế V2 = 11,20 (lít)
2) Nếu n < m thì x = 1,5y ;
Vậy x = 0,03 ; y = 0,02
0,03n + 0,02m = 0,09 3n + 2m = 9
3n = 9 - 2m n = 3 -
n và m nguyên dương nên m = 3 và n = 1.
chiếm 60% thể tích hỗn hợp.
chiếm 40% thể tích hỗn hợp.
Bài 27.8 trang 43 SBT Hóa học 11: Chất A có công thức phân tử C6H14. Khi A tác dụng với clo, có thể tạo ra tối đa 3 dẫn xuất monoclo (C6H13Cl) và 7 dẫn xuất điclo ().
Hãy viết công thức cấu tạo của A và của các dẫn xuất monoclo, điclo của A.
Phương pháp giải:
+) Viết các đồng phân của C6H14. sau đó xác định các trường hợp thế của clo.
+) Viết CTCT của các dẫn xuất monoclo, điclo của A.
Lời giải:
Hướng dẫn : Ứng với công thức phân tử C6H14 có 5 đồng phân :
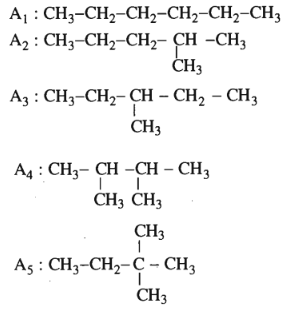
Số dẫn xuất monoclo C6H13Cl có thể tạo ra từ A1 là 3, từ A2 là 5, từ A3 là 4. từ A4 là 2, từ A5 là 3. Như vậy, chất A chỉ có thể có cấu tạo như A1 hoặc A5.
Số dẫn xuất điclo C6H12Cl2 có thể tạo ra từ A1 là 12 và từ A5 là 7.
Như vậy, chất A có công thức cấu tạo A5.