Tailieumoi.vn giới thiệu Giải sách bài tập Hóa học lớp 9 Bài 29: Axit cacbonic và muối cacbonat chi tiết giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 9. Mời các bạn đón xem:
Giải SBT Hóa học 9 Bài 29: Axit cacbonic và muối cacbonat
Bài 29.1 trang 37 SBT Hóa học 9: Trộn dung dịch X với dung dịch Y, thấy xuất hiện kết tủa. Dung dịch X, Y là :
A. NaOH và K2SO4;
B. K2CO3 và Ba(NO3)2;
C. KCl và Ba(NO3)2 ;
D. Na2CO3 và KNO3.
Phương pháp giải:
Viết phương trình hóa học để xác định sản phẩm tạo thành.
Lời giải:
Đáp án B.
K2CO3 và Ba(NO3)2 -----> 2KNO3 + BaCO3
Bài 29.2 trang 37 SBT Hóa học 9: Dẫn khí cacbonic vào dung dịch natri hiđroxit. Sản phẩm có thể là chất nào ? Giải thích
Lời giải:
Dẫn CO2 vào dung dịch NaOH có 3 trường hợp xảy ra :
a) CO2 + NaOH ------> NaHCO3
b) CO2 + 2NaOH —----> Na2CO3 + H20
c) Cả hai phản ứng trên. Sản phẩm phản ứng là hỗn hợp NaHCO3 và Na2CO3
Bài 29.3 trang 37 SBT Hóa học 9: Có những chất sau : NaHCO3, Ca(OH)2, CaCl2, CaCO3.
a) Chất nào tác dụng được với dung dịch HCl ?
b) Chất nào tác dụng được với dung dịch Na2CO3 ?
c) Chất nào tác dụng được với dung dịch NaOH ?
Viết các phương trình hoá học
Lời giải:
a) Các chất NaHCO3, Ca(OH)2, CaCO3 tác dụng với dung dịch HCl.
b) Các chất CaCl2, Ca(OH)2 tác dụng với dung dịch Na2CO3.
c) Chất NaHC03 tác dụng với dung dịch NaOH.
Bài 29.4 trang 37 SBT Hóa học 9: Có hỗn hợp bột CaCO3 và CaSO4. Nêu cách để xác định thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp. Viết các phương trình hoá học, nếu có.
Phương pháp giải:
Dựa vào tính chất hóa học khác nhau giữa muối sunfat và muối cacbonat.
Lời giải:
Cân lấy một lượng hỗn hợp, thí dụ 10 gam đem ngâm trong dung dịch HCl dư, khuấy nhẹ. Nếu không còn khí thoát ra, nghĩa là lượng CaCO3 đã tham gia hết, còn lại chất rắn là CaSO4. Lọc lấy chất rắn, rửa sạch. Nung chất rắn trong chén sứ, để nguội và cân. Đó là khối lượng CaSO4 khan. Từ đó ta tính được tỉ lệ phần trăm các chất trong hỗn hợp ban đầu.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Bài 29.5 trang 37 SBT Hóa học 9: Viết các phương trình hoá học thực hiện những chuyển đổi hoá học sau :
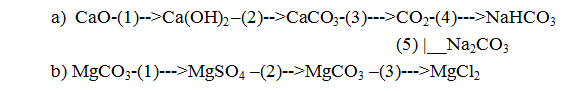
Phương pháp giải:
Xem tính chất hóa học của các hợp chất vô cơ đã học.
Lời giải:
Các phương tình hóa học :
a)
b)
Bài 29.6 trang 37 SBT Hóa học 9: Hãy viết phương trình hoá học của các phản ứng sau :
(1) 2C + ... ----------- > 2CO
(2) Fe2O3 + ... ---------> 2Fe + CO2
(3) CO2 + ... --------- > CaCO3 + H2O
Phương pháp giải:
Xem lại tính chất hóa học của C và hợp chất của C.
Lời giải:
Bài 29.7 trang 37 SBT Hóa học 9: Cho 19 gam hỗn hợp Na2CO3 và NaHCO3 tác dụng với 100 gam dung dịch HCl, sinh ra 4,48 lít khí (đktc).
Khối lượng mỗi muối trong hỗn hợp lần lượt là :
A. 10,6 gam và 8,4 gam ;
B. 16 gam và 3 gam ;
C. 10,5 gam và 8,5 gam ;
D. Kết quả khác.
Phương pháp giải:
Viết các phương trình hóa học, lập hệ phương trình 2 ẩn là số mol của 2 muối.
Lời giải:
Đáp án A.
Phương trình hóa học :
x mol y mol
y mol y mol
Bài 29.8 trang 38 SBT Hóa học 9: Nung 150 kg CaCO3 thu được 67,2 kg CaO. Hiệu suất của phản ứng là
A. 60% ; B. 40% ;
C. 80% ; D. 50%.
Phương pháp giải:
Viết và tính toán theo phương trình hóa học.
Lời giải:
Đáp án C.
Cứ 100g CaCO3 thì tạo ra 56g CaO
Khi dùng 150kg CaCO3 tạo ra:
Bài 29.9 trang 38 SBT Hóa học 9: Nung nóng m gam hỗn hợp CaCO3 và MgCO3 đến phản ứng hoàn toàn, sau phản ứng thu được 2,72 gam hỗn hợp 2 oxit và 1344 ml khí CO2 (ở đktc). Hãy tính giá trị của m.
Phương pháp giải:
Viết phương trình hóa học và lập hệ phương trình 2 ẩn là số mol của hai muối.
Lời giải:
Phương trình hóa học của phản ứng:
x mol x mol x mol
y mol y mol y mol
Theo phương trình hóa học trên và dữ liệu đề bài, ta có
Giải ra, ta có: x = 0,02(mol); y = 0,04(mol)
Bài 29.10 trang 38 SBT Hóa học 9: Cho 1,06 gam muối cacbonat kim loại hoá trị I tác dụng hết với dung dịch HCl thấy thoát ra 224 ml khí cacbonic (ở đktc). Xác định công thức phân tử muối cacbonat.
Phương pháp giải:
Đặt công thức muối cacbonat là M2CO3. Viết PTHH và tìm M
Lời giải:
Gọi M là kí hiệu nguyên tử khối của kim loại hoá trị I. Công thức muối là M2C03. Phương trình hoá học của phản ứng :
(2M+60)gam 22400 ml
1,06 gam 224 ml
Theo phương trình hóa học trên ta có:
. Đó là muối .