Với giải sách bài tập Hóa học 10 Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học sách Cánh diều hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 10. Mời các bạn đón xem:
Giải SBT Hóa học lớp 10 Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bài 6.1 trang 17 sách bài tập Hóa học 10: Chọn phương án đúng để hoàn thành các câu sau:
a) Mỗi nguyên tố hoá học được xếp vào một ...(1)... trong bảng tuần hoàn. Mỗi hàng trong bảng tuần hoàn được gọi là một ...(2)... Mỗi cột trong bảng tuần hoàn được gọi là một ...(3)...
A. (1) nhóm, (2) chu kì, (3) ô.
B. (1) ô, (2) chu kì, (3) nhóm.
C. (1) ô, (2) họ, (3) nhóm.
D. (1) ô, (2) chu kì, (3) nhóm chính.
b) Trong bảng tuần hoàn các nguyên tố hoá học do Mendeleev đề xuất, các nguyên tố được sắp xếp theo chiều tăng dần của ...(1).... Trong bảng tuần hoàn các nguyên tố hoá học hiện đại, các nguyên tố được sắp xếp theo chiều tăng dần của ...(2)....
A. (1) số electron hoá trị, (2) khối lượng nguyên tử.
B. (1) số hiệu nguyên tử, (2) khối lượng nguyên tử.
C. (1) khối lượng nguyên tử, (2) số hiệu nguyên tử.
D. (1) số electron hóa trị, (2) số hiệu nguyên tử.
Lời giải:
a) Đáp án đúng là: B
Mỗi nguyên tố hoá học được xếp vào một (1) ô trong bảng tuần hoàn. Mỗi hàng trong bảng tuần hoàn được gọi là một (2) chu kì. Mỗi cột trong bảng tuần hoàn được gọi là một (3) nhóm.
b) Đáp án đúng là: C
Trong bảng tuần hoàn các nguyên tố hoá học do Mendeleev đề xuất, các nguyên tố được sắp xếp theo chiều tăng dần của (1) khối lượng nguyên tử. Trong bảng tuần hoàn các nguyên tố hoá học hiện đại, các nguyên tố được sắp xếp theo chiều tăng dần của (2) số hiệu nguyên tử.
Bài 6.2 trang 17 sách bài tập Hóa học 10: Số hiệu nguyên tử của nguyên tố hoá học bằng
A. số thứ tự của ô nguyên tố.
B. số thứ tự của chu kì.
C. số thứ tự của nhóm.
D. số electron lớp ngoài cùng của nguyên tử.
Lời giải:
Đáp án đúng là: A
Số hiệu nguyên tử của nguyên tố hoá học bằng số thứ tự của ô nguyên tố.
(1) Số thứ tự của nhóm luôn luôn bằng số electron ở lớp vỏ ngoài cùng của nguyên tử nguyên tố thuộc nhóm đó.
(2) Số electron ở lớp vỏ ngoài cùng càng lớn thì số thứ tự của nhóm càng lớn.
(3) Nguyên tử các nguyên tố trong cùng một hàng có cùng số lớp electron.
(4) Nguyên tử các nguyên tố trong cùng một cột có cùng số electron hoá trị.
Lời giải:
Phát biểu (1) sai vì chỉ các nguyên tố nhóm A thì số thứ tự của nhóm luôn luôn bằng số electron ở lớp vỏ ngoài cùng của nguyên tử nguyên tố thuộc nhóm đó.
Phát biểu (2) sai. Ví dụ Fe thuộc nhóm VIIIB nhưng chỉ có 2 electron ở lớp ngoài cùng.
Phát biểu (3) và (4) đúng.
Những thông tin thu được từ ô nguyên tố này là:
A. Vàng có kí hiệu là Au, nguyên tử có 79 proton, nguyên tử khối trung bình là 196,97.
B. Vàng và các hợp chất của vàng có kí hiệu là Au, có số hiệu nguyên tử là 79, nguyên tử khối trung bình là 196,97.
C. Vàng và các hợp chất của vàng có kí hiệu là Au, có số hiệu nguyên tử là 79, vàng có hai đồng vị với số khối là 196 và 197.
D. Vàng có kí hiệu là Au, số hiệu nguyên tử là 79, có hai đồng vị với số khối là 196 và 197.
Lời giải:
Đáp án đúng là: A
Dựa vào các thông tin ở ô nguyên tố xác định được: Vàng có kí hiệu là Au, nguyên tử có 79 proton, nguyên tử khối trung bình là 196,97.
A. ô số 6, chu kì 2, nhóm VIA.
B. ô số 6, chu kì 3, nhóm VIB.
C. ô số 8, chu kì 2, nhóm VIA.
D. ô số 8, chu kì 2, nhóm VIB.
Lời giải:
Đáp án đúng là: C
Oxygen có 8 electron nên Z = 8, oxygen ở ô số 8 trong bảng tuần hoàn.
Oxygen ở chu kì 2 (do có 2 lớp electron); nhóm VIA (do 6 electron hóa trị, nguyên tố p).
A. ô số 26, chu kì 3, nhóm VIIIB.
B. ô số 26, chu kì 3, nhóm VIIIA.
C. ô số 26, chu kì 4, nhóm VIIIA.
D. ô số 26, chu kì 4, nhóm VIIIB.
Lời giải:
Đáp án đúng là: D
Từ cấu hình electron của Fe xác định sắt có 26 electron, số hiệu nguyên tử là 26. Vậy sắt ở:
+ Ô thứ 26 (do Z = 26)
+ Chu kì 4 (do có 4 lớp electron)
+ Nhóm VIIIB (do nguyên tố d, cấu hình electron lớp ngoài cùng và phân lớp sát lớp ngoài cùng: 3d64s2).
A. F và Cl nằm ở cùng một nhóm.
B. F và Cl có số electron lớp ngoài cùng bằng nhau.
C. F và Cl có số electron lớp ngoài cùng khác nhau.
D. F và Cl nằm ở cùng một chu kì.
E. Số thứ tự chu kì của Cl lớn hơn F.
G. Cl là nguyên tố nhóm B, F là nguyên tố nhóm A.
Lời giải:
Đáp án đúng là: A, B, E
F và Cl cùng có 7 electron ở lớp ngoài cùng, cùng thuộc nhóm VIIA, tuy nhiên Cl ở chu kì 3 còn F ở chu kì 2.
Lời giải:
- a ghép với 3, giải thích:
Dựa vào cấu hình electron 1s22s22p6 xác định nguyên tố thuộc nhóm VIIIA (do nguyên tố p, cấu hình electron lớp ngoài cùng có dạng ns2np6).
- b ghép với 4, giải thích:
Dựa vào cấu hình electron [Ar]3d54s1 xác định nguyên tố thuộc chu kì 4 (do có 4 lớp electron).
- c ghép với 1, giải thích:
Dựa vào cấu hình electron [He]2s22p1 xác định nguyên tố thuộc nhóm IIIA (do nguyên tố p, cấu hình electron lớp ngoài cùng có dạng ns2np1).
- d ghép với 2, giải thích:
Dựa vào cấu hình electron 1s22s22p63s1 xác định nguyên tử có 11 electron vậy Z = 11, nguyên tố thuộc ô 11 trong bảng tuần hoàn.
A. 2, 1, 2.
B. 1, 2, 2.
C. 1, 1, 3.
D. Không xác định được.
Lời giải:
Đáp án đúng là: B
- Nguyên tố s là nguyên tố nhóm A mà nguyên tử có cấu hình electron lớp ngoài cùng là ns1÷2. Nguyên tố thuộc khối s: Na: [Ne]3s1.
- Nguyên tố p là nguyên tố nhóm A mà nguyên tử có cấu hình electron lớp ngoài cùng là ns2np1÷6. Nguyên tố thuộc khối p: Br: [Ar]3d104s24p5 và F: 1s22s22p5.
- Nguyên tố d là nguyên tố nhóm B mà nguyên tử có cấu hình electron phân lớp ngoài cùng và phân lớp sát lớp ngoài cùng là (n – 1)d1÷10ns1÷2. Nguyên tố thuộc khối d: Cr: [Ar]3d54s1 và Cu: [Ar]3d104s1.
A. s.
B. p.
C. d.
D. f.
Lời giải:
Đáp án đúng là: D
Các nguyên tố f được xếp riêng bên dưới bảng tuần hoàn.
Lời giải:
- Khối s là các nguyên tố có cấu hình electron lớp ngoài cùng là ns1÷2, tức là cấu hình electron đang hoàn thành phân lớp s. Phân lớp s chỉ chứa tối đa 2 electron, nên khối s chỉ có 2 cột, ứng với hai cấu hình electron lớp ngoài cùng là ns1 và ns2.
- Tương tự, khối p là các nguyên tố mà cấu hình electron lớp ngoài cùng là ns2np1÷6, tức là cấu hình electron đang hoàn thành phân lớp p. Phân lớp p chứa tối đa 6 electron nên khối p có 6 cột, ứng với 6 cấu hình electron lớp ngoài cùng: ns2np1; ns2np2; ns2np3; ns2np4; ns2np5; ns2np6.
Lời giải:
Vì chu kì là tập hợp các nguyên tố có cùng số lớp electron nên số lượng các ô trong một chu kì bằng số lượng electron trong một lớp.
Ở lớp thứ nhất chỉ chứa tối đa 2 electron (vào phân lớp 1s); ở lớp thứ hai chỉ chứa tối đa 8 electron (vào phân lớp 2s, 2p) nên chu kì 1 có 2 nguyên tố và chu kì 2 có 8 nguyên tố.
Với chu kì 3, sau khi điền đầy đủ phân lớp 3s và 3p (8 electron ứng với số lượng 8 nguyên tố), thì chuyển sang điền electron vào phân lớp 4s chứ không phải 3d, nên chu kì 3 chỉ có 8 nguyên tố.
Chu kì 4 sẽ hoàn thiện các phân lớp 4s, 4p (tổng số electron tối đa trên các phân lớp này là 8 electron) và cả phân lớp 3d (tối đa 10 electron) nên chu kì 4 có 18 nguyên tố.
Lời giải:
Cấu hình electron Ca (Z = 20): 1s22s22p63s23p64s2. Vậy Ca ở:
+ Ô thứ 20 (do Z = 20)
+ Chu kì 4 (do có 4 lớp electron)
+ Nhóm IIA (do nguyên tố s, 2 electron ở lớp ngoài cùng).
(1) Cho một dãy số, trong đó mỗi số là tổng của số hiệu nguyên tử và số lớp electron của một nguyên tử ứng với một nguyên tố hoá học.
(2) Chữ cái đầu tiên trong kí hiệu hoá học của mỗi nguyên tố thu được từ việc giải mã dãy số ở quy tắc thứ nhất sẽ tương ứng với một chữ cái trong mật mã.
Em hãy thử giải mật mã theo quy tắc trên với dãy số sau: 8, 2, 69, 29, 58, 19, 26, 42, 76 (các chữ cái của mật mã sắp xếp theo đúng thứ tự tương ứng với các con số).
Lời giải:
Dựa vào bảng tuần hoàn ta có thể xác định được số thứ tự của chu kì của nguyên tố đó, cũng tức là số lớp electron chỉ có thể nằm trong khoảng từ 1 đến 7. Kết quả thu được như sau:
Mật mã: CHEMISTRY
Xem thêm các bài giải SBT Hoá học lớp 10 Cánh diều hay, chi tiết khác:
Bài 5: Lớp, phân lớp và cấu hình electron
Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bài 8: Định luật tuần hoàn và ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Lý thuyết Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
I.Lịch sử phát minh
- D. I. Mendeleev (1834 – 1907), một nhà Hóa học người Nga, được coi là cha đẻ của bảng tuần hoàn các nguyên tố hóa học.
- Mendeleev nhận thấy có mối liên hệ giữa khối lượng nguyên tử và tính chất các nguyên tố tương ứng qua dãy một số nguyên tố có tính chất tương tự nhau: dãy halogen (Cl, Br, I), kim loại kiềm (K, Rb, Cs), kim loại kiềm thổ (Ca, Sr, Ba). Ông sắp xếp chúng vào một bảng với khối lượng nguyên tử tương ứng như sau:
Bảng 6.1. Cách sắp xếp 9 nguyên tố hóa học theo khối lượng nguyên tử của Mendeleev
|
Cl = 35,5 |
Br = 80 |
I = 127 |
|
K = 39 |
Rb = 85,4 |
Cs = 133 |
|
Ca = 40 |
Sr = 87,6 |
Ba = 137 |
- Sau đó bằng cách thêm các nguyên tố khác theo mô hình này Mendeleev đã công bố phiên bản mở rộng của bảng tuần hoàn vào năm 1869, bao gồm tất cả các nguyên tố đã biết, cũng như dự đoán nhiều nguyên tố mới. Ông cho rằng “Nếu các nguyên tố được sắp xếp theo thứ tự tăng dần khối lượng nguyên tử, sẽ xuất hiện sự tuần hoàn về các tính chất của chúng”.
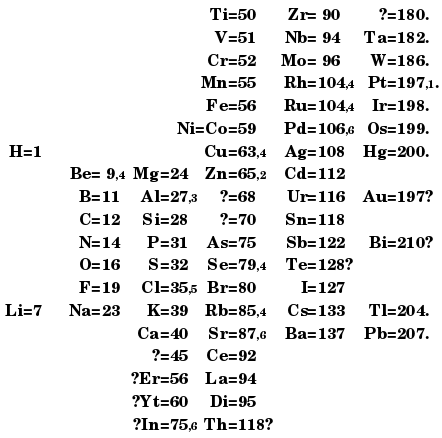
Hình 6.1. Bảng tuần hoàn các nguyên tố hóa học của Mendeleev năm 1869
- Năm 1871, Mendeleev đã đưa ra định luật tuần hoàn “Tính chất của các đơn chất, cấu tạo và tính chất các hợp chất của chúng có tính tuần hoàn theo khối lượng nguyên tử của các nguyên tố”. Nhờ định luật này, Mendeleev đã dự đoán tới 10 nguyên tố mới, trong đó có 3 nguyên tố được tiên đoán khá tỉ mỉ về tính chất của đơn chất và hợp chất của chúng (các nguyên tố Se, Ga và Ge).
- Bảng tuần hoàn các nguyên tố hóa học hiện đại ngày nay được xây dựng trên cơ sở sử dụng mối liên hệ “số hiệu nguyên tử - tính chất” thay vì mối liên hệ “khối lượng nguyên tử - tính chất”. Cách xây dựng này không những giúp nhanh chóng so sánh, suy luận về tính chất của đơn chất và hợp chất, mà còn cung cấp thông tin phong phú về mỗi nguyên tố hóa học.
II. Nguyên tắc sắp xếp của bảng tuần hoàn các nguyên tố hóa học
- Các nguyên tố hóa học được sắp xếp từ trái sang phải và từ trên xuống dưới theo chiều tăng dần điện tích hạt nhân của nguyên tử.
- Các nguyên tố mà nguyên tử có cùng số lớp electron được xếp vào cùng một hàng.
- Các nguyên tố mà nguyên tử có số electron hóa trị như nhau được xếp vào cùng một cột.
Lưu ý: Electron hóa trị là những electron có khả năng tham gia hình thành liên kết hóa học (thường là những electron ở lớp ngoài cùng).
III. Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bảng tuần hoàn các nguyên tố hóa học hiện nay (gọi tắt là bảng tuần hoàn) gồm 118 nguyên tố hóa học. Vị trí của mỗi nguyên tố hóa học trong bảng tuần hoàn được thể hiện qua số thứ tự ô nguyên tố, chu kì và nhóm.
1. Ô nguyên tố
- Mỗi nguyên tố hóa học được xếp vào một ô trong bảng tuần hoàn, gọi là ô nguyên tố.
- Mỗi ô chứa một số thông tin của một nguyên tố hóa học như: kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và nguyên tử khối trung bình, ...
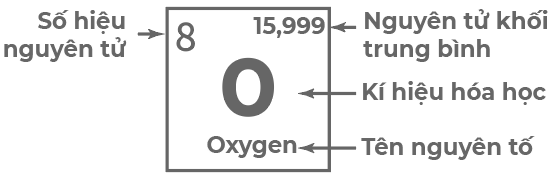
Hình 6.2. Các thông tin cơ bản trong một ô nguyên tố hóa học
- Số thứ tự của ô nguyên tố bằng số hiệu nguyên tử của nguyên tố đó.
Ví dụ: Nguyên tử O có số hiệu nguyên tử là 8 nên O nằm ở ô số 8 trong bảng tuần hoàn.
2. Chu kì
- Chu kì là tập hợp các nguyên tố hóa học mà nguyên tử của chúng có cùng số lớp electron, được xếp thành hàng theo chiều tăng dần điện tích hạt nhân từ trái sang phải.

Hình 6.3. Các chu kì nhỏ trong bảng tuần hoàn nguyên tố hóa học
- Bảng tuần hoàn gồm 7 chu kì, được đánh số từ 1 đến 7.
- Số thứ tự của chu kì bằng số lớp electron trong nguyên tử của các nguyên tố thuộc chu kì đó.
Ví dụ: Nguyên tử của nguyên tố O có 2 lớp electron nên O thuộc chu kì 2 của bảng tuần hoàn.
3. Nhóm
- Nhóm là tập hợp các nguyên tố hóa học mà nguyên tử có cấu hình electron tương tự nhau, được xếp thành cột theo chiều tăng dần điện tích hạt nhân từ trên xuống dưới.
- Các nguyên tố được chia thành nguyên tố nhóm A và nguyên tố nhóm B dựa theo sự khác nhau về đặc điểm cấu hình electron.
- Nguyên tử của các nguyên tố trong cùng một nhóm A (hoặc nhóm B) có cấu hình electron tương tự nhau nên có tính chất hóa học tương tự nhau.
- Bảng tuần hoàn gồm 18 cột, được chia thành 8 nhóm A, đánh số từ IA đến VIIIA; 8 nhóm B, được đánh số từ IB đến VIIIB. Mỗi nhóm A hay B đều chỉ có một cột, trừ nhóm VIIIB có ba cột.

Hình 6.4. Một số nhóm nguyên tố trong bảng tuần hoàn
IV. Liên hệ giữa cấu hình electron nguyên tử với vị trí của nguyên tố trong bảng tuần hoàn
Từ cấu hình electron nguyên tử của một nguyên tố hóa học, có thể xác định được vị trí của nguyên tố đó trong bảng tuần hoàn theo quy tắc sau:
- Số thứ tự của ô nguyên tố bằng số hiệu nguyên tử của nguyên tố đó.
- Số thứ tự của chu kì bằng số lớp electron trong nguyên tử của nguyên tố thuộc chu kì đó.
- Nguyên tố nhóm A có cấu hình electron lớp ngoài cùng dạng ns1÷2 hoặc ns2np1÷6 và nguyên tố nhóm B có cấu hình electron phân lớp ngoài cùng và phân lớp sát lớp ngoài cùng dạng ( n - 1)d1÷10ns1÷2.
Với nguyên tố nhóm A, số thứ tự của nhóm bằng số electron lớp ngoài cùng của nguyên tử nguyên tố đó (trừ He).
Ví dụ: Nguyên tử Na (Z = 11) với cấu hình electron nguyên tử là 1s22s22p63s1 có:
+ Số electron = số hiệu nguyên tử = số thứ tự của nguyên tố trong bảng tuần hoàn = 11
+ Số lớp electron = số thứ tự chu kì = 3
+ Cấu hình electron lớp ngoài cùng của Na là 3s1, có 1 electron nên nguyên tố Na thuộc nhóm IA.
Lưu ý:
- Nguyên tố nhóm B còn bao gồm các nguyên tố thuộc họ lanthanide và actinide.
- Với nguyên tố nhóm B, số thứ tự của nhóm bằng tổng số electron thuộc hai phân lớp (n - 1)d và ns. Nếu tổng số electron của hai phân lớp (n - 1)d và ns là 8, 9, 10 thì nguyên tố đó thuộc nhóm VIIIB; là 11 thì thuộc nhóm IB; là 12 thì thuộc nhóm IIB.
Ví dụ: Nguyên tử Fe (Z = 26) 1s22s22p63s23p63d64s2 có:
+ Số electron = số hiệu nguyên tử = số thứ tự của nguyên tố trong bảng tuần hoàn = 26
+ Số lớp electron = số thứ tự chu kì = 4.
+ Cấu hình electron phân lớp ngoài cùng và phân lớp sát ngoài cùng của Fe là 3d64s2, có 8 electron nên nguyên tố Fe thuộc nhóm VIIIB.
V. Phân loại nguyên tố hóa học
1. Dựa theo cấu hình electron
- Dựa vào cấu hình electron nguyên tử, người ta phân loại các nguyên tố hóa học thành các khối nguyên tố s, p, d, f.
- Nguyên tố s là nguyên tố nhóm A mà nguyên tử có cấu hình electron lớp ngoài cùng là ns1÷2.
Ví dụ: Nguyên tử Na (Z = 11) có cấu hình electron lớp ngoài cùng là 3s1 nên Na là nguyên tố s.
- Nguyên tố p là nguyên tố nhóm A mà nguyên tử có cấu hình electron lớp ngoài cùng là ns2np1÷6.
Ví dụ: Nguyên tử O (Z = 8) có cấu hình electron lớp ngoài cùng là 2s22p4 nên O là nguyên tố p.
- Nguyên tố d là nguyên tố nhóm B mà nguyên tử có cấu hình electron phân lớp ngoài cùng và phân lớp sát lớp ngoài cùng là (n-1)d1÷10ns1÷2.
Ví dụ: Nguyên tử Fe (Z = 26) có cấu hình electron phân lớp ngoài cùng và phân lớp sát lớp ngoài cùng là 3d64s2 nên Fe là nguyên tố d.
- Nguyên tố f là nguyên tố nhóm B mà nguyên tử có cấu hình electron phân lớp ngoài cùng và phân lớp sát lớp ngoài cùng là (n-2)f0÷14 (n-1)d0÷10ns1÷2. Các nguyên tố f được xếp riêng bên dưới bảng tuần hoàn.
Chú ý: Các khối nguyên tố d và f đều là kim loại.
2. Dựa theo tính chất hóa học
- Dựa vào tính chất hóa học, các nguyên tố hóa học được phân loại thành kim loại, phi kim và khí hiếm.