Tailieumoi.vn giới thiệu Giải bài tập Hóa học lớp 11 Bài 21: Công thức phân tử hợp chất hữu cơ chính xác, chi tiết nhất giúp học sinh dễ dàng làm bài tập Công thức phân tử hợp chất hữu cơ lớp 11.
Giải bài tập Hóa học lớp 11 Bài 21: Công thức phân tử hợp chất hữu cơ
Câu hỏi và bài tập( trang 95 SGK Hóa học 11)
Bài 1 trang 95 SGK Hóa học 11: Tính khối lượng mol phân tử của các chất sau:
a) Chất A có tỉ lệ khối hơi so với không khí bằng 2,07.
b) Thể tích hơi của 3,3 gam chất khí X bằng thể tích của 1,76 gam khí oxi (đo cùng điều kiện về nhiệt độ, áp suất).
Phương pháp giải :
a)
b)
Lời giải:
a) MA = dA/KK x = 2,07 x 29,0 = 60,0 (g/mol).
b) Trong cùng điều kiện, thể tích khí tỉ lệ thuận với số mol khí:
VX = => nX = = = 0,055 mol
=> MX = = 60 (g/mol)
Bài 2 trang 95 SGK Hóa học 11: Limonen là một chất có mùi thơm dịu được tách từ tinh dầu chanh. Kết quả phân tích nguyên tố cho thấy limonen được cấu tạo từ hai nguyên tố C và H, trong đó C chiếm 88,235% về khối lượng. Tỉ khối hơi của limonen so với không khí gần bằng 4,69. Lập công thức phân tử của limonen.
Phương pháp giải :
Mlimonen = 4,69 x MKK = ? (g/mol)
Gọi CTPT của limonen là CxHy;
=> công thức đơn giản nhất
Có phân tử khối => công thức phân tử của Limomen.
Lời giải:
Gọi công thức của limonen là CxHy
Ta có:
%H = 100% - %C = 100% - 88,235% = 11,765%
Dlimonen/kk = 4,69 Mlimonen = 4,69.29 = 136
Ta có:
= 7,35 : 11,765 = 5:8
x : y = 5: 8
Vậy công thức đơn giản nhất của limonen là (C5H8)n
Vì Mlimonen = 136 n(12.5 + 8.1) = 136 n = 2
Vậy công thức phân tử của limonen là C10H16
Bài 3 trang 95 SGK Hóa học 11: Đốt cháy hoàn toàn 0,3 gam chất A (phân tử chỉ chứa C, H, O) thu được 0,44 gam khí cacbonic và 0,18 gam nước. Thể tích hơi của 0,3 gam chất A bằng thể tích của 0,16 gam khí oxi (ở cùng điều kiện về nhiệt độ, áp suất).
Xác định công thức phân tử của chất A.
Phương pháp giải :
BTKL: mO = mA – mC - mH =?
Gọi CTPT của A là CxHyOz
=> Công thức đơn giản nhất
Có PTK của A => CTPT của A
Lời giải:
Cùng điều kiện về nhiệt độ và áp suất thì tỉ lệ thể tích bằng tỉ lệ số mol
BTKL => mO = mA – mC - mH = 0,3 - 0,01.12 - 0,02.1 = 0,16(g)
=> nO = 0,16/16 = 0,01 (mol)
Gọi CTPT của A là CxHyOz
=> Công thức đơn giản nhất là CH2O
Ta có: (CH2O)n =60
=> 30n = 60
=> n = 2
CTPT : C2H4O2
Bài 4 trang 95 SGK Hóa học 11: Từ tinh dầu hồi, người ta tách được anetol - một chất thơm được dùng sản xuất kẹo cao su. Anetol có khối lượng mol phân tử bằng 148,0 g/mol. Phân tích nguyên tố cho thấy, anetol có %C = 81,08%; %H = 8,10%, còn lại là oxi. Lập công thức đơn giản nhất và công thức phân tử của anetol.
Phương pháp giải:
Gọi công thức tổng quát của anetol là CxHyOz (x,y,z € N*)
%O = 100% - (%C + %H) = ?
Tìm được CTĐGN, có phân tử khối của anetol CTPT của anetol
Lời giải:
Gọi công thức tổng quát của anetol là CxHyOz (x,y,z € N*)
%O = 100% - (%C + %H) = 100% - (81,08 + 8,1)% = 10,82%
(Ta quy về các số nguyên tối giản bằng cách chia cho số nhỏ nhất trong các giá trị trên là 0,676)
=> Công thức đơn giản nhất của anetol là C10H12O
Ta có: M(C10H12O)n = 148 (g/mol)
=> (10.12 + 12 + 16).n = 148 => n=1
Vậy công thức phân tử là C10H12O
Bài 5 trang 95 SGK Hóa học 11: Hợp chất X có phần trăm khối lượng cacbon, hiđro và oxi lần lượt bằng 54,54%, 9,1% và 36,36%. Khối lượng mol phân tử của X bằng 88 g/mol. Công thức phân tử nào sau đây ứng với hợp chất của X?
A. C4H10O. B. C4H8O2.
C. C5H12O D. C4H10O2
Phương pháp giải:
Gọi công thức tổng quát của X là CxHyOz (x,y,z € N*)
Tìm được CT ĐGN, có phân tử khối của X => CTPT của X
Lời giải :
Gọi công thức tổng quát của X là CxHyOz (x,y,z € N*)
(Ta quy về các số nguyên tối giản bằng cách chia cho số nhỏ nhất trong các giá trị trên là 2,2725)
=> Công thức đơn giản nhất của X là C2H4O
=> Công thức tổng quát là (C2H4O)n
Ta có: MX = 88 (g/mol)
(12.2 + 4+ 16)n = 88
=> n = 2
Vậy công thức phân tử là C4H8O2
Đáp án B
Bài 6 trang 95 SGK Hóa học 11: Hợp chất Z có công thức đơn giản nhất là CH3O và có tỉ khối hơi so với hiđro bằng 31. Công thức phân tử nào sau đây ứng với hợp chất Z?
A. CH3O. B. C2H6O2.
C. C2H6O. D. C3H9O3.
Phương pháp giải:
Công thức tổng quát của Z là (CH3O)n
MZ = 31. MH2 = 31.2 = 62 (g/mol)
=> (CH3O)n = 62
=> n = ? => CTPT của Z
Lời giải:
MZ = 31 x 2 = 62 (g/mol)
Công thức tổng quát của Z: (CH3O)n. Phân tử khối của CH3O = 31
=> 31.n = 62
=> n = 2
=> CTPT của Z là C2H6O2.
Đáp án B
I. Công thức đơn giản nhất:
1. Định nghĩa
Công thức đơn giản nhất là công thức biểu thị tỉ lệ tối giản về số nguyên tử của các nguyên tố trong phân tử.
2. Cách thiết lập công thức đơn giản nhất
Thiết lập công thức đơn giản nhất của hợp chất hữu cơ CxHyOzNt là thiết lập tỉ lệ
II. Công thức phân tử
1. Định nghĩa
Công thức phân tử là công thức biểu thị số lượng nguyên tử của mỗi nguyên tố trong 1 phân tử.
2. Cách thiết lập công thức phân tử:
- Có ba cách thiết lập công thức phân tử
Cách 1 : Dựa vào thành phần % khối lượng các nguyên tố
- Cho CTPT CxHyOz: ta có tỉ lệ
Từ đó ta có :
; ;
Cách 2 : Dựa vào công thức đơn giản nhất.
Cách 3 : Tính trực tiếp theo khối lượng sản phẩm cháy.
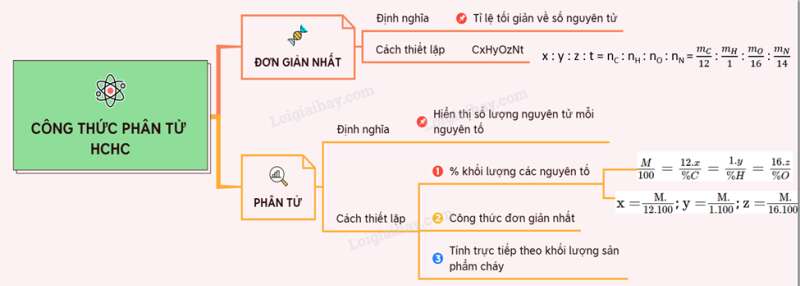
Sơ đồ tư duy: Công thức phân tử hợp chất hữu cơ
Phương pháp giải một số dạng bài tập về công thức phân tử hợp chất hữu cơ
Dạng 1
Lập công thức đơn giản nhất, công thức phân tử hợp chất hữu cơ khi biết thành phần phần trăm khối lượng của các nguyên tố.
* Một số lưu ý cần nhớ:
|
Để làm được dạng bài tập này ta cần: - Lập tỉ lệ mol của các nguyên tố trong hợp chất hữu cơ: n C : n H : n O : n N = = => CT ĐGN của hợp chất hữu cơ - Đặt CTPT thành (CTĐGN)n Biện luận giá trị của n => CTPT của hợp chất hữu cơ. |
* Một số ví dụ điển hình
Câu 1: Chất hữu cơ A chứa 7,86% H ; 15,73% N về khối lượng. Đốt cháy hoàn toàn 2,225 gam A thu được CO2, hơi nước và khí nitơ, trong đó thể tích khí CO2 là 1,68 lít (đktc). CTPT của A là (biết MA < 100) :
A. C6H14O2N.
B. C3H7O2N.
C. C3H7ON.
D. C3H7ON2.
Câu 1
Ta có :
Do đó : %O = (100 – 40,45 – 15,73 – 7,86)% = 35,96%.
Công thức đơn giản nhất của A là C3H7O2N.
Đặt công thức phân tử của A là (C3H7O2N)n. Theo giả thiết ta có :
(12.3 + 7 + 16.2 + 14).n < 100 => n < 1,12 => n =1
Vậy công thức phân tử của A là C3H7O2N.
Đáp án B
Câu 2: Một hợp chất hữu cơ Z có % khối lượng của C, H, Cl lần lượt là : 14,28% ; 1,19% ; 84,53%. CTPT của Z là :
A. CHCl2.
B. C2H2Cl4.
C. C2H4Cl2.
D. một kết quả khác.
Câu 2:
Ta có :
công thức đơn giản nhất của Z là CHCl2.
Đặt công thức phân tử của A là (CHCl2)n (n > 0).
Độ bất bão hòa của phân tử => n = 2
Vậy công thức phân tử của Z là : C2H2Cl4.
Đáp án B
Câu 3: Một chất hữu cơ A có 51,3% C ; 9,4% H ; 12% N ; 27,3% O. Tỉ khối hơi của A so với không khí là 4,034. CTPT của A là
A. C5H11O2N.
B. C10H22O4N2.
C. C6H13O2N.
D. C5H9O2N.
Câu 3:
Ta có :
=> công thức đơn giản nhất của A là C5H11O2N
Đặt công thức phân tử của A là (C5H11O2N)n
Theo giả thiết ta có :
(12.5 + 11 + 16.2 + 14).n = 4,034.29
=>n = 1
Vậy công thức phân tử của A là C5H11O2N.
Đáp án A
Dạng 2
Dựa vào quá trình phân tích định lượng để tìm ra công thức phân tử, công thức đơn giản nhất
* Một số lưu ý cần nhớ:
|
- Đặt công thức phân tử của hợp chất là CxHyOzNt . Lập sơ đồ chuyển hóa : CxHyOzNt + O2 → CO2 + H2O + N2 - Áp dụng định luật bảo toàn nguyên tố để tìm số nguyên tử C, H, O, N… trong hợp chất, suy ra công thức của hợp chất CxHyOzNt
|
* Một số ví dụ điển hình:
Ví dụ 1: Đốt cháy hoàn toàn m gam một amin X bằng lượng không khí vừa đủ thu được 17,6 gam CO2, 12,6 gam H2O và 69,44 lít N2 (đktc). Giả thiết không khí chỉ gồm N2 và O2 trong đó oxi chiếm 20% thể tích không khí. X có công thức là
A. C2H5NH2.
B. C3H7NH2.
C. CH3NH2.
D. C4H9NH2.
Hướng dẫn giải chi tiết:
Bảo toàn nguyên tố C:
Bảo toàn nguyên tố H:
Bảo toàn nguyên tố O:
Vì N2 chiếm 80% thể tích không khí, O2 chiết 20% thể tích không khí
Do đó :
Căn cứ vào các phương án ta thấy công thức của X là C2H5NH2
Đáp án A
Ví dụ 2: Oxi hóa hoàn toàn 4,02 gam một hợp chất hữu cơ X chỉ thu được 3,18 gam Na2CO3 và 0,672 lít khí CO2. CTĐGN của X là :
A. CO2Na.
B. CO2Na2.
C. C3O2Na.
D. C2O2Na.
Hướng dẫn giải chi tiết:
nNa2CO3 = 0,03 mol; nCO2 = 0,03 mol
Vì đốt cháy X thu được CO2 và Na2CO3 => trong X chứa C, Na và O
Bảo toàn nguyên tố Na:
Bảo toàn nguyên tố C:
Vậy CTĐGN của X là : CNaO2.
Đáp án A
Ví dụ 3: Một hợp chất hữu cơ A có tỉ khối so với không khí bằng bằng 2. Đốt cháy hoàn toàn A bằng khí O2 thu được CO2 và H2O. Có bao nhiêu công thức phân tử phù hợp với A ?
A. 2
B. 1
C. 3
D. 4
Hướng dẫn giải chi tiết:
Theo giả thiết ta có : MA = 29.2 = 58 gam/mol
Vì khi đốt cháy A thu được CO2 và nước nên thành phần nguyên tố trong A chắc chắn có C, H, có thể có hoặc không có O.
Đặt công thức phân tử của A là CxHyOz (y 2x + 2), ta có :
12x + y + 16z = 58 z
+ Nếu z = 0 12x + y = 58 A là C4H10
+ Nếu z = 1 12x + y = 42 A là C3H6O
+ Nếu z = 2 12x + y = 26 A là C2H2O2
Đáp án C
Dạng 3
Biện luận tìm công thức phân tử hợp chất hữu cơ
* Một số ví dụ điển hình:
Ví dụ 1: Hợp chất X có CTĐGN là C4H9ClO. CTPT nào sau đây ứng với X ?
A. C4H9ClO.
B. C8H18Cl2O2.
C. C12H27Cl3O3.
D. Không xác định được.
Hướng dẫn giải chi tiết:
Đặt công thức phân tử của X là (C4H9OCl)n (n N*).
Độ bất bão hòa của phân tử => n = 1
Vậy công thức phân tử của X là C4H9OCl
Đáp án A
Ví dụ 2: Hợp chất X có công thức đơn giản nhất là CH2O và có tỷ khối hơi so với hiđro bằng 90. Công thức phân tử của X là
A. CH2O
B. C4H8O4
C. C6H12O6
D. C2H4O2
Hướng dẫn giải chi tiết:
Đặt công thức phân tử (CTPT) của X là (CH2O)n (n Î N*).
Phân tử khối của X:
Vậy công thức phân tử của A là C6H12O6.
Đáp án C
Ví dụ 3: Hợp chất X có CTĐGN là CH3O. CTPT nào sau đây ứng với X ?
A. C3H9O3.
B. C2H6O2.
C. CH3O.
D. Không xác định được.
Hướng dẫn giải chi tiết:
Đặt công thức phân tử (CTPT) của X là (CH3O)n với .
Độ bất bão hòa của phân tử => n = 2
Vậy công thức phân tử của A là C2H6O2.
Đáp án B