Tailieumoi.vn xin giới thiệu phương trình NaOH + CO2 → NaHCO3 gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Natri. Mời các bạn đón xem:
Phương trình NaOH + CO2 → NaHCO3
1. Phương trình phản ứng hóa học:
NaOH + CO2 → NaHCO3
2. Hiện tượng nhận biết phản ứng
- Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
3. Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
4. Cách viết phương trình ion thu gọn của phản ứng CO2 tác dụng với NaOH
Bước 1: Viết phương trình phân tử:
CO2 + NaOH → NaHCO3
Bước 2: Viết phương trình ion đầy đủ bằng cách: chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion; các chất điện li yếu, chất kết tủa, chất khí để nguyên dưới dạng phân tử:
CO2 + Na+ + OH- → Na+ + HCO3-
Bước 3: Viết phương trình ion thu gọn từ phương trình ion đầy đủ bằng cách lược bỏ đi các ion giống nhau ở cả hai vế:
CO2 + OH- → HCO3-
5. Xác định sản phẩm của phản ứng CO2 tác dụng với NaOH
- CO2 phản ứng với NaOH chỉ thu được muối NaHCO3 khi T = .
- CO2 phản ứng với NaOH chỉ thu được muối Na2CO3 khi T = .
- CO2 phản ứng với NaOH thu được cả muối NaHCO3 và Na2CO3 khi 1< T =< 2.
6. Tính chất hóa học
6.1 Tính chất hóa học của NaOH
NaOH Là một bazơ mạnh nó sẽ làm quỳ tím chuyển màu xanh, còn dung dịch phenolphtalein thành màu hồng. Một số phản ứng đặc trưng của Natri Hidroxit được liệt kê ngay dưới đây.
Phản ứng với axit tạo thành muối + nước:
NaOHdd + HCldd→ NaCldd + H2O
Phản ứng với oxit axit: SO2, CO2…
2 NaOH + SO2→ Na2SO3 + H2O
NaOH + SO2→ NaHSO3
Phản ứng với muối tạo bazo mới + muối mới (điều kiện: sau phản ứng phải tạo thành chất kết tủa hoặc bay hơi):
2 NaOH + CuCl2→ 2NaCl + Cu(OH)2↓
Tác dụng với kim loại lưỡng tính:
2 NaOH + 2Al + 2H2O→ 2NaAlO2 + 3H2↑
2NaOH + Zn → Na2ZnO2 + H2↑
Tác dụng với hợp chất lưỡng tính:
NaOH + Al(OH)3 → NaAl(OH)4
2NaOH + Al2O3 → 2NaAlO2 + H2O
6.2. Tính chất hóa học của CO2
Cacbon dioxit (CO2) mang tính chất hóa học tiêu biểu của một oxit axit.
- CO2 tan trong nước tạo thành axit cacbonic (là một điaxit rất yếu)
- CO2 tác dụng với oxit bazơ → muối.
- CO2 tác dụng với dung dịch bazơ → muối + H2O
CO2 bền, ở nhiệt độ cao thể hiện tính oxi hóa khi tác dụng với các chất khử mạnh
7. Cách thực hiện phản ứng
- Dẫn khí CO2 từ từ đến dư vào ống nghiệm chứa NaOH và vài giọt chất chỉ thị.
8. Bạn có biết
- NaOH phản ứng với CO2 tùy theo tỉ lệ về số mol mà sản phẩm thu được có thể là muối cabonat trung hòa hoặc muối axit hoặc hỗn hợp cả hai muối.
- NaOH phản ứng với CO2 chỉ thu được muối NaHCO3 khi T = 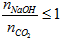
9. Bài tập liên quan
Ví dụ 1: Cho 0,1 mol NaOH phản ứng với lượng dư CO2 ở đktc thu được dung dịch X. Khối lượng muối tan có trong X là
A. 13,8 gam.
B. 12,8 gam.
C. 11,8 gam.
D. 8,4 gam.
Hướng dẫn giải
Do CO2 dư nên có phản ứng
Đáp án D.
Ví dụ 2: Dẫn khí CO2 từ từ đến dư vào dung dịch NaOH thu được dung dịch X.Muối tan có trong dung dịch X là
A. Na2CO3.
B. Na2CO3 và KHCO3.
C. NaHCO3.
D. Na2CO3 và NaOH.
Hướng dẫn giải
Do CO2 dư nên có phản ứng NaOH + CO2 → NaHCO3
Muối tan có trong dung dịch X là NaHCO3.
Đáp án C.
Ví dụ 3: Cho 2,24 lít khí CO2 ở đktc phản ứng với dung dịch chứa 0,05 mol NaOH. Khối lượng muối tan có trong dung dịch sau phản ứng là
A. 13,8 gam.
B. 12,8 gam.
C. 10 gam.
D. 4,2 gam.
Hướng dẫn giải
Có T = 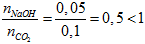
Đáp án D.
Ví dụ 4: “Nước đá khô” không nóng chảy mà dễ thăng hoa nên được dùng để tạo môi trường lạnh và khô, rất tiện cho việc bảo quản thực phẩm. “Nước đá khô” là
A. SO2 rắn.
B. CO2 rắn.
C. CO rắn.
D. H2O rắn.
Hướng dẫn giải:
Đáp án B
Nước đá khô là CO2 rắn.
Ví dụ 5: Cho khí CO2 vào lượng dư dung dịch nào sau đây sẽ tạo kết tủa?
A.MgCl2.
B. Ca(OH)2.
C. Ca(HCO3)2.
D.NaOH.
Hướng dẫn giải:
Đáp án B
A và C không phản ứng → loại.
D. CO2 + 2NaOHdư → Na2CO3 + H2O → loại.
B. CO2 + Ca(OH)2 dư → CaCO3↓ + H2O
Ví dụ 6: Chất khí nào sau đây, được tạo ra từ bình chữa cháy và dùng để sản xuất thuốc giảm đau dạ dày?
A. CO2.
B. N2.
C. CO.
D. CH4.
Hướng dẫn giải:
Đáp án A
Chất khí được tạo ra từ bình chữa cháy là CO2.
Thuốc giảm đau dạ dày là NaHCO3.
NaOH + CO2 → NaHCO3.
8. Một số phương trình phản ứng hóa học khác của Natri và hợp chất:
2NaOH + CuSO4 → Na2SO4 + Cu(OH)2↓
2NaOH + FeSO4 → Na2SO4 + Fe(OH)2↓