Với giải Bài 4 trang 71 Hóa học lớp 10 Chân trời sáng tạo chi tiết tron Bài 11: Liên kết hydrogen và tương tác van der waals giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 11: Liên kết hydrogen và tương tác van der waals
Bài 4 trang 71 Hóa học 10: Biểu diễn liên kết hydrogen giữa các phân tử:
a) Hydrogen fluoride
b) Ethanol (C2H5OH) và nước
Phương pháp giải:
Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết
Lời giải:
a) Hydrogen fluoride: Nguyên tử H của phân tử HF này liên kết với nguyên tử F của phân tử HF khác (biểu diễn bằng 3 nét gạch ---)
b) Ethanol (C2H5OH) và nước
- Ethanol (C2H5OH) và nước tồn tại 4 kiểu liên kết hydrogen như sau
+ H của C2H5OH liên kết hydrogen với O của H2O (I)
+ H của C2H5OH này liên kết hydrogen với O của C2H5OH khác (II)
+ H của H2O liên kết hydrogen với O của C2H5OH (III)
+ H của H2O này liên kết hydrogen với O của H2O khác (IV) 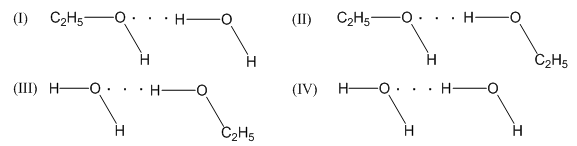
Bài tập vận dụng:
Câu 1. Hợp chất nào dưới đây tạo được liên kết hydrogen liên phân tử?
A. CH4
B. NH3
C. PH3
D. H2S
Đáp án đúng là: B
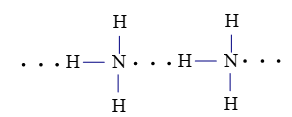
Hợp chất nào dưới đây tạo được liên kết hydrogen liên phân tử là NH3.
Liên kết hydrogen giữa nguyên tử H (liên kết với nguyên tử N có độ âm điện lớn) với nguyên tử N còn cặp electron hóa trị chưa tham gia liên kết.
Câu 2. Khẳng định đúng là
A. NH3 có độ tan trong nước lớn hơn PH3
B. NH3 có độ tan trong nước thấp hơn PH3
C. NH3 có độ tan trong nước tương tự PH3
D. Cả A, B và C đều sai.
Đáp án đúng là: A
NH3 có độ tan trong nước lớn hơn PH3 là đúng vì NH3 có thể tạo liên kết hydrogen với nước còn PH3 thì không. Do đó NH3 tan tốt trong nước.
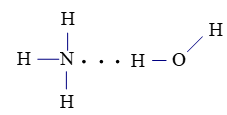
Câu 3. Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các
A. lưỡng cực tạm thời
B. lưỡng cực cảm ứng
C. lưỡng cực vĩnh viễn
D. một ion âm
Đáp án đúng là: A
Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời.

Xem thêm lời giải bài tập Hóa học 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 1 trang 71 Hóa học 10: Hợp chất nào dưới đây được liên kết hydrogen liên phân tử...
Bài 3 trang 71 Hóa học 10: Khí hiếm nào dưới đây có nhiệt độ sôi thấp nhất?...
Xem thêm các bài giải SGK Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 11: Liên kết hydrogen và tương tác van der waals
Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học