Với tóm tắt lý thuyết Khoa học tự nhiên lớp 9 Bài 23: Ethylic alcohol sách Cánh diều hay, chi tiết cùng với bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn KHTN 9.
Khoa học tự nhiên 9 Bài 23: Ethylic alcohol
A. Lý thuyết KHTN 9 Bài 23: Ethylic alcohol
I. Cấu tạo phân tử
- Ethylic alcohol có công thức phân tử C2H6O và có công thức cấu tạo: CH3 – CH2 – OH
- Trong phân tử ethylic alcohol có một nguyên tử H không liên kết với nguyên tử C mà liên kết với O tạo thành nhóm – OH
II. Tính chất vật lí
- Ethylic alcohol là chất lỏng, không màu, có mùi đặc trưng, vị cay, tan vô hạn trong nước, hòa tan được nhiều chất như iodine, benzene, xăng,…
- Ethylic alcohol sôi ở 78,3oC và có khối lượng riêng là 0,789 gam/cm3
- Độ cồn là số mililít ethylic alcohol nguyên chất có trong 100ml dung dịch ở 20oC.
III. Tính chất hóa học
1. Phản ứng cháy của ethylic alcohol
Ethylic alcohol cháy với ngọn lửa xanh mờ, tỏa nhiều nhiệt tạo ra CO2 và H2O theo phương trình hóa học:
C2H5OH + 3O2 2CO2 + 3H2O
2. Phản ứng của ethylic alcohol với natri
Ethylic alcohol tác dụng với Na tạo ra H2 theo phương trình hóa học:
2C2H5OH + 2Na 2C2H5ONa + H2
Trong phản ứng trên, nguyên tử H trong nhóm – OH đã được thay thế bởi nguyên tử Na
Nhóm – OH trong phân tử đã tạo ra những tính chất hóa học đặc trưng của ethylic alcohol.
IV. Điều chế ethylic alcohol
1. Điều chế từ tinh bột
Tinh bột glucose ethylic alcohol
2. Điều chế từ C2H4
CH2 = CH2 + HOH CH3 – CH2 – OH
V. Ứng dụng của ethylic alcohol
Ethylic alcohol được ứng dụng trong nhiều lĩnh vực của đời sống và sản xuất.

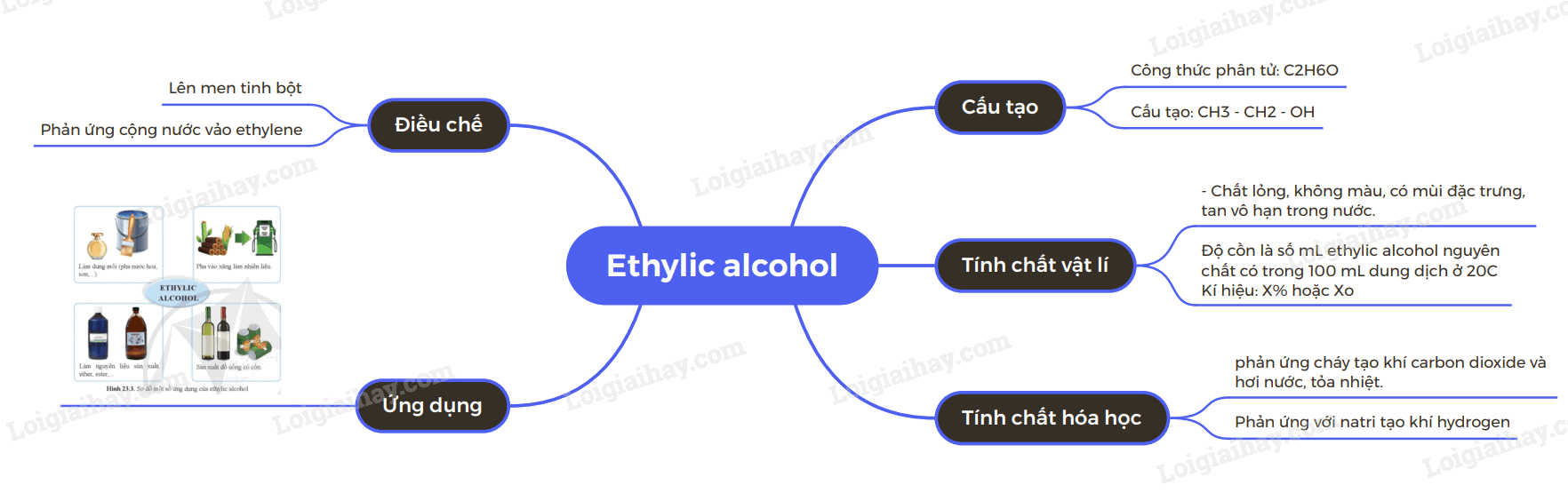
Sơ đồ tư duy Ethylic alcohol
B. Trắc nghiệm KHTN 9 Bài 23: Ethylic alcohol
Đang cập nhật …
Xem thêm các bài tóm tắt lý thuyết KHTN lớp 9 Cánh diều hay, chi tiết khác:
Lý thuyết Bài 22: Nguồn nhiên liệu
Lý thuyết Bài 23: Ethylic alcohol
Lý thuyết Bài 25: Lipid và chất béo
Lý thuyết Bài 26: Glucose và saccharose
Lý thuyết Bài 27: Tinh bột và cellulose