Lời giải bài tập Hóa học lớp 12 Bài 2: Xà phòng và chất giặt rửa tổng hợp sách Cánh diều hay, chi tiết sẽ giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập môn Hóa học 12. Mời các bạn đón xem:
Giải bài tập Hóa học 12 Bài 2: Xà phòng và chất giặt rửa tổng hợp
Lời giải:
Một số loại xà phòng: bột giặt, sữa tắm,…
Dựa vào đặc điểm cấu tạo của xà phòng nên xà phòng có khả năng làm sạch vết bẩn. Xà phòng được điều chế từ phản ứng xà phòng hóa
Câu hỏi 1 trang 14 Hóa 12: Hãy cho biết tác dụng và thành phần hóa học của xà phòng.
Lời giải:
Thành phần xà phòng: hỗn hợp các muối sodium hoặc potassium của acid béo và một số chất phụ gia.
Tác dụng: làm sạch các vết bẩn, chất diệt khuẩn, chất dưỡng da.
Lời giải:
Phần ưu nước (tan được trong nước) là nhóm carboxylate – COO – có xu hướng quay ra ngoài và thâm nhập vào nước.
Phần kị nước (không tan trong nước nhưng tan trong dầu, mỡ) là các gốc hydrocarbon mạch dài như C17H35-, C15H31-,…quay về phía vết dầu, mỡ và thâm nhập vào vết dầu, mỡ.
Luyện tập 1 trang 15 Hóa 12: Sodium acetate có tác dụng giặt rửa như xà phòng không? Vì sao?
Lời giải:
Sodium acetate không có tác dụng giặt rửa như xà phòng vì không có phần kị nước, CH3COONa tan hoàn toàn trong nước.
Lời giải:
Sau phản ứng xà phòng hóa, hỗn hợp muối của acid béo và glycerol được tách ra bằng cách cho dung dịch muối ăn bão hòa vào hỗn hợp sản phẩm. Các muối của acid béo nổi lên được lấy ra, sau đó được trộn với các phụ gia để làm xà phòng. Phần dung dịch còn lại gồm chất béo dư, NaOH dư, glycerol. Dùng phương pháp chiết để tách chất béo dư ra khỏi dung dịch. Sau đó sử dụng phương pháp chưng cất để thu hơi glycerol.
Thực hành trang 16 Hóa 12: Chuẩn bị:
- Hóa chất: Dầu thực vật (hoặc mỡ động vật), dung dịch NaOH 40%, dung dịch NaCl bão hòa
- Dụng cụ: Bát sứ, đũa thủy tinh, đèn cồn
Tiến hành: Cho vào bát sứ khoảng 2 ml dầu thực vật (hoặc khoảng 2g mỡ) và 4 – 5 ml dung dịch NaOH 40%. Đun hỗn hợp sôi nhẹ và khuấy đều bằng đũa thủy tinh. Thỉnh thoảng cho vài giọt nước cất để tránh hỗn hợp phản ứng bị cạn. Sau khoảng 10 phút thì dừng đun, cho thêm 10 ml dung dịch NaCl bão hòa và khuấy đều.
Yêu cầu: Quan sát, mô tả hiện tượng xảy ra và giải thích
Lời giải:
Hiện tượng: dầu thực vật tan ra khi cho NaOH vào, khi đun sôi nhẹ khuấy đều và cho dung dịch NaCl bão hòa sẽ có chất rắn nổi dần lên, tạo thành dung dịch không đồng nhất, phân thành 2 lớp.
Giải thích: dầu thực vật tác dụng với NaOH tạo thành muối acid béo. Khi nhỏ NaCl vào sẽ làm tỉ trọng dung dịch thay đổi nên muối acid béo nổi dần lên.
Lời giải:
Sử dụng bát sứ vì không tác dụng với các chất trong phản ứng và chịu được nhiệt trong phản ứng.
Không sử dụng bát nhôm hoặc xoong nhôm vì nhôm có phản ứng với dung dịch NaOH tạo muối NaAlO2
Lời giải:
Phần ưa nước của (1) là –OSO3-Na+; phần kị nước: CH3[CH2]10CH2 -
Phần ưa nước của (2) là: -SO3-Na+; phần kị nước: CH3[CH2]11-C6H4-
Lời giải:
Thành phần chất giặt rửa được điều chế từ dầu mỏ có chứa lưu huỳnh, khi sử dụng trong một thời gian dài sẽ ảnh hưởng đến chất liệu của quần áo, có thể gây dị ứng cho da nhạy cảm vì lưu huỳnh độc, ngoài ra khó phân hủy dễ gây ô nhiễm môi trường
Bài tập
A. Nước cất
B. Dung dịch sodium hydroxide
C. Dung dịch nước Javel
D. Dung dịch xà phòng
Lời giải:
Để tẩy vết dầu, mỡ bám trên quần áo, sử dụng dung dịch xà phòng.
Lời giải:
Chất giặt rửa tự nhiên: lấy từ thiên nhiên như quả bồ hòn, quả bồ kết,…lành tính, không gây kích ứng da, không gây ô nhiễm môi trường, giá thành cao vì các loại cây được sử dụng ngày càng khan hiếm
Chất giặt rửa tổng hợp: khó phân hủy dễ gây ô nhiễm môi trường, sử dụng tiện lợi và giá thành rẻ
a) Hãy dự đoán hiện tượng xảy ra và giải thích
b) Cũng làm thí nghiệm như trên nhưng thay nước xà phòng bằng nước giặt rửa. Hãy dự đoán hiện tượng xảy ra và giải thích.
Lời giải:
a) ống nghiệm (1) trong suốt, ống nghiệm (2) xuất hiện vẩn đục. Vì các chất trong xà phòng tác dụng với ion Ca2+ tạo kết tủa
b) Cả 2 ống nghiệm đều không có hiện tượng. Vì chất giặt rửa dùng được với nước chứa ion Ca2+
Lý thuyết Xà phòng và chất giặt rửa tổng hợp
I. Xà phòng
1. Khái niệm
Xà phòng là hỗn hợp các muối sodium hoặc potassium của acid béo và một số chất phụ gia. Các acid béo ở đây thường là acid no như palmitic acid, stearic acid.
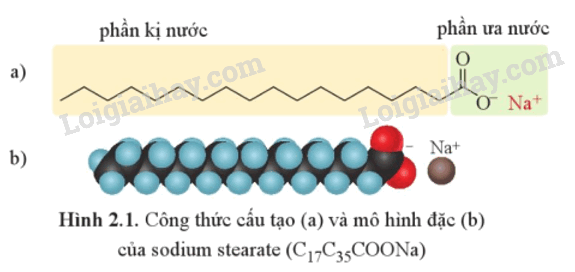
2. Đặc điểm cấu tạo phân tử muối của acid béo trong xà phòng
Muối của acid béo (có trong xà phòng) được cấu tạo gồm một phần ưa nước nối với một phần kị nước
+ Phần ưa nước (tan được trong nước) là nhóm carboxylate – COO-
+ Phần kị nước (không tan trong nước nhưng tan trong dầu, mở) là các gốc hydrocarbon mạch dài, như C17H35-, C15H31-,….
3. Cơ chế giặt rửa của xà phòng
- Khi cho xà phòng vào nước, tạo thành dung dịch xà phòng có sức căng bề mặt nhỏ, giúp xà phòng ngấm vào các sợi vải. Phần kị nước (chẳng hạn gốc C17H35- trong phân tử sodium stearate) quay về phía vết dầu, mỡ và thâm nhập vào vết dầu, mỡ; còn phần ưa nước (nhóm – COO-) lại có xu hướng quay ra ngoài và thâm nhập vào nước. Kết quả là vết dầu, mỡ bẩn bị phân chia thành các hạt rất nhỏ phân tán vào nước.. Nhờ đó, chúng bị rửa trôi khỏi bề mặt của vật cần giặt rửa.
4. Phương pháp sản xuất xà phòng
- Trong công nghiệp, để sản xuất xà phòng, người ta thường đun chất béo (mỡ động vật, dầu thực vật) với dung dịch kiềm đặc ở nhiệt độ cao.
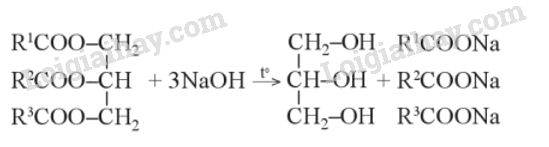
- Ngày nay, một phần xà phòng được sản xuất từ các alkane mạch dài lấy từ công nghiệp chế biến dầu mỏ theo sơ đồ sau:
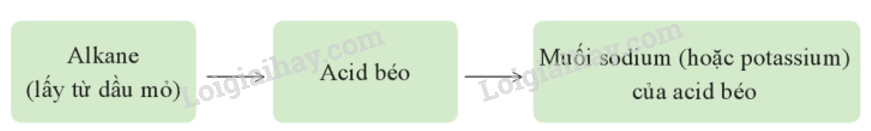
II. Chất giặt rửa
1. Chất giặt rửa tự nhiên
- Từ thời xa xưa, con người đã biết sử dụng các chất giặt rửa có nguồn gốc từ thiên nhiên như quả bồ hòn, quả bồ kết,…
- Saponin trong bồ hòn và bồ kết có khả năng giặt rửa. Khi tiếp xúc với nước, saponin tạo ra lớp bọt nhẹ tương tự xà phòng
2. Chất giặt rửa tổng hợp
- Những chất tổng hợp không phải là muối sodium hoặc potassium của acid béo, nhưng cũng có tính chất giặt rửa tương tự xà phòng được gọi chung là chất giặt rửa tổng hợp.
- Thành phần chính của chất giặt rửa tổng hợp điển hình các muối: CH3[CH2]10CH2SO3-Na+ (1) hoặc
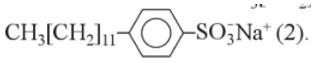
III. Ưu điểm và nhược điểm của các loại chất giặt rửa
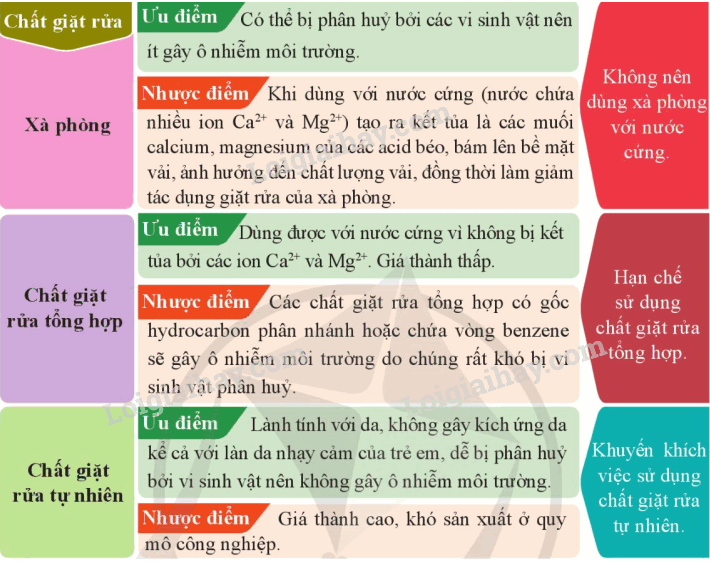
Sơ đồ tư duy Xà phòng và chất giặt rửa tổng hợp
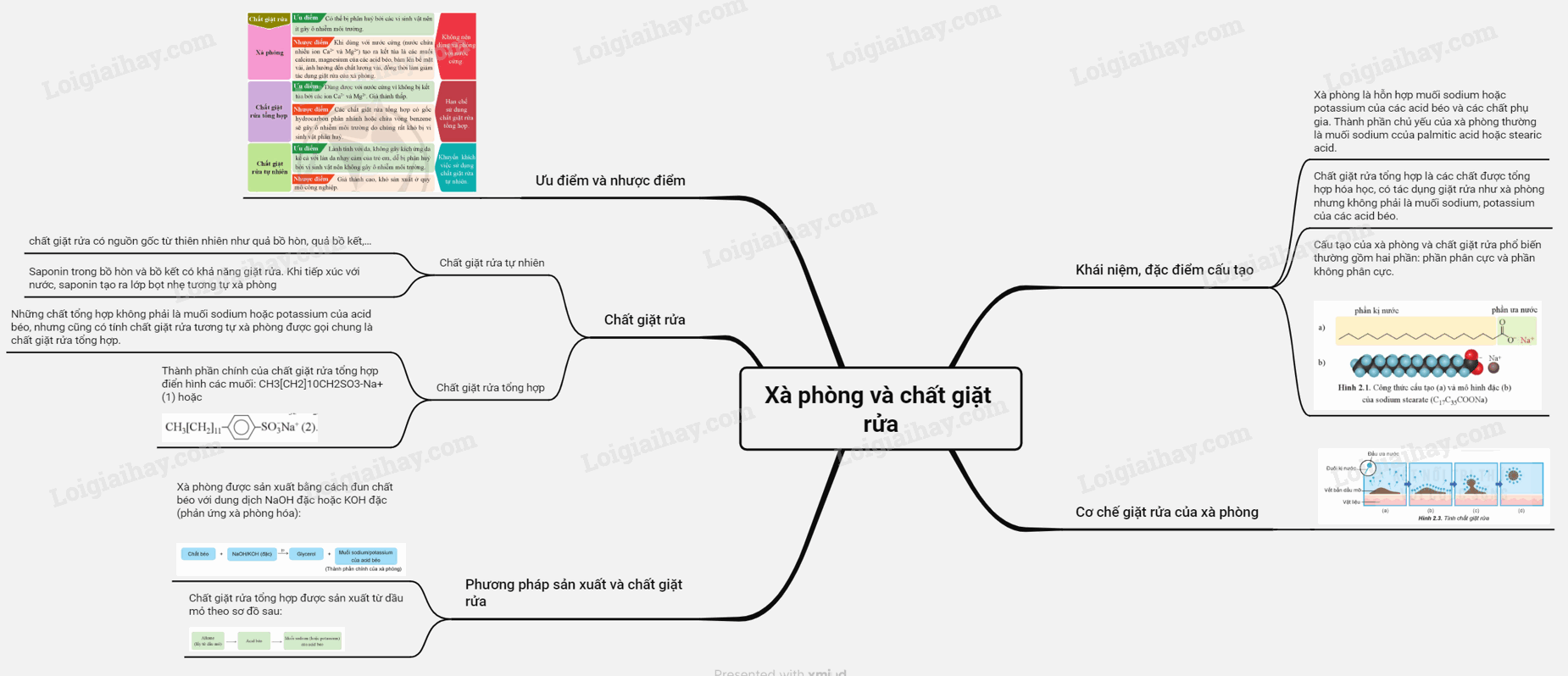
Xem thêm các bài giải bài tập Hóa Học lớp 12 Cánh diều hay, chi tiết khác:
Bài 2. Xà phòng và chất giặt rửa tổng hợp
Bài 3. Giới thiệu về carbohydrate
Bài 4. Tính chất hoá học của carbohydrate