Lời giải bài tập Hóa học lớp 12 Bài 14: Đặc điểm cấu tạo và liên kết kim loại. Tính chất kim loại sách Chân trời sáng tạo hay, chi tiết sẽ giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập môn Hóa học 12. Mời các bạn đón xem:
Giải bài tập Hóa học 12 Bài 14: Đặc điểm cấu tạo và liên kết kim loại. Tính chất kim loại
Lời giải:
- Cấu tạo nguyên tử: Trong cùng chu kì, nguyên tử của nguyên tố kim loại có bán kính nguyên tử lớn hơn và điện tích hạt nhân nhỏ hơn so với nguyên tử của nguyên tố phi kim. Đa số các nguyên tử kim loại có số electron ở lớp ngoài cùng là 1,2, 3.
- Tính chất:
+ Tính chất vật lí chung: tính ánh kim, tính dẫn điện, tính dẫn nhiệt và tính dẻo.
+ Tính chất hóa học:
· Kim loại tác dụng với phi kim.
· Kim loại tác dụng với dung dịch acid.
· Kim loại tác dụng với nước.
· Kim loại tác dụng với dung dịch muối.
- Ứng dụng: một số kim loại được dùng làm đồ trang sức hay làm các vật dụng trang trí; kim loại có tính dẫn điện tốt được dùng làm dây dẫn điện như Cu, Al; kim loại có tính dẫn nhiệt tốt có thể được dùng làm dụng cụ đun nấu…
Lời giải:
Các nguyên tử kim loại trên có số electron ở lớp ngoài cùng là 1 (như Na, Cu), 2 (như Mg, Fe, Zn), 3 (như Al).
Câu hỏi 2 trang 76 Hóa học 12: So sánh liên kết kim loại với liên kết ion và liên kết cộng hoá trị.
Lời giải:
* So sánh liên kết kim loại với liên kết cộng hóa trị:
- Giống nhau: có sự dùng chung electron.
- Khác nhau:
+ Liên kết cộng hóa trị: dùng chung electron giữa hai nguyên tử tham gia liên kết.
+ Liên kết kim loại: dùng chung toàn bộ electron hóa trị trong nguyên tử kim loại.
* So sánh liên kết kim loại với liên kết ion.
- Giống nhau: đều là liên kết sinh ra bởi lực hút tĩnh điện.
- Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu.
+ Liên kết kim loại: lực hút tĩnh điện sinh ra do các electron tự do trong kim loại và ion dương kim loại.
Lời giải:
Vàng, bạc được sử dụng làm đồ trang sức nhờ tính chất vật lí ánh kim và tính dẻo của kim loại.
Lời giải:
Khi tác dụng một lực cơ học đủ mạnh lên tấm kim loại, kim loại sẽ bị biến dạng vì kim loại có tính dẻo nhờ electron tự do liên kết các lớp mạng trong tinh thể với nhau và chúng có thể trượt lên nhưng không tách rời nhau.
Luyện tập trang 78 Hóa học 12: Hãy giải thích:
a) Tại sao tungsten (W) được dùng để làm dây tóc bóng đèn?
b) Tại sao lõi dây điện thường được làm từ kim loại đồng?
Lời giải:
a) Người ta sử dụng tungsten (W) được dùng để làm dây tóc bóng đèn vì tungsten là kim loại có nhiệt độ nóng chảy cao nhất.
b) Đồng có tính dẫn điện tốt (chỉ sau bạc), giá thành rẻ hơn bạc nên được sử dụng để làm lõi dây điện.
Phương pháp giải:
Hầu hết các kim loại (trừ Au, Pt,...) có thể phản ứng với chlorine tạo thành muối chloride.
Hầu hết các kim loại có thể phản ứng với oxygen (trừ Ag, Au, Pt) tạo thành các oxide tương ứng.
Nhiều kim loại có thể khử lưu huỳnh tạo thành các muối sulfide tương ứng. Phản ứng cần đun nóng (trừ Hg).
Lời giải:
- Hiện tượng phản ứng của thí nghiệm sắt phản ứng với chlorine: Sắt cháy sáng tạo thành khói màu nâu đỏ.
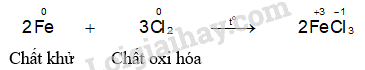
- Hiện tượng phản ứng của thí nghiệm magnesium phản ứng với oxygen: Magnesium cháy sáng chói, toả nhiều nhiệt.
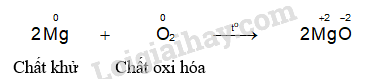
- Hiện tượng phản ứng của thí nghiệm sắt phản ứng với lưu huỳnh: Khi đốt nóng hỗn hợp, lưu huỳnh nóng chảy, hỗn hợp cháy sáng và bắt đầu chuyển thành hợp chất màu đen, phản ứng tỏa nhiều nhiệt.
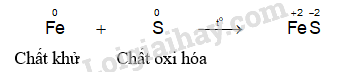
Lời giải:
Những kim loại có < 0 có khả năng phản ứng được với dung dịch HCl hoặc dung dịch H2SO4 loãng giải phóng khí H2: Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb.
Lời giải:
- Ống nghiệm (1): Không hiện tượng.
- Ống nghiệm (2): Xuất hiện bọt khí không màu, sắt tan dần và dung dịch chuyển sang màu xanh nhạt.

- Ống nghiệm (3): Không hiện tượng.
- Ống nghiệm (4): Xuất hiện bọt khí không màu, sắt tan dần và dung dịch chuyển sang màu xanh nhạt.
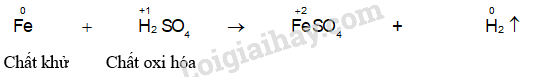
- Ống nghiệm (5): Mẩu kim loại đồng tan dần, xuất hiện bọt khí không màu, mùi hắc, dung dịch chuyển sang màu xanh lam.

Phương pháp giải:
Kim loại có < -0,42 có thể phản ứng với H2O tạo thành base và khí H2.
Lời giải:
Kim loại có thể phản ứng với H2O ở điều kiện thường giải phóng khí H2: Li, K, Ba, Ca, Na.
Lời giải:
Kim loại có < 0,34 và không phản ứng với nước ở điều kiện thường, có khả năng đẩy được đồng ra khỏi dung dịch CuSO4 1 M là Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb.
Lời giải:
- Ống nghiệm (1): Kết tủa màu xám bạc bám vào mẩu đồng. Dung dịch ban đầu không màu chuyển dần sang màu xanh.
Chất khử Chất oxi hóa
- Ống nghiệm (2): Không hiện tượng.
Bài tập
Lời giải:
Khi nhiệt kế thuỷ ngân bị vỡ có thể dùng bột lưu huỳnh để xử lí thuỷ ngân vì lưu huỳnh phản ứng với thủy ngân ngay ở nhiệt độ thường, tạo ra chất rắn HgS không độc, có thể quét dọn được.
Lời giải:
Dây điện cao thế thường sử dụng nhôm vì nhôm nhẹ hơn đồng, làm giảm áp lực lên cột điện, cột điện đỡ bị gãy. Ngoài ra, giá nhôm cũng rẻ hơn so với đồng.
Lời giải:
- Giải thích: Các kim loại thiếc, kẽm đều có thế điện cực chuẩn nhỏ hơn đồng nên thiếc và kẽm có thể đẩy được đồng ra khỏi dung dịch muối đồng. Vì vậy để làm tinh khiết bột đồng có lẫn các kim loại thiếc, kẽm, người ta có thể ngâm hỗn hợp trên vào lượng dư dung dịch Cu(NO3)2. Thiếc và kẽm tan trong dung dịch Cu(NO3)2, tạo thêm kết tủa đồng, lọc hỗn hợp ta thu được kim loại đồng tinh khiết.
- Phương trình hóa học:
Lý thuyết Đặc điểm cấu tạo và liên kết kim loại. Tính chất kim loại
1. Cấu tạo của kim loại
- Đa số các nguyên tử kim loại có số electron ở lớp ngoài cùng là 1,2,3
- Ở điều kiện thường, hầu hết kim loại ở thể rắn (trừ Hg) và có cấu tạo tinh thể.
- Trong tinh thể kim loại, lực hút tĩnh điện giữa các ion dương ở nút mạng với các electron hóa trị chuyển động tự do tạo nên liên kết kim loại
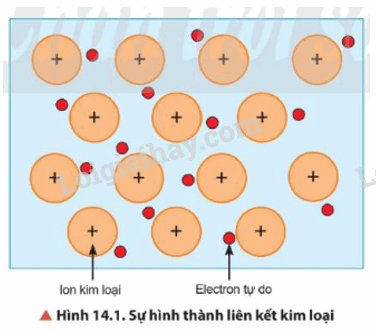
2. Tính chất vật lí của kim loại
- Kim loại có những tính vật lí chung: tính ánh kim, tính dẫn điện, tính dẫn nhiệt và tính dẻo.
a) Tính dẻo
- Kim loại có tính dẻo nên dễ rèn, dễ dát mỏng và dễ kéo sợi
- Tính chất này là do các cation kim loại trong tinh thể kim loại có thể trượt lên nhau mà không tách rời nhờ lực hút tĩnh điện giữa chúng với các electron hóa trị tự do.
b) Tính dẫn điện
Kim loại có tính dẫn điện. Tính dẫn điện tốt nhất là bạc, sau đó đến đồng, vàng, nhôm, sắt,…
c) Tính dẫn nhiệt
Khi đốt nóng một đầu dây kim loại, các electron hóa trị tự do ở vùng nhiệt độ cao có động năng lớn hơn di chuyển đến vùng có nhiệt độ thấp hơn trong tinh thể kim loại và truyền năng lượng cho các cation kim loại ở đây.
d) Ánh kim
Các electron hóa trị tự do trong tinh thể kim loại phản xạ hầu hết những tia sáng mà mắt con người nhìn thấy được, do đó kim loại có bề ngoài sáng lấp lánh, còn gọi là ánh kim
3. Tính chất hóa học của kim loại
- Hầu hết các kim loại (trừ Au, Pt,…) có thể phản ứng với chlorine tạo thành muối chloride.
- Hầu hết các kim loại có thể phản ứng với oxygen (Trừ Ag, Au, Pt) tạo thành các oxide tương ứng.
- Nhiều kim loại có thể khử lưu huỳnh tạo thành các muối sulfide tương ứng. Phản ứng cần đun nóng (trừ Hg)
- Kim loại có thế điện cực chuẩn âm () có khả năng khử được ion H+ (dung dịch HCl, H2SO4 loãng) ở điều kiện chuẩn, giải phóng khí H2
- Kim loại có thế điện cực chuẩn ) có khả năng khử được H2O ở điều kiện thường, giải phóng khí H2.
- Kim loại có thế điện cực nhỏ hơn có khả năng khử được ion kim loại có thế điện cực chuẩn lớn hơn trong dung dịch muối ở điều kiện chuẩn.
Sơ đồ tư duy Đặc điểm cấu tạo và liên kết kim loại. Tính chất kim loại
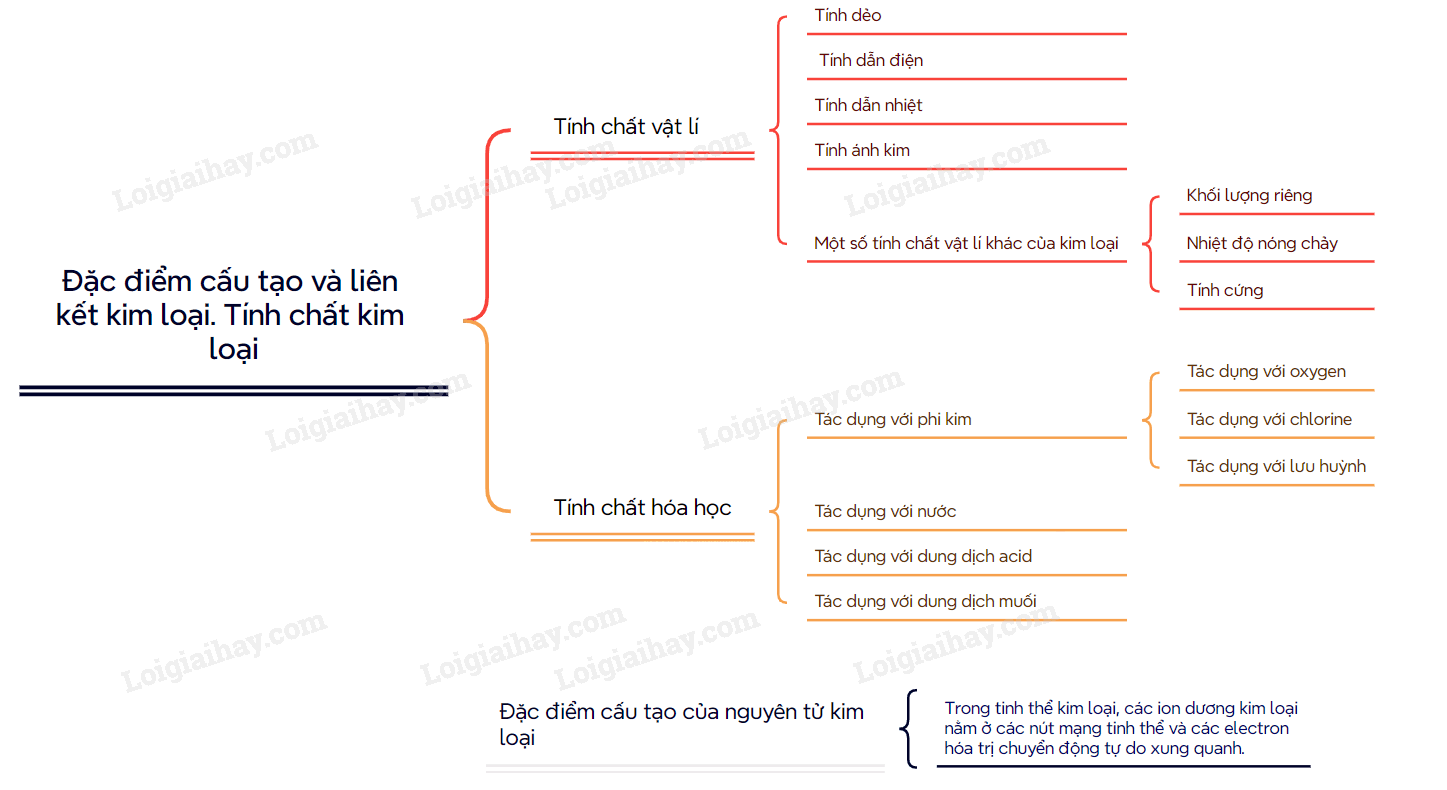
Xem thêm các bài giải bài tập Hóa Học lớp 12 Chân trời sáng tạo hay, chi tiết khác:
Bài 14. Đặc điểm cấu tạo và liên kết kin loại. Tính chất kim loại
Bài 15. Các phương pháp tách kim loại
Bài 16. Hợp kim – Sự ăn mòn kim loại