Tailieumoi.vn giới thiệu Giải bài tập Khoa học tự nhiên lớp 9 Bài 21: Alkene chi tiết sách Cánh diều giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập môn KHTN 9. Mời các bạn đón xem:
Giải bài tập KHTN 9 Bài 21: Alkene
Vật liệu dùng để sản xuất các đồ vật trên được tổng hợp từ những hydrocarbon thuộc loại alkene. Vậy alkene là gì?
Trả lời:
Các đồ vật trong hình 21.1 được làm từ nhựa.
Alkane là những hydrocarbon mạch hở, trong phân tử có một liên kết đôi.
Trả lời:
- Phân tử alkane chỉ gồm liên kết đơn. Ví dụ: CH4, CH3 – CH3, …
- Phân tử alkene ngoài liên kết đơn còn có liên kết đôi giữa 2 nguyên tử C.
Ví dụ: CH2 = CH2, CH3 – CH = CH2, …
Luyện tập 1 trang 105 KHTN 9: Viết công thức cấu tạo của các alkene có công thức phân tử C4H8.
Trả lời:
Công thức cấu tạo của các alkene có công thức phân tử C4H8:
CH2 = CH – CH2 – CH3
CH3 – CH = CH – CH3
Thực hành trang 106 KHTN 9: Thí nghiệm 1
Chuẩn bị
• Dụng cụ: ống cao su dẫn khí, ống thuỷ tinh, ống nghiệm, kẹp ống nghiệm, giá thí nghiệm, ống hút nhỏ giọt.
• Hoá chất: khí ethylene, nước bromine.
Tiến hành thí nghiệm và thảo luận
• Lắp ống nghiệm vào giá, cho vào ống nghiệm khoảng 2 mL nước bromine.
• Nối ống thuỷ tinh với ống dẫn khí ethylene, sau đó dẫn khí ethylene vào nước bromine (hình 21.2).
• Quan sát thí nghiệm, mô tả và giải thích các hiện tượng xảy ra
Trả lời:
- Khi dẫn khí ethylene vào ống nghiệm chứa nước bromine nhạt màu dần, sau đó mất màu. Vì ethylene đã phản ứng với bromine.
Phương trình hóa học:
CH2 = CH2 + Br2 → BrCH2 – CH2Br
Trả lời:
Hiện tượng trong thí nghiệm 1 chứng tỏ có phản ứng hoá học xảy ra khi dẫn ethylene vào nước bromine là: nước bromine mất màu.
Trả lời:
- Khi dẫn khí C2H4 qua ống nghiệm chứa nước bromine thấy nước bromine mất màu.
CH2 = CH2 + Br2 → BrCH2 – CH2Br
- Khi dẫn khí C2H6 qua ống nghiệm chứa nước bromine ta không thấy có hiện tượng gì.
Câu hỏi 3 trang 107 KHTN 9: Những hydrocarbon nào sau đây có thể tham gia phản ứng trùng hợp?
(a) CH4
(b) CH2 = CH2
(c) CH3 – CH = CH2
(d) CH3 – CH2 – CH = CH2
Trả lời:
Các hydrocarbon b, c, d có liên kết đôi C = C thì tham gia phản ứng trùng hợp.
Thực hành trang 107 KHTN 9: Thí nghiệm 2
Chuẩn bị
• Dụng cụ: ống cao su, ống thuỷ tinh vuốt nhọn, giá thí nghiệm.
• Hoá chất: khí ethylene.
Tiến hành thí nghiệm và thảo luận
• Nối ống thuỷ tinh vuốt nhọn với ống dẫn khí ethylene, sau đó kẹp vào giá thí nghiệm. Cho khí ethylene qua ống thuỷ tinh vuốt nhọn rồi đốt.
• Quan sát thí nghiệm, mô tả và giải thích các hiện tượng xảy ra.
Trả lời:
- Hiện tượng: Khi đốt ethylene thấy ngọn lửa cháy có màu xanh nhạt.
- Giải thích: Ethylene dễ cháy trong không khí tạo ra CO2 và H2O theo phương trình hoá học: C2H4 + 3O2 2CO2 + 2H2O.
Câu hỏi 4 trang 107 KHTN 9: Làm thế nào để xác định có khí CO2 tạo ra khi đốt cháy ethylene?
Trả lời:
Dẫn sản phẩm đốt cháy qua nước vôi trong, nếu thấy vẩn đục thì có khí CO2 tạo ra khi đốt cháy ethylene.
Phương trình hoá học minh hoạ:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Phương pháp trên dựa vào tính chất nào của ethylene? Viết phương trình hoá học minh hoạ.
Trả lời:
Phương pháp trên dựa vào tính chất dễ tham phản ứng cộng của ethylene.
Phương trình hóa học:
CH2 = CH2 + Cl2 Cl – CH2 – CH2 - Cl
Tìm hiểu thêm trang 108 KHTN 9: Ethylene và sự chín của trái cây
Chuẩn bị ba quả chuối xanh và một quả chuối vừa chín, hai túi zipper. Cho hai quả chuối xanh vào túi thứ nhất, quả chuối xanh còn lại và quả chuối chín vào túi thứ hai, đóng kín hai túi. Theo dõi quá trình chín của chuối trong hai túi. Tìm hiểu tác dụng của ethylene đối với sự chín của trái cây và giải thích hiện tượng quan sát được.
Trả lời:
Túi zipper chứa 1 quả chuối xanh và 1 quả chuối chín thì quả chuối xanh sẽ chín nhanh hơn so với hai quả chuối xanh trong túi zipper còn lại.
Giải thích: Do quả chuối chín có sản sinh là 1 lượng khí ethylene. Mà khí này có tác dụng làm cho hoa quả mau chín hơn.
Xem thêm các bài giải bài tập Khoa học tự nhiên 9 Cánh diều hay, chi tiết khác:
Lý thuyết KHTN 9 Bài 21: Alkene
I. Khái niệm alkene
Alkene là những hydrocarbon mạch hở, trong phân tử có một liên kết đôi.
II. Ethylene
1. Công thức cấu tạo và tính chất vật lí
Ethylene có công thức phân tử C2H4 và có công thức cấu tạo như sau: H2C = CH2
Ở điều kiện thường, ethylene là chất khí không màu, không mùi, nhẹ hơn không khí, ít tan trong nước.
2. Tính chất hóa học
Phản ứng làm mất màu nước bromine
Ethylene làm mất màu nước bromine theo phương trình hóa học sau:
H2C = CH2 + Br2 CH2Br – CH2Br
Phản ứng với bromine được gọi là phản ứng cộng
Tương tự ethylene, các alkene khác cũng làm mất màu nước bromine.
Phản ứng trùng hợp
Ở điều kiện thích hợp, ở phân tử ethylene cộng hợp liên kết với nhau, liên kết kèm bền trong liên kết đôi của phân tử ethylene bị phá vỡ theo phương trình sau
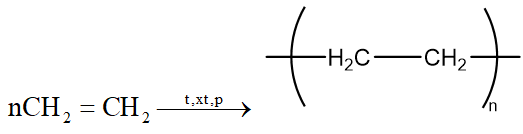
Phản ứng cháy
Ethylene khi cháy tọa khí CO2 và H2O
PTHH: C2H4 + 3O2 2CO2 + 2H2O
3. Ứng dụng
Một số ứng dụng quan trọng của ethylene: