 Giải bởi Vietjack
Giải bởi Vietjack
Lời giải:
Phân tử có kích thước lớn thường đi đôi với nhiều electron. Chính vì vậy, khả năng tạo các ion lưỡng cực tức thời và lưỡng cực cảm ứng của các phân tử có kích thước lớn cũng nhiều hơn, từ đó tương tác van der Waals giữa các phân tử lớn cũng mạnh hơn so với các phân tử có kích thước nhỏ.
Biểu diễn liên kết hydrogen giữa các phân tử sau:
a. methanol (CH3OH) và nước.
b. ethylene glycol (HOCH2CH2OH) và nước
Từ đó nhận xét tính tan của methanol và ethylene glycol trong nước.
Mặc dù chlorine có độ âm điện là 3,16 xấp xỉ với nitrogen là 3,04 nhưng giữa các phân tử HCl không tạo được liên kết hydrogen với nhau, trong khi giữa các phân tử NH3 tạo được liên kết hydrogen với nhau, nguyên nhân là do
Nhiệt độ sôi của các hợp chất với hydrogen của các nguyên tố nhóm VA, VIA và VIIA được biểu diễn qua đồ thị sau:
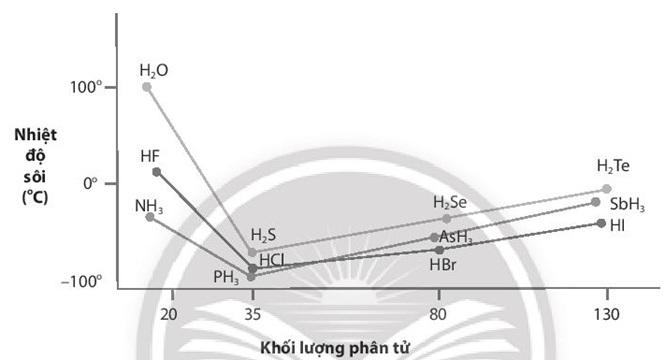
Giải thích nhiệt độ sôi cao bất thường của các hợp chất với hydrogen của các nguyên tố đầu tiên trong mỗi nhóm.