Cho 2 kí hiệu nguyên tử sau: .
Biểu diễn cấu hình electron của A, B theo ô orbital, từ đó cho biết số electron độc thân của mỗi nguyên tử.
 Giải bởi Vietjack
Giải bởi Vietjack
+ Dựa vào kí hiệu nguyên tử có ZA = 9.
Cấu hình electron nguyên tử A: 1s22s22p5.
Biểu diễn cấu hình electron nguyên tử A theo ô orbital:
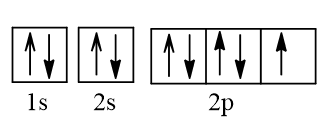
Vậy ở trạng thái cơ bản, A có 1 electron độc thân.
+ Dựa vào kí hiệu nguyên tử có ZB = 14.
Cấu hình electron nguyên tử B: 1s22s22p63s23p2.
Biểu diễn cấu hình electron nguyên tử B theo ô orbital:
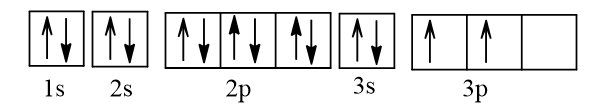
Vậy ở trạng thái cơ bản, B có 2 electron độc thân.
Nguyên tử của nguyên tố X có electron ở mức năng lượng cao nhất là 3p. Nguyên tử của nguyên tố Y cũng có electron ở mức năng lượng 3p và có một electron ở lớp ngoài cùng. Nguyên tử X và Y có số electron hơn kém nhau là 2. Nguyên tố X, Y lần lượt là
Trong tự nhiên nguyên tố copper (kí hiệu: Cu) có 2 đồng vị là và , trong đó đồng vị chiếm 27% về số nguyên tử. Tính phần trăm khối lượng của trong phân tử Cu2O (biết rằng nguyên tử khối trung bình của O bằng 16).
Nguyên tử nguyên tố X có tổng số hạt electron trong các phân lớp s là 5. Số electron của X ít hơn số electron của Y là 4 hạt.
Xác định vị trí X, Y trong bảng tuần hoàn có giải thích ngắn gọn.
Số hiệu nguyên tử của nguyên tố Y là 19. Vị trí của Y trong bảng tuần hoàn là
Nguyên tử sulfur có phân lớp electron ngoài cùng là 3p4. Phát biểu nào sau đây là sai khi nói về nguyên tử sulfur?
Số proton và số neutron có trong một nguyên tử aluminium () lần lượt là
Nguyên tử của nguyên tố M có cấu hình electron là 1s22s22p4. Số electron độc thân của M ở trạng thái cơ bản là