Tailieumoi.vn xin giới thiệu phương trình FeCl3 + 3NaHCO3 → 3NaCl + 3CO2 ↑ + Fe(OH)3↓ gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Sắt. Mời các bạn đón xem:
Phương trình FeCl3 + 3NaHCO3 → 3NaCl + 3CO2 ↑ + Fe(OH)3↓
1. Phương trình phản ứng hóa học
FeCl3 + 3NaHCO3 → 3NaCl + 3CO2 ↑ + Fe(OH)3↓
2. Hiện tượng nhận biết phản ứng
- Xuất hiện kết tủa đỏ nâu Fe(OH)3 đồng thời có khí CO2 thoát ra
3. Điều kiện phản ứng
- Nhiệt độ phòng.
4. Tính chất hoá học
4.1. Tính chất hoá học của FeCl3
- Tính chất hóa học của muối:
- Có tính oxi hóa: Khi tác dụng với chất khử, hợp chất sắt (III) clorua bị khử thành hợp chất sắt (II) hoặc kim loại sắt tự do.
Fe3+ + 1e → Fe2+
Fe3+ + 3e → Fe
Tính chất hóa học của muối:
- Tác dụng với dung dịch kiềm:
FeCl3 + 3KOH → Fe(OH)3 + 3KCl
- Tác dụng với muối
FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl
- Tác dụng với dung dịch axit:
- Sục khí H2S vào dung dịch FeCl3 có hiện tượng vẫn đục:
2FeCl3 + H2S → 2 FeCl2 + 2 HCl + S
Tính oxi hóa
Fe + 2FeCl3 → 3FeCl2
Cu + 2FeCl3 → 2FeCl2 + CuCl2
4.2. Tính chất hoá học của NaHCO3
- Tác dụng với axit mạnh (HCl, HNO3, H2SO4,...) tạo thành muối mới và giải phóng khí CO2.
NaHCO3 + HCl → NaCl + CO2 ↑+ H2O
- Tác dụng với dung dịch kiềm tạo thành muối trung hòa và nước.
2NaHCO3 + 2KOH → Na2CO3 + K2CO3 + 2H2O
- Bị nhiệt phân hủy.
2NaHCO3 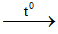
5. Cách thực hiện phản ứng
- Cho FeCl3 tác dụng với NaHCO3
6. Bài tập liên quan
Ví dụ 1: Cho bột sắt vào dung dịch HCl sau đó thêm tiếp vài giọt dung dịch CuSO4. Quan sát thấy hiện tượng nào sau đây?
A. Bọt khí bay lên ít và chậm dần.
B. Bọt khí bay lên nhanh và nhiều dần lên.
C. Không có bọt khí bay lên.
D. Dung dịch không chuyển màu.
Hướng dẫn giải
Đáp án : B
Ví dụ 2: Cho các dung dịch loãng: (1) FeCl3, (2) FeCl2, (3) H2SO4, (4) HNO3, (5) hỗn hợp gồm HCl và NaNO3. Những dung dịch phản ứng được với kim loại Cu là:
A. (1), (3), (4).
B. (1), (2), (3).
C. (1), (4), (5).
D. (1), (3), (5).
Hướng dẫn giải
Các dung dịch phản ứng được với Cu gồm : FeCl3, HNO3, hỗn hợp HCl và NaNO3
2FeCl3 + Cu → CuCl2 + FeCl2
8HNO3 + 3Cu → 3Cu(NO3)2+ 2NO + 4H2O
3Cu + 8HCl + 2NaNO3 → 3CuCl2 + NO + 2NaCl + 4H2O
Đáp án : C
Ví dụ 3: Quặng nào sau đây giàu sắt nhất?
A. Pirit sắt FeS2
B. Hematit đỏ Fe2O3
C. Manhetit Fe3O4
D. Xiđerit FeCO3
Hướng dẫn giải
Quặng giàu sắt nhất là manhetit Fe3O4 với hàm lượng sắt khoảng 72,4%
Đáp án : C
7. Một số phương trình phản ứng hoá học khác của Sắt (Fe) và hợp chất:
FeCl3 + 6H2O + 3NaAlO2 → 3Al(OH)3 ↓ + 3NaCl + Fe(OH)3↓
10FeCl3 + 24H2SO4 + 6KMnO4 → 15Cl2 ↑ + 5Fe2(SO4)3 +24H2O + 6MnSO4+ 3K2SO4
2FeS + 10H2SO4 → Fe2(SO4)3 + 9SO2 + 10H2O
FeS + 6HNO3 → 2H2O + H2SO4 + 3NO ↑ + Fe(NO3)3