Lời giải bài tập Hóa học lớp 10 Bài 1: Nhập môn hóa học sách Cánh diều hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 1 từ đó học tốt môn Hóa 10.
Giải bài tập Hóa học lớp 10 Bài 1: Nhập môn hóa học
Giải hóa học 10 trang 6 Cánh diều
Mở đầu trang 6 Hóa học 10: Nội dung nào dưới đây thuộc đối tượng nghiên cứu của hóa học?
(1) Sự hình thành hệ Mặt Trời
(2) Cấu tạo của chất và sự biến đổi của chất.
(3) Quá trình phát triển của loài người
(4) Tốc độ của ánh sáng trong chân không.
Phương pháp giải:
Hóa học là ngành khoa học thuộc lĩnh vực khoa học tự nhiên, nghiên cứu về thành phần, cấu trúc, tính chất, sự biến đổi của các đơn chất, hợp chất và năng lượng đi kèm những quá trình biến đổi đó.
Lời giải:
Hóa học nghiên cứu về thành phần, cấu trúc, tính chất, sự biến đổi của các đơn chất, hợp chất và năng lượng đi kèm những quá trình biến đổi đó
Đáp án (2)
I. Đối tượng nghiên cứu của hóa học
Phương pháp giải:
- Chất xung quanh ta được tạo nên từ nguyên tử của các nguyên tố hóa học, được phân thành đơn chất và hợp chất.
- Nguyên tử có kích thước vô cùng nhỏ, thể hiện đầy đủ tính chất hóa học của 1 nguyên tố
Lời giải:
Một số chất thông dụng xung quanh em và nguyên tử cấu tạo nên chất đó là:
- Chất: Sắt được cấu tạo từ nguyên tử của nguyên tố sắt (Fe)
- Chất: Gang được cấu tạo từ các nguyên tử của nguyên tố: sắt (Fe), carbon (C),…
- Chất: Cồn có thành phần chính là ethanol (C2H5OH) được cấu tạo từ các nguyên tử của nguyên tố: carbon (C), oxygen (O), hydrogen (H)
- Chất: Muối ăn có công thức hóa học là NaCl được cấu tạo từ các nguyên tử của nguyên tố: sodium (Na), chlorine (Cl)
- Chất: khí oxygen (O2) được cấu tạo từ nguyên tử của nguyên tố: oxygen (O)
Chú ý:
Cần phân biệt được nguyên tử và phân tử.
Ví dụ: phân tử oxygen (O2), nguyên tử oxygen (O)
Câu hỏi 2 trang 7 Hóa học 10: Hãy cho biết loại liên kết trong phân tử nước và trong muối ăn
Phương pháp giải:
- Các loại liên kết hóa học là:
+ Liên kết ion: liên kết được hành thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu (thường là giữa kim loại và phi kim)
+ Liên kết cộng hóa trị: liên kết được tạo nên giữa 2 nguyên tử bằng 1 hay nhiều cặp electron dùng chung (thường là giữa các phi kim)
+ Liên kết kim loại: liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thể do sự tham gia của các electron tự do
Lời giải:
- Nước (H2O) tạo bởi các nguyên tử các nguyên tố oxygen (O) và hydrogen (H), đều là các phi kim có độ âm điện không chênh lệch nhau nhiều nên trong phân tử nước có liên kết cộng hóa trị.
- Muối ăn (NaCl) tạo bởi kim loại điển hình sodium (Na) và phi kim điển hình chlorine (Cl) nên trong phân tử NaCl có liên kết ion.
Phương pháp giải:
- Tính chất vật lí: màu sắc, trạng thái, tính tan, nhiệt độ sôi, nhiệt độ nóng chảy
- Tính chất hóa học: khả năng cháy, khả năng tác dụng với chất khác
Lời giải:
- Những tính chất vật lí khác nhau:
+ Kim cương: Rất cứng và giòn, hoàn toàn trong suốt, không màu và lấp lánh.
+ Than chì: Màu đen, xếp thành lớp, rất mềm, sờ vào thấy trơn.
+ Than đá (khai thác từ mỏ): Màu đen, nhìn giống nhựa.
- Những tính chất hóa học khác nhau:
+ Kim cương: Rất khó cháy, chỉ cháy trong O2 tinh khiết ở nhiệt độ cao (khoảng 800oC)
+ Than chì: Cũng khó cháy nhưng dễ hơn kim cương
+ Than đá: Dễ cháy, khi cháy có khói, có tàn
Phương pháp giải:
- Một số phản ứng hóa học xảy ra trong tự nhiên:
+ Phản ứng quang hợp của cây xanh dưới ánh sáng mặt trời
+ Phản ứng oxi hóa thanh sắt để lâu ngày trong không khí ẩm
- Một số phản ứng hóa học xảy ra trong sản xuất:
+ Phản ứng tạo ra SO2
+ Phản ứng tạo ra NH3
Lời giải:
- Một số phản ứng hóa học xảy ra trong tự nhiên:
+ Trong tự nhiên, phản ứng quang hợp xảy ra trong tự nhiên dưới tác dụng của ánh sáng mặt trời:
6nCO2 + 5nH2O → (C6H10O5)n + 6nO2
+ Phản ứng quang hợp có vai trò đặc biệt quan trọng, nó tạo ra O2 giúp cân bằng lượng O2 đã bị tiêu thụ cho các hoạt động sống của con người, nó cũng tạo ra tinh bột là nguồn thức ăn quan trọng.
- Một số phản ứng hóa học xảy ra trong sản xuất:
+ Trong sản xuất, phản ứng tạo ra SO2:
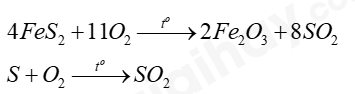
+ SO2 sản xuất ra có mục đích chính là sản xuất H2SO4, là hóa chất quan trọng hàng đầu trong nhiều ngành sản xuất
II. Phương pháp học tập và nghiên cứu hóa học
Câu hỏi 4 trang 7 Hóa học 10: Hãy cho biết sự khác nhau giữa biến đổi hóa học và biến đổi vật lí.Phương pháp giải:
- Biến đổi vật lí: chất vẫn giữ nguyên là chất ban đầu.
- Biến đổi hóa học: chất ban đầu bị thay đổi, chuyển hóa thành chất mới.
Lời giải:
- Biến đổi hóa học và biến đổi vật lí đều là sự biến đổi của chất nhưng kết quả của sự biến đổi khác nhua ở điểm:
+ Biến đổi vật lí: Chất vẫn giữ nguyên là chất ban đầu
Ví dụ: Nước đá (thể rắn) nóng chảy thành nước lỏng, nước lỏng sôi thành hơi nước, trong đó nước đá, nước lỏng, hơi nước đều có công thức là H2O
+ Biến đổi hóa học: Chất ban đầu bị thay đổi, chuyển hóa thành chất mới
Ví dụ: Đốt nóng hỗn hợp bột Fe (trắng xám) và S (vàng) sẽ tạo thành chất mới FeS (đen)
Câu hỏi 5 trang 7 Hóa học 10: Hãy nêu vai trò, ứng dụng của nước và oxygen mà em biết
Phương pháp giải:
- Oxygen:
+ Oxygen duy trì sự sống
+ Oxygen duy trì sự cháy
- Nước:
+ Sử dụng nước trong đời sống
+ Sử dụng nước trong công nghiệp
+ Sử dụng nước trong nông nghiệp
Lời giải:
Vai trò, ứng dụng của nước và oxygen
- Oxygen:
+ Oxygen có vai trò quyết định đối với sự sống của con người và động vật: Dùng O2 để hô hấp
+ Phần lớn (80%) lượng O2 sản xuất ra được dùng để luyện thép và công nghiệp hóa chất, từ đó sẽ tạo ra các sản phẩm phục vụ đời sống con người
+ Phần còn lại, O2 được dùng trong y khoa, hàn cắt kim loại, nhiên liệu cho tên lửa.
- Nước:
+ Nước là một phần không thể thiếu trong đời sống, mọi sinh vật đều sử dụng trực tiếp nước dưới dạng thức ăn, đồ uống
+ Nước cũng có vai trò quan trọng trong mọi ngành công nghiệp như để làm nguyên liệu, dung môi, chất rửa, chất làm lạnh…
+ Trong nông nghiệp, nước dùng để tưới cây trồng, tạo môi trường sống cho các loài sống dưới nước…
Giải hóa học 10 trang 8 Cánh diều
Phương pháp giải:
Đang cập nhật
Lời giải:
Đang cập nhật
Phương pháp giải:
Đang cập nhật
Lời giải:
Đang cập nhật
Vận dụng 4 trang 8 Hóa học 10: Vì sao không được đốt than, củi trong phòng kín?
Phương pháp giải:
Đang cập nhật
Lời giải:
Đang cập nhật
III. Vai trò của hóa học trong thực tiễn
Phương pháp giải:
Đang cập nhật
Lời giải:
Đang cập nhật
Giải hóa học 10 trang 9 Cánh diều
Vận dụng 5 trang 9 Hóa học 10: Vì sao hydrogen (H2) được coi là nhiên liệu của tương lai?
Phương pháp giải:
Vì H2 cháy trong không khí (có O2) sẽ tạo ra H2O (không gây ô nhiễm môi trường)
Lời giải:
- Hydrogen (H2) được coi là nhiên liệu của tương lai vì:
+ Khi H2 cháy chỉ tạo ra H2O, không có khí thải khác gây ô nhiễm môi trường
+ H2 cũng được sản xuất từ H2O (một nguồn nguyên liệu rất dồi dào)
Phương pháp giải:
- Nông nghiệp: Sản xuất phân đạm
- Công nghiệp: Sản xuất thuốc nổ, dược phẩm, nhiên liệu cho tên lửa, chất gây lạnh…
Lời giải:
- NH3 được dùng để sản xuất HNO3, một trong những hóa chất cơ bản, quan trọng trong công nghiệp. Từ HNO3 sẽ sản xuất ra phân đạm, thuốc nổ, dược phẩm, phẩm nhuộm…
- NH3 cũng dùng để sản xuất phân đạm, ngành công nghiệp không thể thiếu các loại phân đạm như (NH2)2CO, NH4NO3, (NH4)2SO4…
- Từ NH3 điều chế ra N2H4 làm nhiên liệu cho tên lửa
- Các máy lạnh công nghiệp dùng NH3 để làm chất gây lạnh
Phương pháp giải:
- Ca(OH)2 là hóa chất rẻ tiền
- Ca(OH)2 tác dụng với khí thải tạo thành muối, tác dụng với ion kim loại nặng tạo thành các base không tan => Dễ thu gom
Lời giải:
- Ca(OH)2 là 1 hóa chất rẻ tiền, có thể được sản xuất đễ dàng từ nguyên liệu sẵn có là đá vôi (CaCO3).
- Dùng Ca(OH)2 để xử lý sơ bộ khí thải hoặc nước thải vì Ca(OH)2 chuyển hóa khí thành dạng muối, nước thải thành các kết tủa ít độc hại hơn, dễ thu gom, vận chuyển và xử lý hơn.
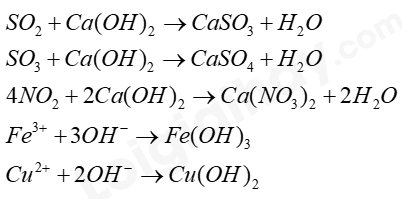
Lý thuyết Nhập môn hóa học
I. Đối tượng nghiên cứu của hóa học
1. Chất
- Tất cả những chất xung quanh ta đều được tạo nên từ các nguyên tử của các nguyên tố hóa học.
Ví dụ: Kim cương được tạo nên từ nguyên tử của nguyên tố carbon (C).
- Cấu tạo quyết định đến tính chất vật lí và hóa học của chất.
Ví dụ: Kim cương và than chì đều được tạo nên từ nguyên tử của nguyên tố carbon nhưng kim cương thì cứng, không màu, dẫn điện kém còn than chì lại mềm, màu xám đen và dẫn điện tốt. Điều này được giải thích là do sự khác nhau về cấu tạo của than chì và kim cương.
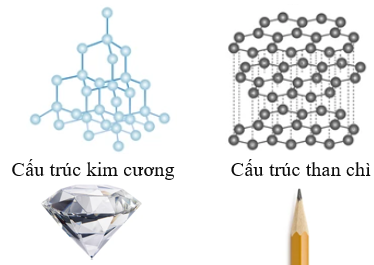 Hình 1.2. Cấu trúc của kim cương và than chì
Hình 1.2. Cấu trúc của kim cương và than chì
- Hiểu biết về cấu tạo hóa học góp phần dự đoán và giải thích tính chất của các chất.
2. Sự biến đổi của chất
- Hóa học nghiên cứu về các phản ứng xảy ra trong tự nhiên, chẳng hạn như trong khí quyển, trong các nguồn nước, trong cơ thể động vật và thực vật, trong sản xuất hóa học, ...
Ví dụ: Sắt bị gỉ do tiếp xúc với oxygen và hơi nước trong không khí.
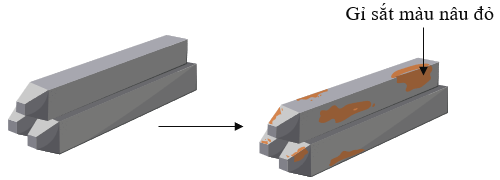 Hình 1.3. Thanh sắt bị gỉ do tiếp xúc với không khí ẩm
Hình 1.3. Thanh sắt bị gỉ do tiếp xúc với không khí ẩm
II. Phương pháp học tập và nghiên cứu hóa học
Một số điều cốt lõi cần thiết trong quá trình học tập môn Hóa học:
- Nắm vững nội dung chính của các vấn đề lí thuyết hóa học.
Các nội dung đó bao gồm: cấu tạo của chất, sự biến đổi vật lí và hóa học của chất, các yếu tố ảnh hưởng đến quá trình biến đổi chất, ứng dụng của chất, hóa học trong đời sống và sản xuất.
- Chủ động tìm hiểu thế giới tự nhiên thông qua các hoạt động khám phá.
Hoạt động khám phá trong môn Hóa học bao gồm:
+ Quan sát hoặc tiến hành quá trình thực nghiệm nghiên cứu, thu thập thông tin.
+ Phân tích, xử lí số liệu.
+ Giải thích, dự đoán được kết quả nghiên cứu một số sự vật hiện tượng trong tự nhiên và đời sống.
Hình thức của hoạt động khám phá bao gồm:
+ Tìm hiểu trên mạng internet.
+ Tham gia hoạt động trong lớp, trong phòng thí nghiệm.
+ Tham gia hoạt động ngoài lớp học do giáo viên, nhà trường tổ chức.
- Liên hệ, gắn kết những nội dung kiến thức đã học và kinh nghiệm đã được tích lũy trong quá trình tìm hiểu, khám phá để phát hiện, giải thích các hiện tượng tự nhiên, vận dụng vào các tình huống thực tiễn, ...
III. Vai trò của hóa học trong thực tiễn
1. Trong đời sống
Hóa học luôn ở xung quanh ta và có vai trò rất quan trọng trong cuộc sống.
- Hóa học về lương thực - thực phẩm: Con người cần sử dụng các loại lương thực – thực phẩm chứa các chất đường, tinh bột, chất đạm, chất béo, vitamin và khoáng chất để hoạt động và phát triển.
Ví dụ: Thịt, cá, trứng, sữa cung cấp chất đạm; trái cây cung cấp vitamin.
+ Trong cơ thể người, luôn diễn ra rất nhiều phản ứng hóa học, như phản ứng chuyển hóa thức ăn thành các dạng các dạng mà cơ thể có thể hấp thu, phản ứng oxi hóa – khử cung cấp năng lượng cho cơ thể.
- Hóa học về thuốc: Hóa học giúp tìm và sản xuất được những loại thuốc có hiệu quả điều trị cao, an toàn cùng như rẻ tiền.
Ví dụ: Cisplatin [PtCl2(NH3)2] thường được sử dụng để điều trị nhiều bệnh ung thư như: ung thư tinh hoàn, ung thư buồng trứng, ...
- Hóa học về mĩ phẩm: Nghiên cứu về hóa học giúp biết cách lựa chọn hoặc tạo ra những chất có màu sắc đẹp và an toàn, có mùi hương thích hợp và tồn tại lâu hơn, ...
Ví dụ: Son môi từ dầu gấc (chứa chủ yếu b - carotene) giúp môi hồng hào, không bị thâm môi mà còn mềm mại, không bị khô nứt môi.
- Hóa học về chất tẩy rửa: Xà phòng, bột giặt, nước rửa bát, ... là những ví dụ về việc sử dụng các chất hóa học với mục đích tẩy rửa trong gia đình.
2. Trong sản xuất
Con người đã chủ động tạo ra các quá trình hóa học phục vụ mục đích tồn tại và phát triển.
- Hóa học về năng lượng: Có rất nhiều phản ứng hóa học xảy ra kèm theo sự giải phóng năng lượng.
Ví dụ: Các quá trình đốt cháy nhiên liệu như xăng, dầu, than, củi, ... Nhiên liệu cần cho tất cả các quá trình sản xuất, các nhà máy nhiệt điện, ô tô, máy bay, tên lửa, ...
+ Hiểu biết về hóa học giúp lựa chọn được nhiên liệu phù hợp với từng quá trình sản xuất, đặc biệt là xu hướng sử dụng nhiên liệu sạch, nhiên liệu tái tạo trong tương lai.
- Hóa học về sản xuất hóa chất: Các hóa chất cơ bản như NH3, H2SO4, HCl, HNO3, ... có vai trò đặc biệt quan trọng, là nguyên liệu cho các ngành sản xuất khác, được sản xuất với lượng lớn trong các nhà máy sản xuất hóa chất.
Ví dụ: Một lượng lớn NH3 tổng hợp từ N2 và H2 được sử dụng để sản xuất phân đạm.
- Hóa học về vật liệu:
+ Các loại vật liệu mới, tiên tiến như vật liệu chịu nhiệt, chịu áp suất; vật liệu xúc tác nhằm đẩy nhanh tốc độ các phản ứng hóa học, ...
Ví dụ: Tantalum carbide (TaC) và hafnium carbide (HfC) là những vật liệu có thể được nhiệt độ tới 4000oC. Chúng là các vật liệu tiềm năng cho phần vỏ chịu nhiệt của những con tàu vũ trụ.
+ Các vật liệu thông thường như sắt, thép, xi măng, nhựa, ... đều được tạo ra từ các quá trình hóa học.
- Hóa học về mội trường: Nước thải, khí thải nhà máy trước khi xả ra môi trường phải được xử lí bằng các biện pháp thích hợp; khí thải động cơ ô tô, xe máy cũng cần phải được xử lí để đạt đến tiêu chuẩn cho phép.
Ví dụ: Khí thải chứa CO2, SO2, ... cũng như nước thải chứa ion kim loại nặng như Fe3+, Cu2+, ... ở một số nhà máy thường được xử lí bằng cách cho tác dụng với sữa vôi Ca(OH)2.
Bài giảng Hóa học 10 Bài 1: Nhập môn hóa học - Cánh diều
Xem thêm các bài giải SGK Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Bài 2: Thành phần của nguyên tử