Tailieumoi.vn giới thiệu Giải bài tập hóa học 8 Bài 15: Định luật bảo toàn khối lượng, chi tiết nhất giúp học sinh dễ dàng làm bài tập Định luật bảo toàn khối lượng lớp 8.
Giải bài tập Hóa học lớp 8 Bài 15: Định luật bảo toàn khối lượng
Câu hỏi và bài tập (trang 54 sgk Hóa học lớp 8)
b) Giải thích vì sao trong một phản ứng hóa học tổng khối lượng các chất được bảo toàn.
Lời giải:a) Định luật bảo toàn khối lượng: "Trong một phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng".
b) Giải thích: Trong phản ứng hóa học diễn ra sự thay đổi liên kết giữa các nguyên tử. Sự thay đổi này chỉ liên quan đến electron, còn số nguyên tử mỗi nguyên tố giữ nguyên và khối lượng nguyên tử thì không đổi, vì vậy tổng khối lượng các chất được bảo toàn.
Hãy tính khối lượng của bari clorua BaCl2 đã phản ứng.
Lời giải:
Phương trình chữ của phản ứng:
Natri sunfat + bari clorua Bari sunfat + natri clorua
Theo định luật bảo toàn khối lượng:
= 23,3 + 11,7 - 14,2 = 20,8 (g)
a) Viết công thức về khối lượng của phản ứng xảy ra.
b) Tính khối lượng của khí oxi đã phản ứng.
Lời giải:
a) Công thức về khối lượng của phản ứng:
mMg + mO2 = mMgO
b) Khối lượng của khí oxi tham gia phản ứng:
mO2 = mMgO – mMg
=> mO2 = 15 – 9 = 6(g)
1. Thí nghiệm
Đặt 2 cốc chứa dung dịch BaCl2 và Na2SO4 lên 1 đĩa cân. Đặt các quả cân lên đĩa còn lại sao cho 2 bên thăng bằng.
Sau đó, đổ cốc đựng dung dịch BaCl2 vào cốc đựng dung dịch Na2SO4, ta thấy xuất hiện chất kết tủa và kim cân vẫn ở vị trí thăng bằng.
=> có phương trình hóa học xảy ra
=> tổng khối lượng chất trước phản ứng bằng tổng khối lượng các chất sau phản ứng
2. Định luật bảo toàn khối lượng:
“Trong một phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng của các chất phản ứng”
Giả sử có phản ứng: A + B → C + D
Định luật bảo toàn khối lượng được viết như sau : mA + mB = mC + mD
VD: Cho phản ứng hóa học: Bari clorua + natri sunfat → bari sunfat + natri clorua
Công thức bảo toàn khối lượng là: mbari clorua + mnatri sunfat = mbari sunfat + mnatri clorua
3. Áp dụng:
Trong một phản ứng có n chất, nếu biết khối lượng của (n – 1) chất thì tính được khối lượng của chất còn lại.
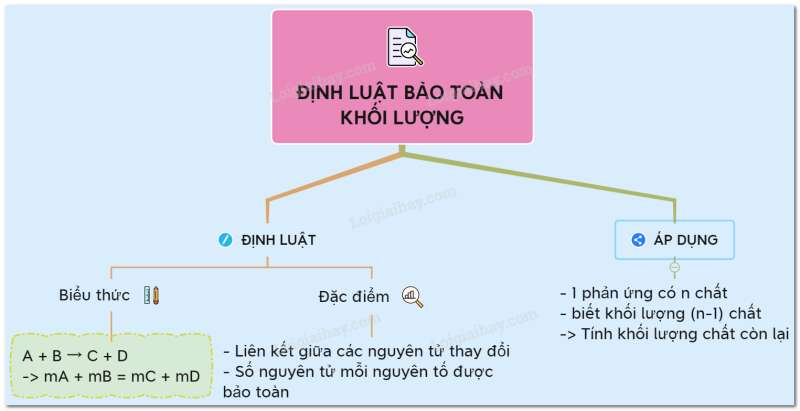
Sơ đồ tư duy: Định luật bảo toàn khối lượng