Tailieumoi.vn xin giới thiệu phương trình 2HCOOC2H5 + 7O2 → 6CO2 + 6H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình 2HCOOC2H5 + 7O2 → 6CO2 + 6H2O
1. Phản ứng hóa học:
2HCOOC2H5 + 7O2 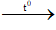
2. Điều kiện phản ứng
- Đốt cháy trong oxi hoặc không khí.
3. Cách thực hiện phản ứng
- Đốt cháy etyl fomat trong không khí, sau phản ứng thu được khí CO2 và hơi nước.
4. Hiện tượng nhận biết phản ứng
- Phản ứng cháy tỏa nhiều nhiệt, sản phẩm cháy làm đục nước vôi trong.
5. Tính chất hóa học
5.1. Tính chất hóa học của HCOOC2H5
a. Phản ứng thủy phân trong mỗi trường axit
HCOOC2H5 + H-OH 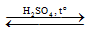
b. Phản ứng thủy phân trong mỗi trường kiềm
HCOOC2H5 + NaOH 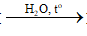
c. Phản ứng đốt cháy: Phản ứng oxi hóa hoàn toàn tạo CO2 và H2O
HCOOC2H5 + 7/2 O2 → 3CO2 + 3H2O
d. Tham gia vào phản ứng tráng bạc
HCOOC2H5 + 2AgNO3 + 3NH3 + H2O → 2Ag + 2NH4NO3 + NH4OCOOC2H5
5.2. Tính chất hóa học của O2
Khi tham gia phản ứng, nguyên tử O dễ dàng nhận thêm 2e. Nguyên tử oxi có độ âm điện lớn (3,44), chỉ kém flo (3,98).
Do vậy, oxi là nguyên tố phi kim hoạt động hoá học, có tính oxi hoá mạnh. Trong các hợp chất (trừ hợp chất với flo), nguyên tố oxi có số oxi hoá là -2.
Oxi tác dụng với hầu hết các kim loại (trừ Au, Pt, ...) và các phi kim (trừ halogen). Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ.
a. Tác dụng với kim loại
Tác dụng với hầu hết kim loại (trừ au và Pt), cần có to tạo oxit:
b. Tác dụng với phi kim
Tác dụng với hầu hết phi kim (trừ halogen), cần có to tạo oxit:
ĐB: Tác dụng với H2 nổ mạnh theo tỉ lệ 2:1 về số mol:
c. Tác dụng với hợp chất
- Tác dụng với các chất có tính khử:
- Tác dụng với các chất hữu cơ:
6. Bạn có biết
- Các este khác cũng có phản ứng cháy tương tự etyl fomat.
- Đốt cháy etyl fomat thu được CO2 và H2O có số mol bằng nhau.
7. Bài tập liên quan
Ví dụ 1: Khi đốt cháy etyl fomat thu được H2O và CO2 với tỷ lệ số mol là
A. > 1.
B. < 1.
C. = 1.
D. không xác định được.
Hướng dẫn:
Đáp án C.
Ví dụ 2: Đốt cháy 1 mol etyl fomat trong không khí cần số mol oxi là
A. 3,5.
B. 2.
C. 3.
D. 2,5.
Hướng dẫn:
Đáp án A.
Ví dụ 3: Nhận định nào sau đây là sai?
A. Etyl fomat khi bị đốt cháy và tỏa nhiều nhiệt.
B. Đốt cháy etyl fomat, sau phản ứng thu được khí CO2 và hơi nước.
C. Đốt cháy 0,1 mol etyl fomat trong không khí cần 0,35 mol oxi.
D. Khi đốt cháy hoàn toàn etyl fomat, sản phẩm thu được không làm đục nước vôi trong.
Hướng dẫn:
CO2 làm đục nước vôi trong.
Đáp án D.
8. Một số phương trình phản ứng hoá học khác của Este và hợp chất: