Với Giải hóa học lớp 10 trang 64 Cánh diều chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 64 Cánh diều
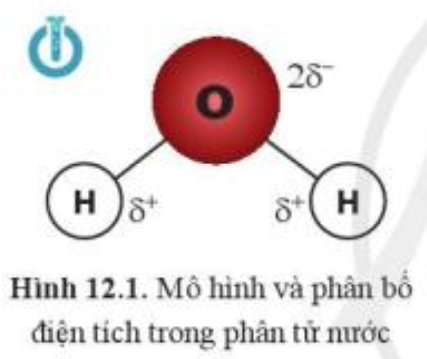
Mở đầu trang 64 Hóa học 10: Hai phân tử nước có thể liên kết được với nhau. Dựa vào sự phân bố điện tích trong phân tử nước (hình 12.1), cho biết liên kết giữa hai phân tử nước có thể được hình thành qua cặp nguyên tử nào?
(1) O với O
(2) H với H
(3) O với H
Giải thích sự lựa chọn của em.
Phương pháp giải:
Dựa vào lý thuyết liên kết hydrogen: Liên kết hydrogen là một loại liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron riêng. Các nguyên tố có độ âm điện lớn thường gặp trong liên kết ydrogen là N, O, F.
Lời giải:
Dựa vào sự phân bố điện tích trong phân tử nước (hình 12.1), liên kết giữa hai phân tử nước được hình thành qua cặp nguyên tử O với H.
Do nguyên tử H mang điện tích dương nên liên kết với nguyên tử mang điện tích âm là O. Ngoài ra O còn 2 cặp electron riêng và độ âm điện lớn hơn H. Vì vậy phân tử H2O được tạo bởi các liên kết hydrogen của cặp nguyên tử O – H, liên kết này có bản chất tĩnh điện, tương tác hút điện giữa và , giúp liên kết hai phân tử H2O với nhau.
Xem thêm các bài giải Hóa học lớp 10 Cánh diều tạo hay, chi tiết khác: