Với Giải hóa học lớp 10 trang 31 Chân trời sáng tạo chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 31 Chân trời sáng tạo
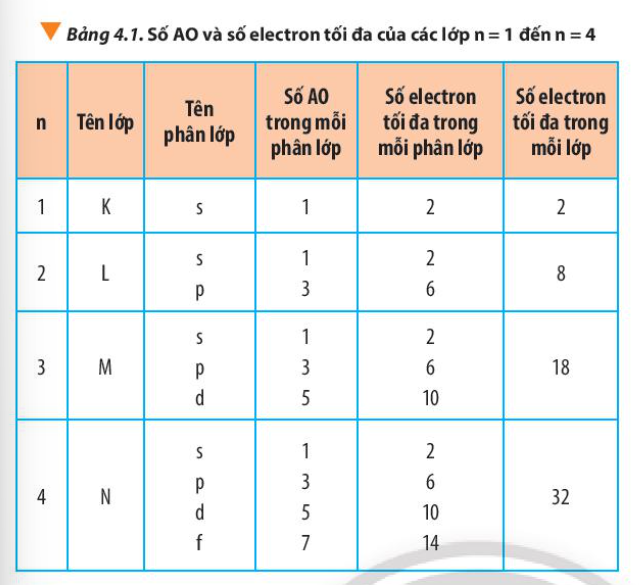
Câu hỏi 11 trang 31 Hóa học 10: Từ Bảng 4.1, hãy chỉ ra mối quan hệ giữa số thứ tự lớp và số electron tối đa trong mỗi lớp
Phương pháp giải:
Quan sát Bảng 4.1 và rút ra nhận xét
Lời giải:
- Lớp 1 có tối đa 2 electron = 2.12
- Lớp 2 có tối đa 8 electron = 2.22
- Lớp 3 có tối đa 18 electron = 2.32
- Lớp 4 có tối đa 32 electron = 2.42
=> Số electron tối đa trong lớp n là 2n2
Luyện tập 1 trang 31 Hóa học 10: Nguyên tử nitrogen có 2 lớp electron trong đó có 2 phân lớp s và 1 phân lớp p. Các phân lớp s đều chứa số electron tối đa, còn phân lớp p chỉ chứa một nửa số electron tối đa. Nguyên tử nitrogen có bao nhiêu electron?
Phương pháp giải:
Nitrogen có 2 lớp
- Lớp 1 có phân lớp 1s
- Lớp 2 có phân lớp 2s 2p
- Phân lớp s có tối đa 2 electron
- Phân lớp p có tối đa 6 electron
Lời giải:
Nitrogen có 2 lớp
- Lớp 1 có phân lớp 1s
- Lớp 2 có phân lớp 2s 2p
- Phân lớp s có tối đa số electron => 1s có 2 electron, 2s có 2 electron
- Phân lớp p chỉ chứa 1 nửa số electron tối đa => 2p có 3 electron
=> Nguyên tử nitrogen có số electron = 2 + 2 + 3 = 7 electron
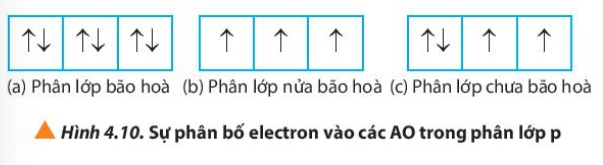
Câu hỏi 12 trang 31 Hóa học 10: Quan sát Hình 4.10, hãy nhận xét số lượng electron độc thân ở mỗi trường hợp
Phương pháp giải:
Quan sát Hình 4.10 và rút ra nhận xét
Lời giải:
(a) Phân lớp bão hòa => Không có electron độc thân
(b) Phân lớp nửa bão hòa => Số electron độc thân = số orbital của phân lớp đó
(c) Phân lớp chưa bão hòa => số electron độc thân nhỏ hơn số orbital trong phân lớp đó
Câu hỏi 13 trang 31 Hóa học 10: Hãy đề nghị cách phân bố electron vào các orbital để số electron độc thân là tối đa
Phương pháp giải:
Đang cập nhật
Lời giải:
Đang cập nhật
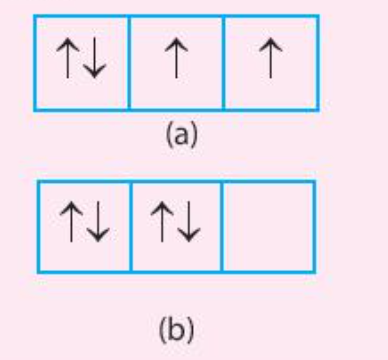
Luyện tập 2 trang 31 Hóa học 10: Trong các trường hợp (a) và (b) dưới đây, trường hợp nào có sự phân bố electron vào các orbital tuân theo và không tuân theo quy tắc Hund
Phương pháp giải:
Trong cùng một phân lớp chưa bão hòa, các electron sẽ phân bố vào các orbital sao cho số electron độc thân là tối đa
Lời giải:
Cả 2 trường hợp (a) và (b) đều chưa đạt được phân lớp bão hòa
- Trường hợp (a) có 2 electron độc thân => Số electron độc thân đã tối đa
- Trường hợp (b) không có electron độc thân => Số electron độc thân chưa tối đa
=> Trường hợp (a) tuân theo quy tắc Hund, trường hợp (b) không tuân theo quy tắc Hund
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác: