Tailieumoi.vn giới thiệu Giải sách bài tập Hóa học lớp 8 Bài 38: Luyện tập chương 5 chi tiết giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 8. Mời các bạn đón xem:
Giải SBT Hóa học 8 Bài 38: Luyện tập chương 5
Bài 38.1 trang 52 SBT Hóa học 8: a) Lập phương trình hoá học của các phản ứng sau :
(1) Lưu huỳnh đioxit + nước ;
(2) Sắt(III) oxit + hiđro ;
(3) Kẽm + dung dịch muối đồng(II) sunfat;
(4) Kẽm + axit sunfuric (loãng);
(5) Canxi oxit + nước.
b) Các loại phản ứng trên thuộc loại phản ứng nào ?
Phương pháp giải:
a) Vận dụng kiến thức đã học, học sinh tự viết PTHH
b) +) Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
+) Phản ứng phân hủy là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
+) Phản ứng oxi hóa – khử là phản ứng hóa học trong đó xảy ra đồng thời sự oxi hóa và sự khử.
+) Phản ứng thế là phản ứng hóa học trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
Lời giải:
a) Các phương trình hóa học:
b) - Phản ứng hóa hợp là các phản ứng : (1); (5).
- Phản ứng oxi hóa - khử là phản ứng : (2).
- Phản ứng thế là các phản ứng: (3), (4).
Bài 38.2 trang 52 SBT Hóa học 8: Có những cụm từ : Sự cháy, phản ứng phân huỷ, phản ứng hoá hợp, phản ứng toả nhiệt. Hãy chọn những cụm từ thích hợp để điền vào những chỗ trống trong các câu sau :
a) ............là phản ứng hoá học, trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
b) .............là phản ứng hoá học có sinh nhiệt trong quá trình xảy ra.
c) ............là phản ứng hoá học trong đó từ một chất sinh ra nhiều chất mới.
d) ............ là sự oxi hoá có toả nhiệt và phát sáng.
Đối với mỗi câu trên hãy dẫn ra một phương trình hoá học để minh hoạ.
Phương pháp giải:
Xem lại định nghĩa về các loại phản ứng để chọn từ thích hợp.
+) Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
+) Phản ứng phân hủy là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
+) Phản ứng oxi hóa – khử là phản ứng hóa học trong đó xảy ra đồng thời sự oxi hóa và sự khử.
+) Phản ứng thế là phản ứng hóa học trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
Lời giải:
a) Phản ứng hoá hợp là phản ứng hoá học, trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
Thí dụ :
b) Phản ứng toả nhiệt là phản ứng hoá học có sinh nhiệt trong quá trình xảy ra.
Thí dụ:
c) Phản ứng phân huỷ là phản ứng hoá học trong đó từ một chất sinh ra nhiều chất mới.
Thí dụ :
d) Sự cháy là sự oxi hoá có toả nhiệt và phát sáng.
Thí dụ:
Bài 38.3 trang 53 SBT Hóa học 8: Từ những hoá chất cho sẵn : KMnO4, Fe, dung dịch CuSO4, dung dịch H2SO4 loãng, hãy viết các phương trình hoá học để điều chế các chất theo sơ đồ chuyển hoá sau : Cu —> CuO —> Cu. Biết Fe có thể phản ứng với CuSO4 theo phương trình :
Phương pháp giải:
Nguyên liệu cần sử dụng là:
B1: Điều chế
B2: Điều chế
B3: Điều chế
Lời giải:
Nguyên liệu cần cho biến đổi hóa học là:
Bài 38.4 trang 53 SBT Hóa học 8: Khi điện phân nước thu được 2 thể tích H2 và 1 thể tích khí O2 (cùng điều kiện nhiệt độ, áp suất). Từ kết quả này, em hãy chứng minh công thức hoá học của nước.
Phương pháp giải:
PTHH:
Tính tỉ lệ => Điều phải chứng minh.
Lời giải:
Phương trình điện phân nước:
2V 1V
Trong cùng điều kiện nhiệt độ áp suất tỷ lệ thể tích bằng tỷ lệ mol, nên:
Suy ra:
Do đó công thức phân tử nước là
Bài 38.5 trang 53 SBT Hóa học 8: Để đốt cháy 68 g hỗn hợp khí hiđro và khí CO cần 89,6 lít oxi (ở đktc). Xác định thành phần phần trăm khối lượng của các khí trong hỗn hợp ban đầu. Nêu các phương pháp giải bài toán.
Phương pháp giải:
Cách 1:
Cách 2:
+) Gọi khối lượng khí CO là x g
+) Khối lượng là
+) PTHH:
+) Dựa vào PTHH lập pt biểu diễn số mol oxi theo số mol CO và H2
+) Giải pt => x => phần phần trăm khối lượng của các khí
Cách 3:
+) Gọi số mol CO là x ; số mol là y
+) Lập hệ pt 2 ẩn x, y.
+) Giải hệ pt => x, y => phần phần trăm khối lượng của các khí
Lời giải:
Cách 1:
Phương trình hóa học :
;
Số mol oxi:
- Từ các phương trình hóa học trên, ta nhận thấy:
2 mol hidro (hay CO) đều phản ứng với 1 mol oxi
8 mol hỗn hợp phản ứng với 4 mol oxi.
- Gọi số mol CO là x ; số mol là (8 - x ).
28x +2 ( 8 - x ) = 68
Giải ra ta có : x = 2.
Cách 2:
- Gọi khối lượng khí CO là x g
- Khối lượng là
Ta có phương trình :
Giải ra ta được : x = 56 g hay hay .
Sau đó tính % thể tích các chất như trên.
Cách 3:
Theo đề bài, ta có: 28x + 2y = 68.
- Phương trình hóa học :
x mol
y mol
Giải hệ phương trình 2 ẩn:
Giải ra ta có x= 2, y= 6. Sau đó tính thành phần phần trăm thể tích các chất như trên.
Bài 38.6 trang 53 SBT Hóa học 8: Khử 50 g hỗn hợp đồng(II) oxit và sắt(II) oxit bằng khí hiđro. Tính thể tích khí hiđro cần dùng, biết rằng trong hỗn hợp, đồng(II) oxit chiếm 20% về khối lượng. Các phản ứng đó thuộc loại phản ứng gì ?
Phương pháp giải:
+) Tính số mol đồng(II) oxit và sắt(II) oxit
+) PTHH:
+) Dựa theo PTHH, tính được số mol của hiđro theo số mol của oxit
+) Tính tổng số mol hiđro ở 2 phản ứng => cần dùng.
Lời giải:
Theo đề bài, CuO chiếm 20% về khối lượng, vậy:
trong hỗn hợp là:
=
=
Phương trình hóa học :
1 mol 1 mol
0,125 mol 0,125 mol
1 mol 1 mol
0,56 mol 0,56 mol
cần dùng là : 0,56 + 0,125 = 0,685 (mol)
cần dùng là : 0,685 x 22,4 = 15,334 (lít).
Các phản ứng trên thuộc loại phản ứng oxi hóa - khử
Bài 38.7 trang 53 SBT Hóa học 8: Cho 0,2 mol kẽm tác dụng với dung dịch có chứa 49 gam axit sunfuric.
a) Viết phương trình hóa học.
b) Sau phản ứng chất nào còn dư.
c) Tính thể tích khí hiđro thu được (đktc).
Phương pháp giải:
+) Tính số mol axit sunfuric.
+) Viết PTHH: Zn + H2SO4 → ZnSO4 + H2
+) Dựa thep PTHH, tìm được chất nào dư, chất nào phản ứng hết. Thể tích khí hiđro được tính theo chất phản ứng hết.
Lời giải:
b) Tỷ lệ số mol của Zn và H2SO4:
axit H2SO4 còn dư, kim loại Zn hết sau phản ứng.
c) Tính thể tích khí hiđro thu được theo số mol kim loại kẽm:
Bài 38.8 trang 53 SBT Hóa học 8: Trong phòng thí nghiệm có các kim loại Al, Fe và dung dịch HCl.
a) Cho cùng một khối lượng các kim loại trên tác dụng hết với dung dịch HCl thì kim loại nào cho khí hiđro nhiều hơn ?
b) Nếu thu được cùng một lượng khí hiđro thì khối lượng kim loại nào dùng ít hơn ?
Phương pháp giải:
a) +) Gọi khối lượng của các kim loại cùng tác dụng với dung dịch HCl là a.
+) PTHH:
+) Dựa theo phương trình, tính số mol hiđro theo số mol kim loại.
+) So sánh số mol hiđro thu được ở 2 PTHH => Kết luận.
b) Phần b) là bài toán ngược của phần a), học sinh làm tương tự.
Lời giải:
a) Gọi khối lượng của các kim loại cùng tác dụng với dung dịch HCl là a.
Phương trình hóa học
(2x27)g (3x22,4) lít
a g x lít
56 g 22,4 lít
a g y lít
Vậy cùng một lượng Al và Fe tác dụng hết với dung dịch HCl thì nhôm cho thể tích hiđro nhiều hơn sắt.
b) Nếu thu được cùng một lượng khí hiđro thì lượng nhôm dùng ít hơn lượng sắt.
Bài 38.9 trang 53 SBT Hóa học 8: Dùng khí H2 để khử hết 50 g hỗn hợp A gồm đồng(II) oxit và sắt(III) oxit. Biết trong hỗn hợp sắt(III) oxit chiếm 80% khối lượng. Thể tích khí H2 (đktc) cần dùng là
A. 29,4 lít. B. 9,8 lít.
C. 19,6 lít. D. 39,2 lít.
Phương pháp giải:
+) Tính số mol đồng(II) oxit và sắt(III) oxit
+) PTHH:
+) Dựa theo PTHH, tính được số mol của hiđro theo số mol của oxit
+) Tính tổng số mol hiđro ở 2 phản ứng => cần dùng.
Lời giải:
Theo đề bài:
1 mol 1 mol
0,125 mol 0,125 mol
1 mol 3 mol
0,25 mol 0,25 x 3 mol
cần dùng : 0,125 + 0,75 = 0,875 mol
cần dùng : 0,875 x 22,4 = 19,6 (lít).
=> Chọn C.
Bài 38.10 trang 53 SBT Hóa học 8: Viết công thức hoá học của các muối sau đây :
a) Canxi clorua ; b) Kali clorua ; c) Bạc nitrat;
d) Kali sunfat; đ) Magie nitrat; e) Canxi sunfat.
Lời giải:
a) CaCl2 ; b) KCl; c) AgNO3 ; d) K2SO4 ; đ) Mg(NO3)2 ; e) CaSO4.
Bài 38.11 trang 53 SBT Hóa học 8: a) Cho 13 g kẽm tác dụng với 0,3 mol HCl, khối lượng muối ZnCl2 được tạo thành trong phản ứng này là
A. 20,4 g. B. 10,2 g.
C. 30,6 g. D. 40 g
b) Có thể nói trong HCl có các đơn chất hiđro và clo được không ? Tại sao ?
Phương pháp giải:
a) +) Tính số mol kẽm.
+) Viết PTHH:
+) Dựa thep PTHH, tìm được chất nào dư, chất nào phản ứng hết. Khối lượng muối ZnCl2 được tính theo chất phản ứng hết.
b) Gợi ý: Không thể nói trong HCl có các đơn chất hiđro và clo.
Lời giải:
a) Phương án A.
Cần xác định lượng chất nào (Zn hay HCl) đã tác dụng hết để tính thể tích khí H2 sinh ra.
- Phương trình hoá học :
1 mol 2 mol 1 mol 1 mol
0,15 mol <— 0,3 mol —> 0,15 mol —> 0,15 mol
Theo phương trình hoá học trên và so với đề bài cho, lượng Zn dư, lượng HCl tác dụng hết, nên tính khối lượng ZnCl2 theo HCl.
Theo phương trình hoá học trên, ta có :
b) Không thể nói trong HCl có các đơn chất hiđro và clo, vì theo định nghĩa hợp chất do từ hai nguyên tố hoá học cấu tạo nên. Do đó chỉ có thể nói trong HCl có các nguyên tố hiđro và clo.
Bài 38.12 trang 54 SBT Hóa học 8: Thế nào là gốc axit ? Tính hoá trị của các gốc axit tương ứng với các axit sau: HBr, H2S, HNO3, H2SO4, H2SO3, H3PO4, H2CO3.
Phương pháp giải:
Gợi ý: Gốc axit là phần còn lại của phân tử axit sau khi tách riêng nguyên tử hiđro trong phân tử axit.
Lời giải:
Gốc axit là phần còn lại của phân tử axit sau khi tách riêng nguyên tử hiđro trong phân tử axit.
HBr : Gốc axit là Br có hoá trị I ; H2S : Gốc axit là S có hoá trị II.
HNO3 : Gốc axit là NO3 có hoá trị I ; H2SO4 : Gốc axit là SO4 có hoá trị II.
H2SO3 : Gốc axit là SO3 có hoá trị II ; H3PO4 : Gốc axit là PO4 có hoá trị III.
H2CO3 : Gốc axit là CO3 có hoá trị II.
Bài 38.13 trang 54 SBT Hóa học 8: a) Xác định hoá trị của Ca, Na, Fe, Cu, Al trong các hiđroxit sau đây : Ca(OH)2, NaOH, Fe(OH)3, Cu(OH)2, Al(OH)3.
b) Cho 1,35 g nhôm tác dụng với dung dịch chứa 7,3 g HCl. Khối lượng muối tạo thành là
A. 3,3375 g B. 6,675 g.
C. 7,775 g. D. 10,775 g.
Phương pháp giải:
a) Trong các hiđroxit trên, OH hóa trị I => hóa trị của kim loại chính bằng số nhóm OH.
b) +) Tính số mol Al và HCl
+) Viết PTHH:
+) Dựa thep PTHH, tìm được chất nào dư, chất nào phản ứng hết. Khối lượng muối được tính theo chất phản ứng hết.
Lời giải:
a) Trong phân tử bazơ, số nhóm OH bằng hoá trị của kim loại ; nhóm OH có hoá trị bằng I. Do đó trong :
Ca(OH)2 : Ca có hoá trị II ; NaOH : Na có hoá trị I ; Fe(OH)3 : Fe có hoá trị III ; Cu(OH)2 : Cu hoá trị II ; Al(OH)3 : Al có hoá trị III
b) Phương án B.
Phương trình hoá học :
2 mol 6 mol 2 mol
0,05 mol 0,2 mol x mol
Theo phương trình trên, ta nhận thấy dư HCl, nên tính số mol AlCl3 theo số mol Al :
Bài 38.14 trang 54 SBT Hóa học 8: Hãy nêu phương pháp nhận biết các khí: cacbon đioxit, oxi, nitơ, hiđro.
Phương pháp giải:
Gợi ý: +) Dùng than hồng => nhận ra oxi.
+) CO2: làm tắt ngọn nến đang cháy và làm đục nước vôi trong.
+) Hiđro: cháy được với ngọn lửa màu xanh.
+) Nitơ: làm tắt ngọn nến đang cháy và không làm đục nước vôi trong là khí nitơ.
Lời giải:
- Khí nào làm than hồng cháy sáng là khí oxi.
Khí nào làm tắt ngọn nến đang cháy và làm đục nước vôi trong là khí cacbon đioxit (CO2).
- Khi đưa que đóm đang cháy vào các khí, khí nào cháy được với ngọn lửa màu xanh, đó là khí hiđro. Hoặc có thể cho các khí còn lại qua CuO nung nóng, khí nào làm đổi màu CuO là khí hiđro.
(màu đen) (màu đỏ)
- Khí nào làm tắt ngọn nến đang cháy và không làm đục nước vôi trong là khí nitơ.
Bài 38.15 trang 54 SBT Hóa học 8: Cho 60,5 g hỗn hợp gồm hai kim loại kẽm Zn và sắt Fe tác dụng hết với dung dịch axit clohiđric. Thành phần phần trăm khối lượng của sắt trong hỗn hợp là 46,289%. Tính :
a) Khối lượng mỗi kim loại trong hỗn hợp.
b) Thể tích khí H2 (đktc) sinh ra.
c) Khối lượng các muối tạo thành.
Phương pháp giải:
a) Hướng dẫn giải : - Tính mFe và mZn trong 60,5 g —> nFe và nZn
Viết phương trình hoá học của phản ứng giữa Fe, Zn với dung dịch HCl. Dựa vào số mol Fe, Zn ta tính được thể tích khí H2 cũng như khối lượng 2 muối.
Lời giải:
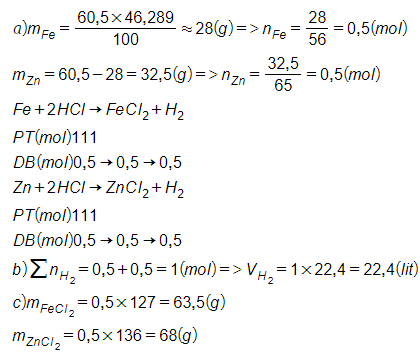
Đáp số :
Bài 38.16 trang 54 SBT Hóa học 8:
Phương pháp giải: Cho 22,4 g sắt tác dụng với dung dịch loãng có chứa 24,5 g axit H2SO4.
a) Tính thể tích khí H2 thu được ở đktc.
b) Chất nào dư sau phản ứng và dư bao nhiêu gam ?
Phương pháp giải:
Viết phương trình hoá học của phản ứng Fe tác dụng với axit H2SO4, tính nFe và từ đó dựa vào phương trình hoá học xem chất nào còn dư, chất nào tác dụng hết. Tính theo chất tác dụng hết.
Lời giải:
a) 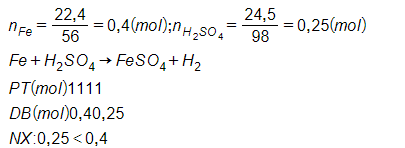
=> H2SO4 hết, Fe dư
b) mFe dư = (0,4 - 0,25) x 56=8,4(g)
Bài 38.17 trang 54 SBT Hóa học 8: Dẫn 6,72 lít (ở đktc) hỗn hợp hai khí H2 và CO từ từ qua hỗn hợp hai oxit FeO và CuO nung nóng, sau phản ứng thấy khối lượng hỗn hợp giảm m gam.
a) Viết các phương trình hoá học.
b) Tính m.
c) Tính phần trăm thể tích các khí, biết tỉ khối hỗn hợp khí so với CH4 bằng 0,45.
Phương pháp giải:
a)
b) Nx: số mol nguyên tử oxi trong oxit mất đi bằng số mol CO hay H2 tham gia => m.
c) Gọi số mol H2, CO trong 1 mol hỗn hợp lần lượt là x mol và y mol
Sử dụng phương pháp đường chéo => tỉ lệ => % thể tích từng khí.
Lời giải:
a) Các phựơng trình hoá học :
b) Khối lượng chất rắn giảm đi sau phản ứng do đã mất bớt các nguyên tử oxi trong oxit để tạo thành kim loại
Theo các phương trình hoá học (1), (2), (3), (4) số mol nguyên tử oxi trong oxit mất đi bằng số mol CO hay H2 tham gia.
Vậy khối lượng chất rắn giảm :
c) Gọi số mol H2, CO trong 1 mol hỗn hợp lần lượt là x mol và y mol
Áp dụng phương pháp đường chéo ta có:
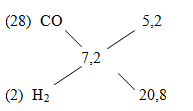
=>
Ta có :
Bài 38.18 trang 54 SBT Hóa học 8: Cho 3,6 g một oxit sắt vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được 6,35 g một muối sắt clorua. Hãy xác định công thức phân tử của oxit sắt.
Phương pháp giải:
Cách 1: Đặt công thức phân tử oxit sắt là FexOy
Viết PTHH:
Lập pt mối liên hệ giữa x, y => Công thức của oxit.
Cách 2 . Đặt công thức oxit sắt là Fe2Ox
Viết PTHH:
Cách 3 : Giải theo số mol FexOy hoặc số mol muối sắt clorua
Lời giải:
Cách 1: Đặt công thức phân tử oxit sắt là FexOy
Phương trình hoá học của phản ứng :
(56x+16y)g
3,6g 6,35g
6,35(56x+16y)=3,6(56x+71y)
-> x=y
Vậy công thức oxit sắt là FeO.
Cách 2 : Đặt công thức oxit sắt là Fe2Ox
Phương trình hoá học của phản ứng:
Dựa vào phương trình trên, ta có :
3,6 x 2(56+35,5x)=6,35(112+16x)
308x=616 -----> x=2
Công thức của oxit sắt là Fe2O2, giản ước ta có công thức phân tử của oxit sắt là FeO.
Cách 3 : Giải theo số mol FexOy hoặc số mol muối sắt clorua
Đặt công thức oxit sắt là FexOy
Phương trình hoá học của phản ứng :
mol
Công thức phân tử oxit sắt là FeO.
Bài 38.19 trang 54 SBT Hóa học 8: Cho dòng khí H2 dư qua 24 g hỗn hợp hại oxit CuO và Fe2O3 nung nóng. Tính khối lượng Fe và Cu thu được sau phản ứng. Biết rằng
Phương pháp giải:
+) Tính số mol Fe2O3 và CuO
+) PTHH:
+) Dựa theo PTHH, tính số mol Fe và Cu theo số mol Fe2O3 và CuO=> Khối lượng Fe và Cu.
Lời giải:
Phương trình hóa học của phản ứng:
1 mol 2 mol
0,1125mol 0,225mol
1 mol 1 mol
0,075mol 0,075mol
Bài 38.20 trang 54 SBT Hóa học 8: Cho 10,4 g oxit của một nguyên tố kim loại hoá trị II tác dụng với dung dịch HCl dư, sau phản ứng tạo thành 15,9 g muối. Xác định nguyên tố kim loại.
Phương pháp giải:
+) Gọi công thức phân tử của oxit là MO.
+) PTHH:
+) Tính theo PTHH lập phương trình ẩn M. Giải phương trình => Kim loại cần tìm
Lời giải:
Gọi M là kí hiệu, nguyên tử khối của kim loại, công thức phân tử của oxit là MO.
Phương trình hoá học của phản ứng:
(M+16)g (M+71)g
10,4g 15,9g
Theo phương trình hoá học trên ta có :
15,9 x (M + 16 ) =10,4 x (M+71)
---> M=88 (Sr)
Nguyên tố kim loại là stronti (Sr)