Tailieumoi.vn giới thiệu Giải sách bài tập Hóa học lớp 8 Bài 11: Luyện tập chương I chi tiết giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 8. Mời các bạn đón xem:
Giải SBT Hóa học 8 Bài 11: Luyện tập chương I
Bài 11. 1 trang 15 SBT Hóa học 8: Viết sơ đồ công thức các hợp chất sau:
H2S, PH3, CO2, SO3
Lời giải:
Sơ đồ công thức các hợp chất H2S, PH3, CO2, SO3 lần lượt là:
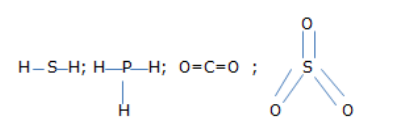
Bài 11. 2 trang 15 SBT Hóa học 8: Cho biết công thức hoá học hợp chất của nguyên tố X với nhóm (SO4) và hợp chất của nhóm nguyên tử Y với H như sau :
X2(SO4)3 ; H3Y.
Hãy chọn công thức hoá học nào là đúng cho hợp chất của X và Y trong số các công thức cho sau đây :
XY2, Y2X, XY, X2Y2, X3Y2.
(a) (b) (c) (d) (e)
Lời giải:
Trong CT: X2(SO4)3 nhóm (SO4) có hóa trị II, gọi hóa trị của X là x
Theo quy tắc hóa trị: x.2 = II.3 ⇒ x = III ⇒ X có hóa trị III.
Và trong H3Y biết H có hóa trị I, gọi hóa trị của Y là y
Theo quy tắc hóa trị: I.3 = y.1 ⇒ y = III ⇒ Y có hóa trị III.
CT hợp chất của X và Y là: XaYb
Theo quy tắc hóa trị : III.a = III.y ⇒ 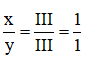
Vậy CT hợp chất X là XY.
⇒ Chọn C
Bài 11. 3 trang 15 SBT Hóa học 8: Lập công thức hoá học và tính phân tử khối của các hợp chất có phân tử gồm Na, Cu(II) và Al lần lượt liên kết với:
a) Brom Br(I).
b) Lưu huỳnh S(II)
Lời giải:
a)Với Br:
* Na và Br(I): Ta có: 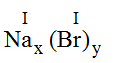
Theo quy tắc: I.x = I.y
Tỉ lệ: 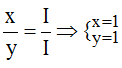
Vậy công thức hóa học của Nax(Br)y là NaBr.
Phân tử khối của NaBr: 23 + 80 = 103 đvC
* Cu(II) và Br(I): Ta có: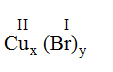
Theo quy tắc: x.II = I.y → 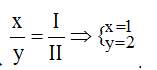 .
.
Vậy công thức hóa học của Cux(Br)y là CuBr2.
Phân tử khối của CuBr2 = 64 + 80.2 = 224 đvC
* Al và Br (I): Ta có: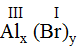
Theo quy tắc: III.x = I.y → 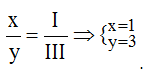 .
.
Vậy công thức hóa học của Alx(Br)y là Al(Br)3.
Phân tử khối của Al(Br)3: 27 + 80.3 = 267 đvC
b) Với S:
* Na và S(II): Ta có:
Theo quy tắc: x.I = II.y → 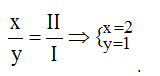 .
.
Vậy công thức hóa học của NaxSy là Na2S.
Phân tử khối = 23.2 + 32 = 78 đvC
* Al và S(II): Ta có: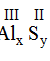
Theo quy tắc: x.III = y.II → 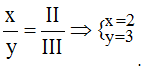 .
.
Vậy công thức của AlxSy là Al2S3.
Phân tử khối = 27.2 + 32.3 = 150 đvC
* Cu(II) và S(II): Ta có: 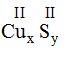
Theo quy tắc: II.x = II.y → 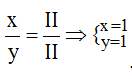 .
.
Vậy công thức hóa học của CuxSy là CuS.
Phân tử khối = 64 + 32 = 96 đvC
Bài 11. 4 trang 16 SBT Hóa học 8: Lập công thức hoá học và tính phân tử khối của các hợp chất có phân tử gồm Ag(I), Mg, Zn và Fe(III) lần lượt liên kết với:
a) Nhóm (NO3).
b) Nhóm (PO4)
Lời giải:
a) Nhóm (NO3):
* Ag và (NO3): Ta có:
Theo quy tắc: x.I = y.I → .
Vậy công thức hóa học của Agx(NO3)y là AgNO3.
Phân tử khối = 108 + 14 + 16.3 = 170 đvC
* Mg và (NO3): Ta có:
Theo quy tắc: x.II = I.y → .
Vậy công thức hóa học của Mgx(NO3)y là Mg(NO3)2.
Phân tử khối của Mg(NO3)2 = 24 + 2.(14 + 16.3) = 148 đvC
* Zn và (NO3): Ta có:
Theo quy tắc: x.II = I.y → .
Vậy công thức hóa học của Znx(NO3)y là : Zn(NO3)2.
Phân tử khối = 65 + 2.(14+ 16.3) = 189 đvC
* Fe (III) và (NO3): Ta có:
Theo quy tắc: x.III = y.I → .
Vậy công thức hóa học của Fex(NO3)y là Fe(NO3)3.
Phân tử khối = 56 + 3.(14 + 16.3) = 242 đvC
b) Nhóm (PO4):
* Ag và (PO4): Ta có:
Theo quy tắc: x.I = III.y →
Vậy công thức hóa học của Agx(PO4)y là Ag3PO4
Phân tử khối = 108.3 + 31 + 16.4 = 419 đvC
* Mg và (PO4): Ta có:
Theo quy tắc: x.I = III.y →
Vậy công thức hóa học là Mg3(PO4)2
Phân tử khối = 24.3 + 2.(31 + 16.4) = 262 đvC
* Zn và (PO4): Ta có: 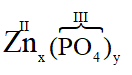
Theo quy tắc: x.I = III.y →
Vậy công thức hóa học là Zn3(PO4)2
Phân tử khối = 65.3 + 2.(31 + 16.4) = 385 đvC
* Fe(III) và (PO4): Ta có:
Theo quy tắc: x.III = y.III →.
Vậy công thức hóa học là FePO4.
Phân tử khối của FePO4 =56 + 31 + 16.4 = 151 đvC
Bài 11. 5 trang 16 SBT Hóa học 8: Công thức hoá học một số hợp chất của nhôm viết như sau :
AICl4 ; AlNO3 ; Al2O3 ; AlS ; Al3(SO4)2 ; Al(OH)2 ; Al2(PO4)3.
Biết rằng trong số này chỉ có một công thức đúng và S có hoá trị II, hãy sửa lại những công thức sai.
Lời giải:
Công thức hoá học đúng : Al2O3.
Sửa lại những công thức sai thành đúng :
AlCl3; Al(NO3)3 ; Al2S3 ; Al2(SO4)3 ; Al(OH)3 ; AlPO4.
Bài 11. 6* trang 16 SBT Hóa học 8: Cho biết tổng số các hạt proton, nơtron và các electron tạo nên nguyên tử một nguyên tố bằng 49, trong đó số hạt không mang điện là 17.
a) Tính số p và số e có trong nguyên tử.
b) Viết tên, kí hiệu hoá học và nguyên tử khối của nguyên tố.
c) Vẽ sơ đồ đơn giản của nguyên tử (xem lại bài tập 4.6*).
Số lớp electron và số electron lớp ngoài cùng có gì giống và khác so với nguyên tử O ? (Xem sơ đồ nguyên tử này trong bài 4. Nguyên tử - SGK).
Phương pháp giải:
a) Trong nguyên tử số p = số e. Mặt khác số n = 17 nên ta có: số p = số e =
b) Xem bảng phụ lục SGK hóa học 8 trang 42
c) Xem lại bài tập 4.6*
Lời giải:
a) Trong nguyên tử vì số p = số e và nơtron là hạt không mang điện, nên theo đề bài, ta có : số p = số e =
b) Tên nguyên tố : lưu huỳnh, kí hiệu hoá học S, nguyên tử khối là 32 đvC.
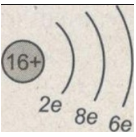
c) Sơ đồ đơn giản của nguyên tử S :
Nguyên tử S có ba lớp electron, khác với nguyên tử O chỉ có hai lớp. Giống với nguyên tử O là cùng có 6e ở lớp ngoài cùng
Bài 11. 7* trang 16 SBT Hóa học 8: Một hợp chất của nguyên tố T hoá trị III với nguyên tố oxi, trong đó T chiếm 53% về khối lượng.
a) Xác định nguyên tử khối và tên nguyên tố T.
b) Viết công thức hoá học và tính phân tử khối của hợp chất.
Phương pháp giải:
Hướng dẫn : Để viết đúng công thức hoá học của hợp chất AxBy phải xác định được các chỉ số x, y. Biết rằng, tỉ lệ phần trăm về khối lượng giữa hai nguyên tố trong hợp chất bằng đúng tỉ lệ khối lượng giữa hai nguyên tố trong 1 phân tử. Từ đây có các tỉ lệ như sau :
Tính và rút gọn thành tỉ lệ hai số nguyên đơn giản nhất, thông thường thì x, y là hai số nguyên này. Ngoài ra, nếu biết trước phân tử khối của AxBy thì xác định được chắc chắn x và y, không tính dựa theo tỉ lệ như trên.
Lời giải:
a) Gọi công thức của hợp chất là T2O3 và x là nguyên tử khối của T. Theo đề bài, ta có :
Tên nguyên tố: nhôm
b) Công thức hóa học của hợp chất:
Phân tử khối bằng: (đvC).
Bài 11. 8* trang 16 SBT Hóa học 8: Hợp chất A tạo bởi hiđro và nhóm nguyên tử (XOY) hoá trị III. Biết rằng phân tử A nặng bằng phân tử H2SO4 và nguyên tố oxi chiếm 65,31% về khối lượng của A.
a) Xác định chỉ số y và nguyên tử khối của nguyên tố X.
b) Viết tên, kí hiệu hoá học của X và công thức hoá học của A.
Phương pháp giải:
a) +) Gọi công thức của A là
+) Tính phân tử khối của H2SO4
+) Phân tử khối của A bằng phân tử khối của H2SO4 nên ta có phương trình:
(đvC)
=> y => phân tử khối của X
b) Dựa vào bảng SGK hóa học 8 trang 42 để xác định tên, kí hiệu và lập công thức hóa học của A
Lời giải:
a) Gọi công thức của A là
Phân tử khối của A bằng: (đvC)
Theo đề bài, ta có:
Nguyên tử khối của X bằng:
(đvC).
b) Tên nguyên tố photpho, kí hiệu hóa học P.
Công thức hóa học của A: .