Tailieumoi.vn giới thiệu Giải bài tập Hóa học 8 Bài 33: Điều chế khí hiđro - Phản ứng thế, chi tiết nhất giúp học sinh dễ dàng làm bài tập Điều chế khí hiđro - Phản ứng thế lớp 8.
a. Zn + H2SO4 → ZnSO4 + H2
b. 2H2O 2H2 + O2
c. 2Al + 6HCl → 2AlCl3 + 3H2
Lời giải:- Phương pháp điều chế hiđro trong phòng thí nghiệm là cho kim loại (đứng trước H trong dãy điện hóa) tác dụng với dung dịch axit HCl hoặc H2SO4 loãng
- Những phản ứng hóa học dưới đây có thể được dùng để điều chế hiđro trong phòng thí nghiệm:
a. Zn + H2SO4 → ZnSO4 + H2
c. 2Al + 6HCl → 2AlCl3 + 3H2
a. Mg + O2 → MgO
b. KMnO4 K2MnO4 + MnO2 + O2
c. Fe + CuCl2 → FeCl2 + Cu
Lời giải:a. 2Mg + O2 → 2MgO
=> Phản ứng oxi hóa - khử (phản ứng hóa hợp)
b. 2KMnO4 K2MnO4 + MnO2 + O2
=> Phản ứng oxi hóa - khử (phản ứng phân hủy).
c. Fe + CuCl2 → FeCl2 + Cu
=> Phản ứng oxi hóa - khử (phản ứng thế)
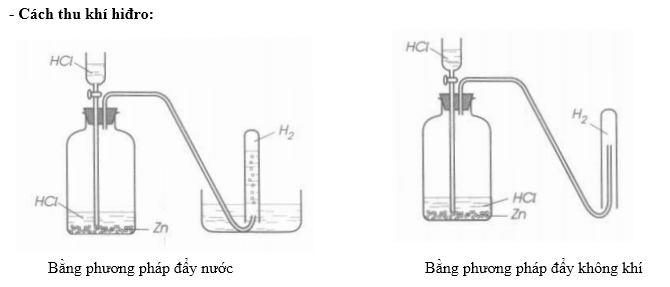
Khi thu khí oxi vào ống nghiệm bằng cách đẩy không khí, phải để vị trí ống nghiệm nằm thẳng đứng, miệng ống nghiệm hướng lên trên vì trọng lượng khí oxi (32g) lớn hơn trọng lượng không khí (29g).
Đối với khí hiđro thì không thể được vì trọng lượng khí hiđro rất nhẹ (2g) so với không khí (29g). Đối với khí H2 thì phải đặt ống nghiệm thẳng đứng và miệng ống nghiệm hướng xuống dưới.
a. Viết phương trình hóa học có thể điều chế hiđro;
b. Phải dùng bao nhiêu gam kẽm, bao nhiêu gam sắt để điều chế được 2,24 lít khí hiđro (ở đktc)?
Lời giải:a. Phương trình hóa học có thể điều chế hiđro.
Zn + 2HCl → ZnCl2 + H2 ↑ (1)
Zn + H2SO4 → ZnSO4 + H2 ↑ (2)
Fe + H2SO4 (loãng) → FeSO4 + H2 ↑ (3)
Fe + 2HCl → FeCl2 + H2 ↑ (4)
b. Số mol khí hiđro là: n = = 0,1 (mol)
Theo phương trình hóa học (1) và (2): nZn = nH2 = 0,1 (mol)
Khối lượng kẽm cần dùng là: m = 0,1x65 = 6,5 (g)
Theo phương trình hóa học (3) và (4): nFe = nH2 = 0,1 (mol)
Khối lượng sắt cần dùng là: m = 0,1x56 = 5,6 (g).
a. Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b. Tính thể tích khí hiđro thu được ở đktc.
a. Số mol sắt là: n = = 0,4 (mol)
Số mol axit sunfuric là: n = = 0,25 (mol)
Phương trình phản ứng:
Fe + H2SO4 → FeSO4 + H2 ↑
1mol 1mol 1mol
0,4 mol 0,25 mol
Ta thấy Fe dư, H2SO4 phản ứng hết
Theo phương trình:
b. Theo phương trình:
1. Điều chế hidro
a. Trong phòng thí nghiệm
- Trong phòng thí nghiệm, khí hiđro được điều chế bằng cách cho axit (HCl hoặc H2SO4 loãng) tác dụng với kim loại kẽm (hoặc sắt, nhôm,…)
- Nguyên liệu:
+ Kim loại: Zn, Fe, Al,…
+ Dung dịch axit: HCl loãng, H2SO4 loãng.
PTHH: Zn + 2HCl → ZnCl2 + H2
b. Trong công nghiệp
* Phương pháp điện phân nước.
2H2O 2H2↑ + O2↑
* Dùng than khử oxi của H2O ở nhiệt độ cao: C + H2O CO + H2
* Điều chế từ khí tự nhiên, khí mỏ dầu.
2. Phản ứng thế
- Phản ứng thế là phản ứng hóa học của đơn chất và hợp chất trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất
Ví dụ: PTHH: Zn + 2HCl → ZnCl2 + H2
(đơn chất) (hợp chất) (hợp chất) (đơn chất)
Nhận xét: Nguyên tử Zn đã thay thế nguyên tử H trong hợp chất HCl.
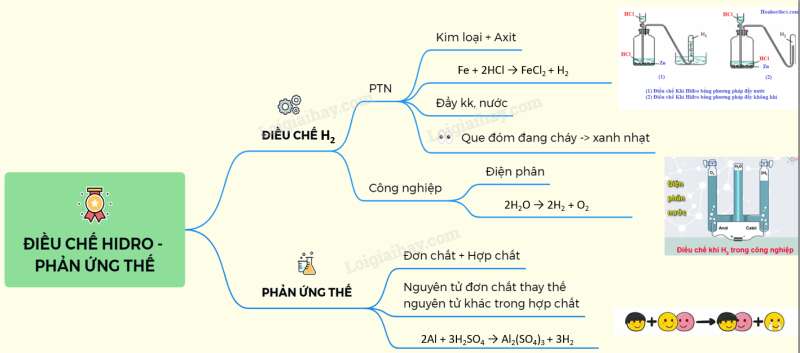
Sơ đồ tư duy: Điều chế khí hiđro - phản ứng thế