Tailieumoi.vn xin giới thiệu Trắc nghiệm Hóa học lớp 10 Bài 14: Ôn tập Chương 3 sách Kết nối tri thức. Bài viết gồm 20 câu hỏi trắc nghiệm với đầy đủ các mức độ và có hướng dẫn giải chi tiết sẽ giúp học sinh ôn luyện kiến thức và rèn luyện kĩ năng làm bài trắc nghiệm Hóa học 10. Ngoài ra, bài viết còn có phần tóm tắt nội dung chính lý thuyết Bài 14: Ôn tập Chương 3. Mời các bạn đón xem:
Trắc nghiệm Hóa học 10 Bài 14: Ôn tập Chương 3
Phần 1: Trắc nghiệm Ôn tập Chương 3
Câu 1. Phát biểu nào sau đây là đúng?
A. Liên kết cộng hóa trị phân cực có thể được coi là dạng trung gian giữa liên kết cộng hóa trị không phân cực và liên kết cho – nhận.
B. Liên kết ion có thể được coi là dạng trung gian giữa liên kết cộng hóa trị không phân cực và liên kết cộng hóa trị phân cực.
C. Liên kết cộng hóa trị không phân cực có thể được coi là dạng trung gian giữa liên kết cộng hóa trị phân cực và liên kết ion.
D. Liên kết cộng hóa trị phân cực có thể được coi là dạng trung gian giữa liên kết cộng hóa trị không phân cực và liên kết ion.
Đáp án: D
Giải thích:
Liên kết cộng hóa trị phân cực có thể được coi là dạng trung gian giữa liên kết cộng hóa trị không phân cực và liên kết ion.
Câu 2. Liên kết đơn là liên kết
A. có một cặp electron dùng chung.
B. có hai cặp electron dùng chung.
C. có ba cặp electron dùng chung.
D. có bốn cặp electron dùng chung.
Đáp án: A
Giải thích:
Liên kết đơn là liên kết có một cặp electron dùng chung, được biểu diễn bằng một gạch nối (–).
Chú ý:
Liên kết đôi là liên kết có hai cặp electron dùng chung, được biểu diễn bằng hai gạch nối (=).
Liên kết ba là liên kết có ba cặp electron dùng chung, được biểu diễn bằng ba gạch nối (º).
Câu 3. Liên kết ba gồm
A. ba liên kết s.
B. hai liên kết s và một liên kết p.
C. hai liên kết s và hai liên kết p.
D. một liên kết s và hai liên kết p.
Đáp án: D
Giải thích:
Liên kết ba (º) gồm một liên kết s và hai liên kết p.
Câu 4. Cho các chất sau: N2, HCl, HF, O2, Cl2. Trong các chất trên, có bao nhiêu chất mà liên kết trong phân tử là liên kết cộng hóa trị không phân cực?
A. 1.
B. 2.
C. 3.
D. 4.
Đáp án: C
Giải thích:
Liên kết cộng hóa trị không phân cực là liên kết trong các phân tử mà cặp electron dùng chung không bị hút lệch về phía nguyên tử nào.
Liên kết trong phân tử N2, O2, Cl 2 là liên kết cộng hóa trị không phân cực.
Chú ý: Liên kết trong phân tử HCl, HF là liên kết cộng hóa trị phân cực (cặp electron chung bị lệch về phía nguyên tử có độ âm điện lớn hơn là Cl, F).
Câu 5. Công thức cấu tạo của phân tử N2 là
A. N – N.
B. N=N.
C. N®N.
D. NºN.
Đáp án: D
Giải thích:
Phân tử nitrogen (N2):
Nguyên tử nitrogen có 5 electron hóa trị, hai nguyên tử nitrogen liên kết với nhau bằng cách mỗi nguyên tử nitrogen đóng góp 3 electron, tạo thành 3 cặp electron dùng chung. Khi đó, trong phân tử N2, mỗi nguyên tử đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.

Giữa hai nguyên tử nitrogen có ba cặp electron dùng chung (biểu diễn bằng ba gạch nối), đó là liên kết ba.
Câu 6. Liên kết hóa học được tạo thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung là
A. liên kết ion.
B. liên kết cộng hóa trị.
C. liên kết hydrogen.
D. liên kết kim loại.
Đáp án: B
Giải thích:
Liên kết cộng hóa trị được tạo thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung.
Câu 7. Liên kết cộng hóa trị phân cực là liên kết trong các phân tử mà
A. cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn.
B. cặp electron dùng chung lệch về phía nguyên tử có độ âm điện nhỏ hơn.
C. cặp electron dùng chung không bị hút lệch về phía nguyên tử nào.
D. cặp electron chung được đóng góp từ một nguyên tử.
Đáp án: A
Giải thích:
Liên kết cộng hóa trị phân cực là liên kết trong các phân tử mà cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn.
Ví dụ: Liên kết trong phân tử HCl là liên kết cộng hóa trị phân cực, cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn (Cl).
Chú ý: Liên kết cộng hóa trị không phân cực là liên kết trong các phân tử mà cặp electron dùng chung không bị hút lệch về phía nguyên tử nào.
Ví dụ: Liên kết trong phân tử Cl2, O2, N2, … là liên kết cộng hóa trị không phân cực.
Câu 8. Liên kết hydrogen và tương tác van der Waals
A. đều làm tăng nhiệt độ sôi và nhiệt độ nóng chảy.
B. đều làm giảm nhiệt độ sôi và nhiệt độ nóng chảy.
C. đều làm tăng nhiệt độ sôi và làm giảm nhiệt độ nóng chảy.
D. đều làm giảm nhiệt độ sôi và làm tăng nhiệt độ nóng chảy.
Đáp án: A
Giải thích:
Liên kết hydrogen và tương tác van der Waals đều làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Câu 9. Trong các liên kết: liên kết cộng hóa trị không phân cực, liên kết cộng hóa trị phân cực và liên kết ion thì độ phân cực liên kết
A. giảm dần.
B. tăng dần.
C. giống nhau.
D. gần giống nhau.
Đáp án: B
Giải thích:
Trong các liên kết: liên kết cộng hóa trị không phân cực, liên kết cộng hóa trị phân cực và liên kết ion thì độ phân cực liên kết tăng dần.
Câu 10. Liên kết cộng hóa trị không phân cực thường có hiệu độ âm điện (|Dc|) trong khoảng nào sau đây?
A. |Dc| ≥ 1,7.
B. 0,4 ≤ |Dc| < 1,7.
C. 0 ≤ |Dc| < 0,4.
D. |Dc| ≥ 2,8.
Đáp án: C
Giải thích:
0 ≤ |Dc| < 0,4: Liên kết cộng hóa trị không phân cực.
0,4 ≤ |Dc| < 1,7: Liên kết cộng hóa trị phân cực.
|Dc| ≥ 1,7: Liên kết ion.
Câu 11. Liên kết trong phân tử nào sau đây là liên kết ion?
A. CO2.
B. O2.
C. KCl.
D. HCl.
Đáp án: C
Giải thích:
Liên kết ion trong phân tử hay tinh thể được tạo thành nhờ lực hút tĩnh điện của các ion mang điện tích trái dấu. Liên kết ion thường tạo thành từ các nguyên tử kim loại điển hình và phi kim điển hình, phân tử thu được là hợp chất ion.
Liên kết trong phân tử KCl là liên kết ion.
Câu 12. Số liên kết s và liên kết p có trong phân tử C2H2 lần lượt là
A. 3 và 3.
B. 3 và 2.
C. 2 và 3.
D. 2 và 2.
Đáp án: B
Giải thích:
Công thức cấu tạo của C2H2 là: H–CºC–H.
Liên kết ba (º) gồm một liên kết s và hai liên kết p.
Phân tử C2H2 có 3 liên kết s và 2 liên kết p.
Câu 13. Nhận xét nào sau đây không đúng khi nói về phân tử CO2?
A. Liên kết giữa C và O là liên kết cộng hóa trị phân cực.
B. Phân tử CO2 có công thức cấu tạo là O=C=O.
C. Phân tử CO2 có cấu tạo thẳng.
D. Phân tử CO2 là phân tử phân cực.
Đáp án: D
Giải thích:
Trong phân tử CO2, hiệu độ âm điện của O và C: 3,44 – 2,55 = 0,89.
=> Liên kết giữa C và O là liên kết cộng hóa trị phân cực. Tuy nhiên, do phân tử CO2 có cấu tạo thẳng nên độ phân cực của hai liên kết đôi (C=O) triệt tiêu nhau, dẫn đến toàn bộ phân tử không bị phân cực.
Câu 14. Cho biết c(Mg) = 1,31 và c(Cl) = 3,16. Dự đoán loại liên kết trong phân tử MgCl2.
A. Liên kết cộng hóa trị phân cực.
B. Liên kết cộng hóa trị không phân cực.
C. Liên kết ion.
D. Liên kết cho – nhận.
Đáp án: C
Giải thích:
Trong phân tử MgCl2, hiệu độ âm điện cuả Cl và Mg là: 3,16 – 1,31 = 1,85 > 1,7.
=> Liên kết trong phân tử MgCl2 là liên kết ion.
Câu 15. Cho biết c(H) = 2,20 và c(Br) = 2,96. Dự đoán loại liên kết trong phân tử HBr.
A. Liên kết cộng hóa trị phân cực.
B. Liên kết cộng hóa trị không phân cực.
C. Liên kết ion.
D. Liên kết cho – nhận.
Đáp án: A
Giải thích:
Trong phân tử HBr, hiệu độ âm điện giữa Br và H là: 2,96 – 2,20 = 0,76.
=>0,4 ≤ |Dc| < 1,7 =>Liên kết trong phân tử HBr là liên kết cộng hóa trị phân cực.
Phần 2: Lý thuyết Ôn tập Chương 3
I. Liên kết ion
1. Khái niệm
Liên kết ion trong phân tử hay tinh thể được tạo thành nhờ lực hút tĩnh điện của các ion mang điện tích trái dấu. Liên kết ion thường tạo thành từ các nguyên tử kim loại điển hình và phi kim điển hình, phân tử thu được là hợp chất ion.
Chú ý:
Nguyên tử kim loại nhường electron để tạo thành ion mang điện tích dương (cation) còn nguyên tử phi kim nhận electron để trở thành ion mang điện tích âm (anion).
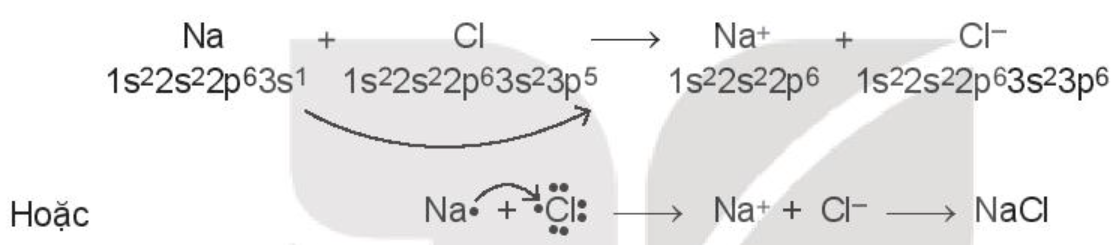
Ví dụ: Xét sự tạo thành liên kết hóa học trong phân tử sodium chloride (NaCl):
Khi kim loại sodium kết hợp với phi kim chlorine, tạo thành các ion Na+ và Cl-, các ion này mang điện tích trái dấu sẽ hút nhau tạo thành liên kết ion.
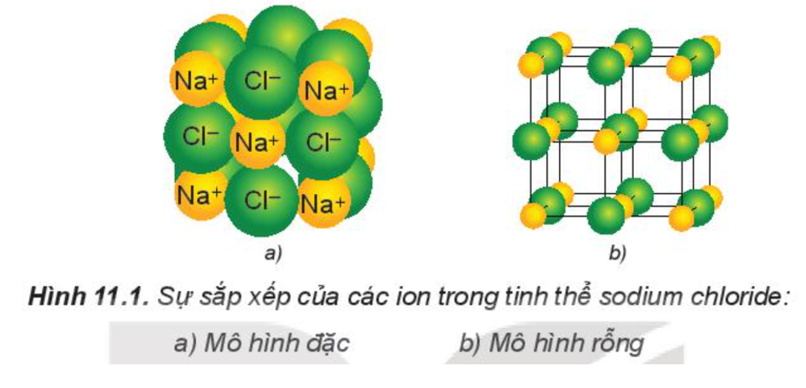
2. Tinh thể ion
Cấu trúc của mạng tinh thể ion: các ion được sắp xếp theo trật tự nhất định trong không gian theo kiểu mạng lưới (ở các nút mạng là các ion dương và ion âm xếp luân phiên liên kết chặt chẽ với nhau do cân bằng lực hút và lực đẩy).
Ví dụ: Tinh thể muối ăn.
II. Liên kết cộng hóa trị
1. Một số khái niệm
- Liên kết cộng hóa trị được tạo thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung.
Kiểu liên kết: Liên kết đơn (–), liên kết đôi (=), liên kết ba (º).
- Liên kết cộng hóa trị không phân cực là liên kết trong các phân tử mà cặp electron dùng chung không bị hút lệch về phía nguyên tử nào.
Ví dụ: Liên kết trong phân tử Cl2, O2, N2, … là liên kết cộng hóa trị không phân cực.
- Liên kết cộng hóa trị phân cực liên kết trong phân tử mà cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn.
Ví dụ: Liên kết trong phân tử HCl là liên kết cộng hóa trị phân cực, cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn (Cl).
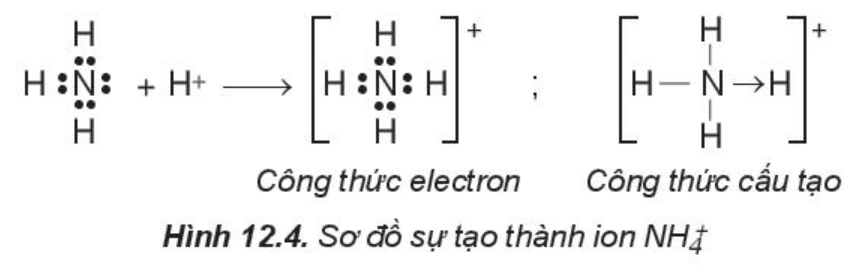
- Liên kết cho – nhận là liên kết mà cặp electron chung được đóng góp từ một nguyên tử.
Ví dụ:
2. Độ âm điện và liên kết hóa học
Dựa vào sự khác nhau về độ âm điện giữa các nguyên tử tham gia liên kết, có thể dự đoán được loại liên kết giữa hai nguyên tử đó.

III. Liên kết hydrogen và tương tác van der Waals
1. Khái niệm
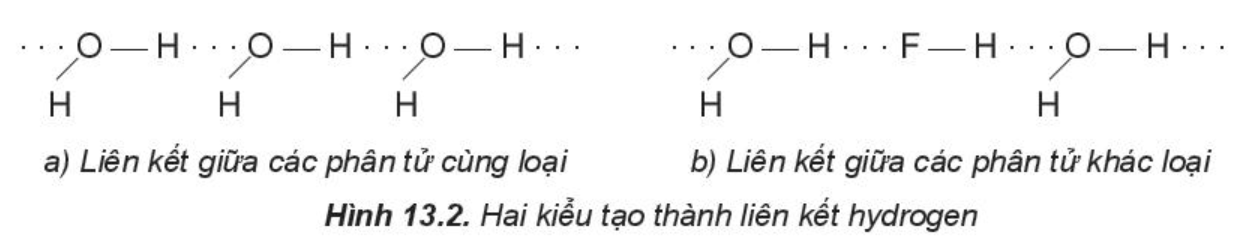
- Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia liên kết.
Ví dụ:
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực giữa các nguyên tử hay phân tử.
Ví dụ: Ở trạng thái lỏng, giữa các phân tử bromine tồn tại một tương tác yếu là tương tác van der Waals.
2. Ảnh hưởng của liên kết hydrogen và tương tác van der Waals
Liên kết hydrogen và tương tác van der Waals đều làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Xem thêm các bài trắc nghiệm Hóa học 10 Kết nối tri thức hay, chi tiết khác:
Trắc nghiệm Bài 13: Liên kết hydrogen và tương tác van der Waals
Trắc nghiệm Bài 14: Ôn tập chương 3
Trắc nghiệm Bài 15: Phản ứng oxi hóa – khử
Trắc nghiệm Bài 16: Ôn tập chương 4
Trắc nghiệm Bài 17: Biến thiên enthalpy trong các phản ứng hóa học